天下第一痛之三叉神经痛!诊疗进展请收藏!
时间:2023-05-19 20:43:01 热度:37.1℃ 作者:网络
三叉神经痛 (trigeminal neuralgia, TN)三叉神经痛是最常见的脑神经疾病,以一侧面部三叉神经分布区内反复发作的阵发性剧烈痛为主要表现,国内统计的发病率52.2/10万,女略多于男,发病率可随年龄而增长。三叉神经痛多发生于中老年人,右侧多于左侧。
三叉神经是由特殊内脏运动神经纤维和一般躯体感觉纤维组成的混合型神经,感觉神经主要 感知面部、口腔及额顶部的感觉,而运动神经主要支配咀嚼肌的运动。
三叉神经分为第一支眼神经、 第二支上颌神经、第三支下颌神经见图1。在临床诊疗工作中,TN 常累及上、下颌的牙齿,病人往往首先就诊口腔科,由于诊断、治疗的不规 范,常导致牙齿不可逆性的治疗或拔除。
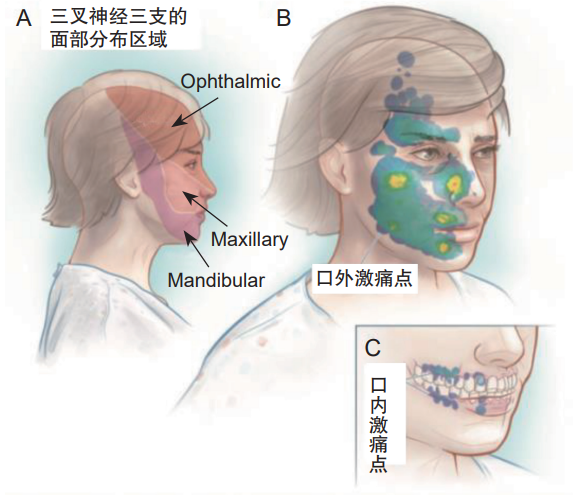
图1.三叉神经三支的面部分布区域及激痛点示意图 Ophthalmic:眼支;Maxillary:上颌支;Mandibular:下颌支。
同时,随时间的延长,三叉神经疼痛发生频率增加,疼痛时 间延长,严重影响病人的生活质量,一部分病人会出现抑郁、焦虑等精神症状,严重者可导致病人自 杀。
尽管国内外对三叉神经痛的研究已经较深入, 但其病因和发病机制仍不十分清楚。虽然TN的治 疗方法多样,但治疗效果却差异较大。近年来对 TN 的临床研究尤其是系统规范的诊疗愈来愈受到重视,新技术新理念进展较快。
本文通过总结国内外关于三叉神经痛的研究现状,对发病机制及诊疗 技术、诊疗理念的新进展以及治疗方法的选择作一 综述,以期为三叉神经痛的临床治疗提供参考依据。
三叉神经痛的病因和发病机制
目前三叉神经痛的病因及发病机制认识尚不一 致。原发性TN的病理生理学假说认为,TN 的发病机制是由血管(动脉或静脉)近端压迫脑干附近的三叉神经感觉根引起的(微血管压迫学说)。
由于外周施万细胞髓鞘向少突胶质细胞形成的中央髓鞘的转变,神经根进入区被认为是易发生脱髓鞘的脆弱区域。血管压迫可能启动局灶性脱髓鞘和再髓鞘化过程,这个过程可能由微血管缺血损伤介导。
这些局部的变化降低了受影响神经纤维的兴奋性阈值,并促进了向邻近纤维的不适当的突触传播。从而导致来自快速有髓 (A-β) 纤维的触觉信号可以 直接激活缓慢的伤害性 (A-δ) 纤维,引起 TN 的高频发作。
几秒钟后,这些重复性放电会自动消失, 然后是一段短暂的不活动期,称为“不应期”,在这段时间内,触发动作不会引起疼痛。
近年的研究表明,钠离子通道阻滞剂在 TN 中 的显著临床效果表明电压门控钠离子通道的异常表 达亦是经典型和特发性 TN 的重要病理生理变化。
研究发现,钠离子通道相关的 Nav1.7、Nav1.3 和 Nav1.8 等在 TN 中异常表达,这可能与动作电位的 快速激活、失活以及维持有关。
触觉 A-β 纤维的 过度长时间敏感性可能导致背角 V 层和三叉神经核 团的二级相关的神经元的高敏感性。而这些二级相 关神经元可接收来自触觉 (A-β) 和疼痛感受(A-δ 和 C)纤维的会聚信息从而导致其敏感性提高,从而提高其对皮肤刺激的疼痛感知。
在原发性及特发性 TN 中,伴有持续性疼痛 TN 与单纯阵发性疼痛的 TN 在病理生理学上是不同的。
既往曾认为伴随有持续性疼痛的 TN 是阵发性 疼痛的重复发作,而目前一项前瞻性研究表明,伴 随有持续性疼痛的 TN 一般在阵发性疼痛发作时或发作之前就已经发生。与阵发性 TN 相比,伴有持续性疼痛的 TN 在女性常见,且有更明显的感觉异常。
研究显示,三叉神经损伤性感觉障碍往往与 异常的伤害性眨眼反射及疼痛相关诱发电位有关,这表明过度激活中枢感觉传导是引起持续面部疼 痛的潜在机制。
最近的一项神经影像学研究使用 MR 分别对纯阵发性 TN 和伴发持续性疼痛 TN 病 人进行三叉神经根检测,结果表明伴发持续性疼痛病人的三叉神经根萎缩程度比单纯阵发性疼痛病人更严重,研究者推测持续性疼痛的发病机制可能与去神经的三叉神经二级神经元的轴突丢失和异常活动有关,这与既往 TN 发病机制的神经变性学说的理论相似。
既往的理论中,关于 TN 发病机 制还有癫痫学说、病灶感染和牙源性学说等理论,因其近年来这些方面的研究进展较少,在此不再作赘述。
三叉神经痛的流行病学分类
TN 的终生患病率为 0.16%~0.3%,而年发病 率为 4~29/10 万人。女性发病率高于男性(女 : 男 比率为 3:2),发病率随年龄增长而增加,平均发病年龄为 53~57 岁,成人发病年龄常见为 24~93 岁。
根据发病的原因,TN 可分为经典型(原发性)、继发性及特发性。经典型(原发性)是最常见的 类型,占全部病例的 75%。
无论是在 MR 检查还是 在手术时,当发现三叉神经血管压迫并伴有疼痛同 侧的形态学改变时,即可诊断为经典型,而单纯三叉神经接触而无形态学改变的常见神经影像学表现 不支持此诊断。
同时前瞻性三叉神经 MR 研究表明,在症状侧经典型 TN 与神经血管压迫并伴有形态学 改变(扭曲、萎缩)有关,而在无症状侧这些形态 学改变很少见。
继发性(占病例的 15%)往往可归因于一种可明确的潜在神经疾病(三叉神经血管 压迫除外),多为已知可引起 TN 的桥小脑角肿瘤、 动静脉畸形及多发性硬化等疾病,其改变三叉神经 根进入区或以其他方式压迫颅外神经。
有 2% 的多发性硬化症病人有与经典型 TN 相似的症状。而 当无法找到 TN 的明显原因时,即可诊断为特发性 类型,占病例的 10%。详细分类见图2。
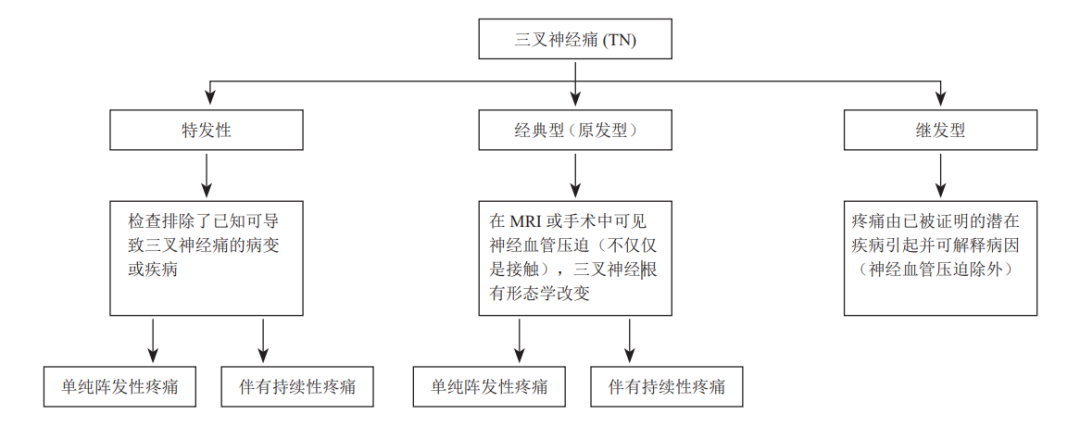
图2.三叉神经痛的分类
根据发作间期是否存在持续疼痛、特发性和经 典性 TN 可进一步细分为亚类。伴有持续疼痛的 TN 发生在 14%~50% 的病人中。
最近的研究表明,伴有持续性疼痛TN与单纯阵发性疼痛TN在病理生理学上是不同的,且伴有持续性疼痛TN的治疗效果不佳因此临床上有必要区分这两种亚型 。
经典型TN和继发性TN的临床特征相似,但继发性TN病人通常更年轻,更可能出现面部感觉丧失,更容易出现双侧疼痛。由于三叉神经痛的 三种形式在临床上可能不易识别,建议在最初诊断时进行磁共振成像 (MRI),以排除多发性硬化症和 桥小脑肿块。
TN的诊断标准及诊断考量因素
2018 年,《国际头痛障碍分类》第3版(ICHD-3) 中规定的TN诊断标准为:
反复发作的单侧 面部疼痛,部位局限于三叉神经分布的区域;
疼痛具有以下所有特点:持续时间从 1 秒至 2 分钟;严重强度的疼痛;伴有电击、枪击、刺伤或尖锐刺 激样疼痛;
由三叉神经分布区域内的无害刺激诱发。
触发性阵发性疼痛是三叉神经痛特有的症状,91%~99% 的病人报告了这种症状,表明这种症状 可能是三叉神经痛的病理特征。
三叉神经痛多由日常生活中常见的无痛性接触引发,而这些触发因素,如餐巾接触上唇、甚至微风吹过面部敏感区域,均可诱发疼痛,且疼痛的位 置并不一定与激痛点一致。
临床上常见下唇及周围的刺激可能会诱发太阳穴疼痛,或者鼻子外侧接触可导致前额或上唇周围的电击性疼痛。具体激痛点见图1 。
目前因没有明确的实验室检测指标,TN 的诊断主要基于病史。病史采集应特别注意可能导致误 诊的因素,如疼痛的症状、原因、牙源性疼痛和相 关的自主神经症状。
收集病史应特别关注疼痛的开始时间:如果疼痛先于或同步同侧三叉神经分布的 带状疱疹皮疹引起的疼痛,则应考虑急性带状疱疹 引起的疼痛性三叉神经病变。
侵入性牙科操作或骨折等创伤可引起三叉神经区域的疼痛,诊断为创 伤后疼痛性三叉神经病变更为合理。
研究表明,创伤后三叉神经病变中的疼痛可与短暂、强烈触发痛TN的疼痛程度相当,但前者通常存在明确的感觉异常及与受损的周围神经相对应的感觉功能丧失。
采集病史时疼痛的位置也很重要,定位明确的或弥漫性牙齿疼痛应由口腔科医师进行评估。如牙裂的牙齿可能会在咀嚼硬食物引起 TN 样疼痛。
而对于双侧颞下颌区的持续性疼痛,应考虑紧张型头痛、 颞下颌关节紊乱和特发性持续性面部疼痛。如果短 暂、剧烈刺痛仅限于头皮或枕部,则应考虑诊断为 枕神经痛、原发性刺痛性头痛和阵发性偏头痛。
舌咽神经痛多位于舌背、软腭和咽部,中间神经痛位 于耳深处。最后,病史采集时病人的伴随症状亦很重要,如每次疼痛发作都伴有自主神经症状,如结膜充血、瞳孔缩小或流泪,短暂单侧神经痛样头痛 发作伴结膜充血和流泪、短暂单侧神经痛样头痛发 作伴头面部自主神经症状或阵发性偏头痛是重要的 鉴别诊断。常见的鉴别诊断见表1。
表1.三叉神经痛的鉴别诊断

三叉神经痛的治疗策略
药物治疗
目前,抗惊厥药物卡马西平和奥卡西平被认为是控制三叉神经痛病人阵发性疼痛的首选治疗方法。
临床应用效果显示在 90% 的病人中这些药物可明显控制疼痛,可取得良好的治疗效果。
其机制主要是药物可阻断电压门控钠离子通道,从而稳定过度 兴奋的神经元膜并抑制竞争性放电。
卡马西平和 奥卡西平可以减少电击样发作的高频放电,但这些 药物对持续性疼痛的作用通常是有限的。
此外,抗惊厥药物(钠离子通道阻滞剂)治疗往往伴有多种并发症,包括头晕、复视、共济失调以及氨基转 移酶升高,其中一种或多种并发症可导致 23% 的病人退出治疗。
与卡马西平相比,奥卡西平的不良 反应更少,药物相互作用更小,病人的耐受度更 高,奥卡西平愈来愈受到病人的选择。
此外,临床研究证明加巴喷丁、普瑞巴林和 抗抑郁药在治疗以持续疼痛为特征的神经病变方 面有效,可与奥卡西平或卡马西平等钠离子通道阻滞剂联合应用于临床。
普瑞巴林和加巴喷丁的作用机制相同,主要是通过抑制中枢神经系统电压依赖 性钙通道的亚基 α2δ 蛋白,减少钙离子内流,减少兴奋性递质的释放,使过度兴奋的神经元恢复正常状态。
临床经验表明,加巴喷丁对三叉神经痛的疗效略逊于卡马西平和奥卡西平,但不良事件发 生率低,可尝试作为单一疗法或附加疗法应用于三 叉神经痛的治疗。
根据国际指南,建议“如果任何一种钠通道阻滞剂无效,合理的治疗将是转诊咨询手术治疗”。
同时当药物虽然有效,但由于服用足量的药物可引起严重不良反应时,也应考虑进行手术。
然而,从临床的角度来看,可首先尝试应用卡马西平和奥卡西平进行治疗 TN。此外,联合卡马西平或奥卡西平与拉莫三嗪、巴氯芬、普瑞巴林或加巴喷丁的附加治疗亦可使 TN 病人获得良好的疗效。
因此,在临床上卡马西平或奥卡西平因不良反应不能达到全剂量服用时,应考虑联合治疗。如果一个疗程药物治疗无效或伴有不可接受的药物不良反应,可以考虑三叉神经手术。
手术治疗
(1)微血管减压术:
目前,微血管减压术已 成为大多数三叉神经痛病人(药物治疗无效)的首 选外科治疗方法。
该手术需要开颅及后颅窝探查, 确定受影响的三叉神经和识别压迫三叉神经根的血管,必要时将其从神经下方移到神经上方,并通常插入一小块海绵,使搏动动脉与神经根分离。
与其他外科手术相比,微血管减压术可获得更长的无疼痛持续时间。
研究表明,微血管减压是治疗经 典三叉神经痛最有效的手术干预。术后 1~2 年,68%~88% 的病人疼痛缓解,61%~80% 的病人在 4~5 年时疼痛缓解。
与手术相关的平均死亡率 为 0.3%,脑脊液漏发生率为 2.0%,脑干梗死或血 管瘤发生率为 0.6%,脑膜炎发生率为 0.4%,2.9% 的病人面部三叉神经感觉部分或全部丧失。
另据报道,5 年后 73% 的病人疼痛得到显著缓解;2%~7% 的病人出现新的疼痛或灼痛、感觉丧失和 其他轻微或短暂的颅神经功能障碍等轻微并发症。MVD 主要并发症如颅神经功能异常 (2%)、卒中 (0.3%) 和死亡 (0.2%) 在临床上少见。
近年来,显微血管减压术、内镜下血管减压术等微创技术在 临床逐步推广使用。郝海涛等的研究发现在 27 例三叉神经痛病人中,术中显微镜下可确认责任血 管 19 例,神经内镜确认责任血管 6 例,全程探查三叉神经脑池段后未见明确责任血管 2 例。
显微镜难以观察责任动脉时,神经内镜可以清楚显示三叉神经根部解剖情况,明确责任动脉。神经内镜可提供更多的观察角度,辅助显微血管减压术治原发性 三叉神经痛的效果良好。
(2)立体定向放射治疗:
立体定向放射外科 (“伽玛刀”)治疗需要在三叉神经根进入桥脑之前准确识其位置并采用辐射束进行精准的照射,可损伤三叉神经根从而起到治疗的目的,避免损坏桥脑。
伽玛刀立体定向放射外科术需要 6~8 周的时间缓解疼痛作用,24%~71% 的病人报告在术 后 1~2 年仍有持续疼痛缓解,33%~56% 的病人 在术后 4~5 年可持续缓解疼痛。
据报道,16% 的病人出现面部麻木,而疼痛没有得到有效缓解。一项荟萃分析结果显示 34% 的病人在 1 年后疼痛无缓解,需要重新接受治疗。
术后 5 年的复查结果显示,“伽玛刀”手术对 50% 的病人有效,同时感觉丧失 (12%~50%)、咀嚼障碍并发症(球囊压迫 高达 50%)和新的烧灼样疼痛 (12%) 等轻微并发症相对普遍。
(3)经皮微创介入治疗:
经皮射频热凝术、球 囊压迫术等技术可对梅克尔 (Meckel) 腔中的三叉神 经节或颅神经节的现有分支产生损伤或撕脱。
射频热凝术优先损伤小直径疼痛纤维,为防止传入神经阻滞引起角膜炎,术中要避免损伤三叉神经的第一分支眼神经。
球囊压迫优先损伤大的有髓神经纤 维。这些治疗方法可立即缓解疼痛,据报道,68% 的病人采用球囊压迫(随访 4.2~10.7 年),58% 的病人采用射频热凝(随访 3.0~9.3 年),28% 的病人采用甘油神经毁损术(随访 4.5~8.0 年)。
球囊压迫术后三叉神经感觉缺失通常是短暂的,但射频热凝后感觉丧失更严重,持续时间更长。
(4)经皮射频热凝术:
射频热凝术的原理是局部射 频加热到 70~75℃可导致三叉神经中传导痛觉的无髓纤维(Aδ 和 C 类纤维)变性,而主导传导触觉 的有髓粗纤维可耐受高温不发生变性,因此局部控制温度可以有选择的破坏痛觉纤维,从而缓解或消 除疼痛,达到治疗的目的。
乔梁等在神经导航 精准穿刺的基础上在射频毁损之前应用神经电生理 监测刺激诱发病人感觉异常,进而确认感觉异常范围与疼痛范围界限,精准确认毁损位置,提高了射频热凝术成功率,进一步控制术后并发症的产生。
(5)经皮球囊压迫术:
该技术采用介入微创的方法 可选择性导致中、大型有髓鞘痛觉神经纤维的损伤, 而有髓鞘和无髓鞘神经纤维免受损伤,可有效切断 三叉神经传导通路,从而明显缓解疼痛。
球囊压迫 时间对疼痛控制及并发症产生有很大影响。有学者指出压迫时间 > 10 分钟可导致病人面部感觉发生严重障碍,压迫时间 1~3 分钟在疗效上并无显著性差异,但压迫超过 3 分钟就有可能会增加病 人术后并发症发生率。
文献证实,该技术术后即刻的有效率为 82.0%~93.8%,4 年内疼痛控制率为 69.4%,10 年内复发率为 31.9%。
复发病人可再次 采用球囊压迫术,可获得一定效果,83.0%~93.8% 的复发病人即刻疼痛缓解,5 年内 54.5% 的病人疼痛 完全缓解。
(6)其他治疗:
三氧注射治疗、富血小板血浆 (platelet rich plasma, PRP) 注射、 等离子治疗。三氧是一种强氧化剂,具有较好的抗炎、杀菌和镇痛等作用。
三氧注射 (ozone therapy, OT) 对于难治性三叉神经痛的治疗安全有效,一般采取传统 Hartel 或改良 Hartel 前入路,在CT引导下将三氧气体注入病人梅克尔 (Meckel) 腔内,通过抗炎和修 复 Meckel 腔内的神经纤维而达到镇痛的目的。
李彤等采用 Meckel 腔内注射三氧治疗三叉神经痛的研究结果表明三叉神经痛多累及第 2、3 支,第 1 支较为少见,这与 Oliviero 等研究结果一致。
三氧注射具有疗效好、创伤小、并发症少等优点。对于需要保留面部正常感觉和肌肉功能的病人尤其适用。
PRP 含有大量生物活性生长因子,能够促进组织修 复和周围神经再生,消除创伤愈合不良所导致的慢 性外周神经源性疼痛。
刘春影等、袁林等的研究中均指出,炎性调节因子不但可以减轻或消除神经源性炎症,还可减轻神经损伤后的肿胀反应,减轻炎性疼痛的同时还可为神经再生提供更好的环境。
田德民等在CT引导下行经皮穿刺三叉神经节注射 PRP,发现可有效减轻三叉神经痛病人的疼痛程度,并可改善神经功能。由于临床应用在初始 应用阶段,尚需后续更多临床试验结果证实。
小结
TN 是可引起明显疼痛不适的疾病,治疗方法众多,卡马西平和奥卡西平是 TN 的一线治疗选择, 但长期用药存在疗效减退和药物不良反应的弊端;外科干预虽占据较为重要的地位,但由于存在较大的创伤,部分病人难以接受。
在未来的诊疗中,应更加注重微创治疗,不断尝试新的治疗方式,以期为三叉神经的诊疗提供更加有效的治疗选择。
参考文献
[1] Cruccu G, Di Stefano G, Truini A. Trigeminal neuralgia[J]. N Engl J Med, 2020, 383(8):754-762.
[2] 崔艳魁 , 程鹏 , 刘玉川 , 等 . 微血管减压与感觉根部分切断治疗三叉神经痛效果评价 [J]. 中国疼痛医学杂志 , 2019, 25(3):181-186.
[3] 荣道建 , 张海波 , 姜雪 , 等 . 神经导航下经皮选择性半月神经节射频热凝治疗三叉神经痛 [J]. 中国疼痛医学杂志 , 2020, 26(8):612-615.
[4] Sahoo NK, Thakral A, Deb P, et al. Histopathologicalevaluation of inferior alveolar neurovascular bundlein cases of trigeminal neuralgia[J]. J Maxillofac OralSurg, 2020, 19(1):54-60.
[5] Perez G, Sanchez R, Sampath R. Trigeminal neuralgiafrom simultaneous compression by cerebellopontineangle epidermoid and duplicated superior cerebellarartery loop: two-dimensional operative video of rep and microvascular decompression with endoscopicassistance[J]. World Neurosurg, 2022, 163:67.
[6] Siqueira SRDT, Alves B, Malpartida HMG, et al. Abnormal expression of voltage-gated sodium channels Nav1.7, Nav1.3 and Nav1.8 in trigeminal neuralgia[J].Neuroscience, 2009, 164:573-577.
[7] Chen Q, Yi DI, Perez JNJ, et al. The molecular basis and pathophysiology of trigeminal neuralgia[J]. Int J Mol Sci, 2022, 23(7):3604.
[8] 孟岚 , 任浩 , 赵春美 , 罗芳 . 射频热凝和脉冲射频治疗三叉神经痛疗效和安全性评价 [J]. 中国疼痛医学杂志 , 2021, 27(12):898-904.
[9] 杨娟 , 高翃 , 罗裕辉 , 等 . 经圆孔射频热凝上颌神经治疗三叉神经痛的临床观察 [J]. 中国疼痛医学杂志 ,2019, 25(5):357-360.
[10] Müller S, Khadhraoui E, Khanafer A, et al. Differen tiation of arterial and venous neurovascular conflicts estimates the clinical outcome after microvascular de compression in trigeminal neuralgia[J]. BMC Neurol,2020, 20(1):279.
[11] Bendtsen L, Zakrzewska JM, Abbott J, et al. European academy of neurology guideline on trigeminal neural gia[J]. Eur J Neurol, 2019, 26:831-849.
[12] Di Stefano G, Maarbjerg S, Nurmikko T, et al. Trig gering trigem-inal neuralgia[J]. Cephalalgia, 2018, 38: 1049-1056.
[13] Debta P, Sarode G, Sarode S, et al. Natural history of trigeminal neuralgia-A hospital-based retrospective study[J]. Oral Dis, 2020, 26(3):647-655.
[14] Di Stefano G, Truini A, Cruccu G. Current and innova tive pharmacological options to treat typical and atypical trigeminal neuralgia[J]. Drugs, 2018, 78(14):1433-1442.
[15] Heinskou TB, Rochat P, Maarbjerg S, et al. Prognostic factors for outcome of microvascular decompression in trigeminal neuralgia: a prospective systematic study using independent assessors[J]. Cephalalgia, 2019, 39(2):197-208.
[16] Chisari CG, Sgarlata E, Arena S, et al. An update on the pharmacological management of pain in patients with multiple sclerosis[J]. Expert Opin Pharmacother, 2020,21(18):2249-2263.


