Cell:刷新认知!基因编辑容易导致染色体丢失,诺奖团队开发潜在应对新策略
时间:2023-10-08 17:22:19 热度:37.1℃ 作者:网络
CRISPR-Cas9基因组编辑使T细胞疗法成为可能,但偶尔丢失目标染色体仍然是一个安全问题。
2023年10月3日,加州大学伯克利分校Jennifer A. Doudna(2020年获得诺贝尔化学奖)及Chun Jimmie Ye共同通讯在Cell 在线发表题为“Mitigation of chromosome loss in clinical CRISPR-Cas9-engineered T cells”的研究论文,为了探索Cas9诱导的染色体丢失是否是一种普遍现象并评价其临床意义,该研究对人原代T细胞进行了系统分析。
排列和汇总的CRISPR筛选显示,染色体丢失在整个基因组中普遍存在,并导致部分和全部目标染色体的丢失,包括在临床前嵌合抗原受体T细胞中。染色体丢失的T细胞在培养中可以持续数周,这意味着可能会干扰临床应用。在Cas9工程T细胞(NCT03399448)的首次人体临床试验中采用了一种改良的细胞制造工艺,减少了染色体丢失,同时在很大程度上保留了基因组编辑的功效。在该方案中观察到p53的表达与染色体丢失的保护相关,这表明T细胞工程的机制和策略在临床上减轻了这种遗传毒性。

CRISPR-Cas9基因组编辑的精确性对于确保临床安全性和避免意外和永久性的基因毒性至关重要。在体外和体内,在意外位点上的混杂脱靶基因组编辑已经得到了广泛的研究和缓解。然而,靶向基因组编辑后的意外染色体异常,如染色体丢失,尚未被系统地调查或预防。因此,这些对基因组编辑的潜在担忧继续存在,包括在临床,以未知的频率存在。
利用Cas9对T细胞进行了广泛的工程改造,以开发针对癌症和自身免疫性疾病的有效免疫疗法。在先前的一项研究中,使用一种临床相关的指导RNA (gRNA)对T细胞受体α恒定区(TRAC)基因进行Cas9介导的基因组编辑后,在原代人T细胞中检测到低水平的染色体非整倍体。然而,染色体丢失在其他靶点发生的程度、这种现象的决定因素、Cas9诱导染色体丢失的T细胞行为以及这些发现的临床相关性仍然未知。随着对这一现象的理解,减少或消除作为基因组编辑结果的染色体丢失的策略将提高工程T细胞疗法对患者的安全性。
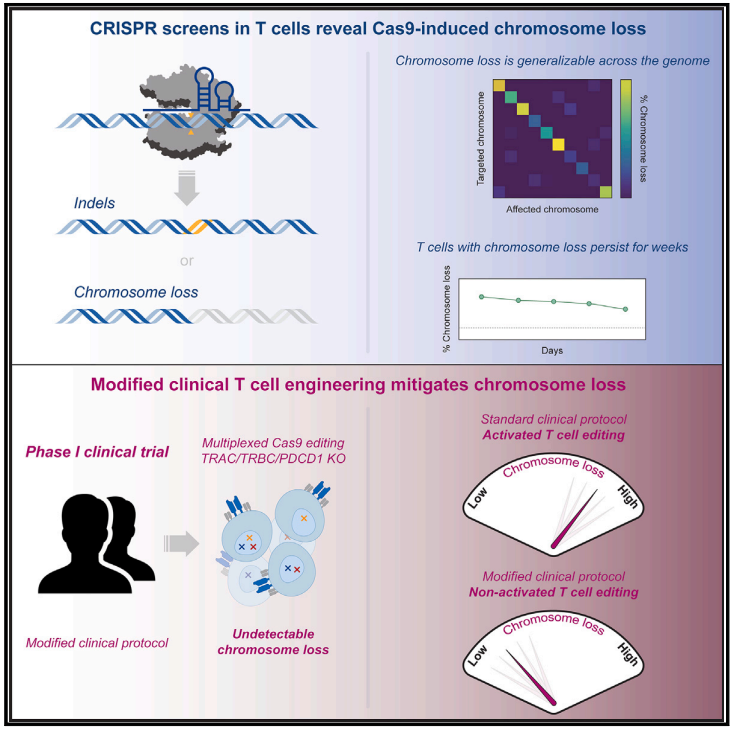
文章模式图(图源自Cell)
该研究分析了人类基因组中每个体细胞染色体上数百个位点的Cas9诱导的基因组编辑后的染色体丢失,以确定这种现象的频率、决定因素和后果。该研究发现Cas9诱导的染色体丢失是一种普遍现象,发生在整个基因组的目标位点。具有Cas9诱导的染色体丢失的T细胞具有适应性和增殖劣势,但可以持续数周的离体培养。
令人惊讶的是,染色体丢失也发生在嵌合抗原受体(CAR) T细胞的临床前生产过程中,但在首次人体I期临床试验中经过Cas9编辑的患者T细胞中很少或检测不到。进一步的实验表明,在临床试验中使用的改进的T细胞编辑方案增加了DNA损伤反应蛋白p53的水平,同时减少了染色体丢失,这表明Cas9诱导的染色体丢失的可能机制以及避免患者出现这种意外结果的意外策略。
参考消息:
https://www.cell.com/cell/fulltext/S0092-8674(23)00975-3#%20


