阿尔茨海默病:过去、现在和未来|9.21世界阿尔茨海默病日
时间:2023-09-18 17:08:26 热度:37.1℃ 作者:网络
论坛导读:阿尔茨海默病(AD)是最常见的痴呆类型,占所有病例的60%至80%。据估计,这种使人虚弱的神经退行性疾病目前影响着全球5000万患者,并间接影响着数千万人的生活,这些人正在应对其亲人多年来的认知衰退,正在成为世界范围内的主要公共卫生问题。几十年来已经探索了许多治疗策略;然而,仍然没有治愈性治疗,优先事项仍然是预防。过去50年来,神经心理学家面临的最大挑战之一是理解痴呆的认知和行为表现及其与潜在脑病理学的关系。随着人口老龄化和许多导致痴呆的神经退行性疾病的年龄相关性,这一挑战在过去几年中显著增加。虽然痴呆的概念已经存在了几千年,但直到上个世纪初才首次发现基本临床综合征和相关的神经退行性改变。
在1901年11月初,德国医生阿洛伊斯·阿尔茨海默(Alois Alzheimer)(1864-1915)在德国法兰克福精神病院收治了一名叫奥古斯特·德特尔(Auguste Deter)的51岁女性患者。阿尔茨海默对其症状的描述几乎肯定是该疾病的第一个神经心理学特征:
“Her memory is seriously impaired. If objects are shown to her, she names them correctly, but almost immediately afterwards she has forgotten everything. When reading a test, she skips from line to line or reads by spelling the words individually, or by making them meaningless through her pronunciation. In writing she repeats separate syllables many times, omits others and quickly breaks down completely. In speaking, she uses gap-fills and a few paraphrased expressions (“milk-pourer” instead of cup); sometimes it is obvious she cannot go on. Plainly, she does not understand certain questions. She does not remember the use of some objects.”
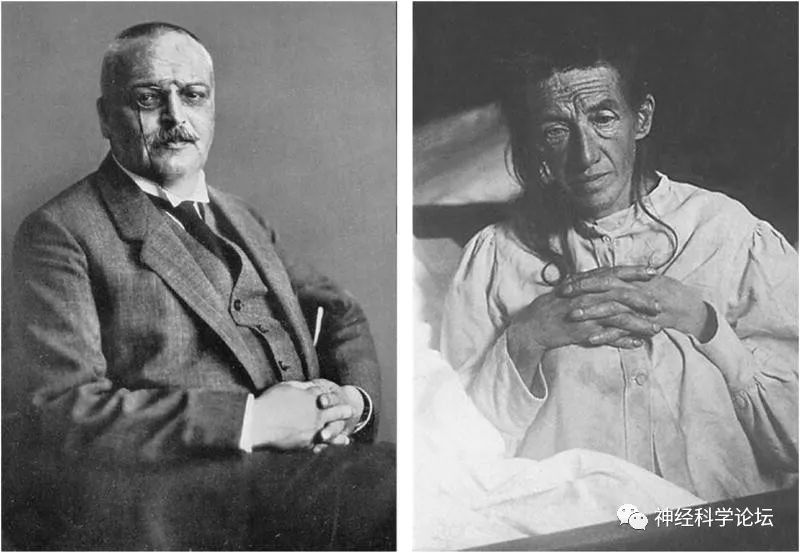
Alois Alzheimer(1864-1915,左)和他的病人Auguste Deter(右)
奥古斯特·迪特尔(Auguste Deter)去世后,阿尔兹海默(Alois Alzheimer)用当时新的银染组织学技术对她的大脑进行了显微镜检查。当他这样做时,他观察到了神经炎斑块、神经原纤维缠结和淀粉样血管病,这些将成为现在以他的名字命名的疾病的标志。阿尔茨海默本人并没有声称发现了“阿尔茨海默病”,尽管他在慕尼黑医学院的导师Emil Kraepelin在他自己的《精神病学手册》(Kraepelin,1910年)中创造了这个术语,正确地认为他发现了“阿尔茨海默病(Alzheimer's disease ,AD) ”,从此阿尔茨海默病就被一直沿用至今。1915年12月阿尔茨海默因扁桃体炎引发的肾炎逝世,享年51岁。
2018年,阿尔茨海默病国际组织估计,阿尔茨海默病发病率和患病率全球约有5000万人患有痴呆症,预计到2050年将增加两倍,其中三分之二生活在低收入和中等收入国家。最新数据估计,到2050年,欧洲的痴呆症患病率将翻一番。越来越多的证据表明,高收入国家的痴呆症发病率正在下降,尽管患病率下降的证据不那么令人信服。
阿尔茨海默病有多种病因,但该疾病的确切原因尚未明确确定。此外,甚至在一个多世纪之后,也没有开发出治愈性的治疗方法。阿尔茨海默病有两种形式:(1)遗传形式或常染色体显性AD (ADAD),发生在65岁之前,占病例的不到1%;(2)散发形式。散发性阿尔茨海默病(SAD)通常发生在65岁以后,该病的发病风险每五年翻一番。
阿尔茨海默病的诊断已经从Alois Alzheimer时代的纯粹病理学诊断发展到1984年的临床排除方法。临床诊断基于国家神经和交流障碍和中风研究所以及阿尔茨海默氏病和相关障碍协会定义的标准,通过国际工作组开发的临床和生物学相结合的方法,以及国家衰老研究所和阿尔茨海默氏病协会工作组随后的努力,结合生物标志物,使阿尔茨海默氏病的分类纯粹是生物学的。最初,阿尔茨海默病的诊断仅限于痴呆阶段,痴呆是一种临床综合征,其特征是影响几个领域的实质性进行性认知障碍,或严重程度足以对日常生活造成明显功能影响的神经行为症状。患有痴呆症的人不再完全独立,这种独立性的丧失是区分痴呆症和轻度认知障碍的主要特征。
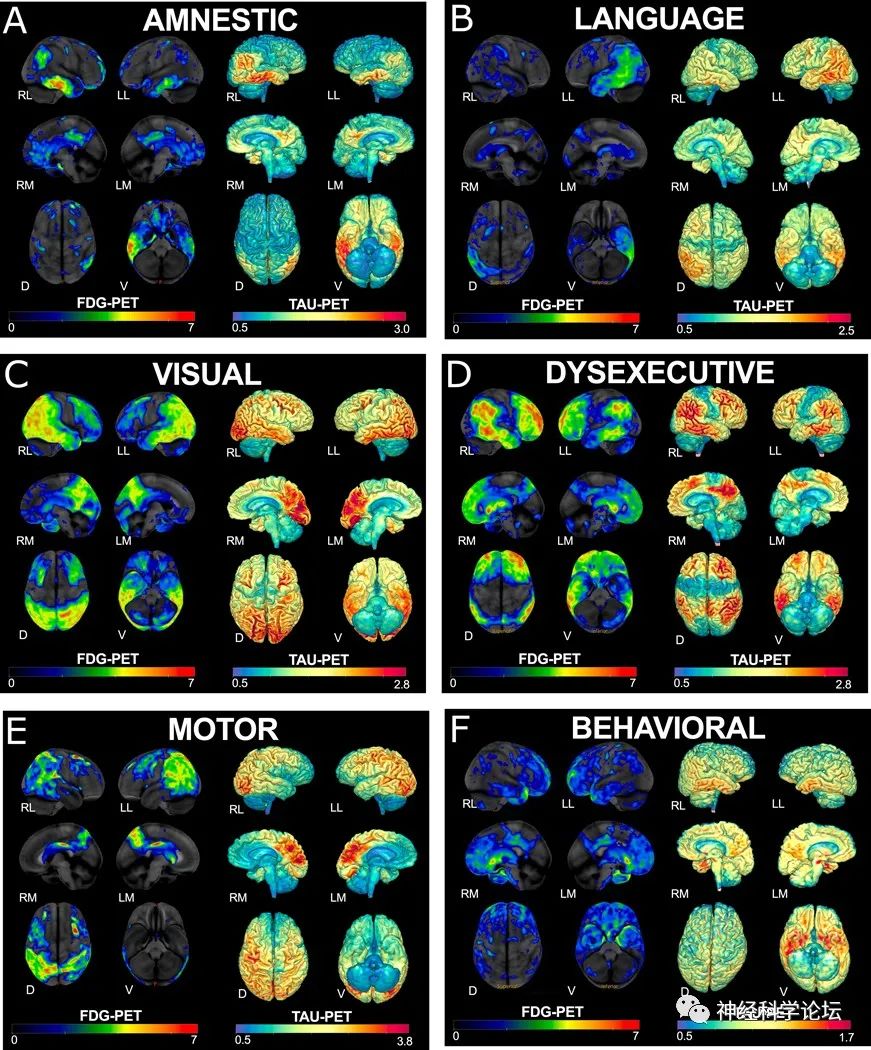
FDG and tau PET across AD phenotypes(Lancet Neurol. 2021 Mar;20(3))
所有AD病例中有一小部分与编码APP(淀粉样前体蛋白)、PSEN1(早老素1)和PSEN2(早老素2)的三种基因的显性基因突变有关,并且通常与疾病的早期发作形式有关,其中临床症状在65岁之前出现。大多数患者表现出迟发性阿尔茨海默病(LOAD ),该病在晚年出现,并且本质上是偶发性的。虽然在这些病例中,该疾病不是遗传性的,也没有单一的遗传原因,但目前的证据支持存在许多遗传风险因素,其中ApoE(载脂蛋白E)基因中E4等位基因的存在——约占人口的16%——是最重要的。生活方式行为,如不良饮食和减少体育活动,以及环境和代谢风险因素,包括糖尿病、脑血管疾病、脑损伤和压力,通常与疾病风险增加有关。
阿尔茨海默病的定义是淀粉样β斑块和神经原纤维缠结,可以在死后或体内用生物标志物检测。散发性AD(即典型AD痴呆)最常见的临床表现是缓慢进行性遗忘障碍,反映了内侧颞叶结构中神经原纤维缠结病理的主要早期分布,最终演变为遗忘为主的多域痴呆。然而,非遗忘表型的特征是基于视觉、语言、执行、行为和运动领域的初始显性困难。这些表现(“非典型AD”)不成比例地影响到65岁前开始出现症状的年轻型痴呆患者。在具有非遗忘症状或缺乏“典型”海马体积丢失的年轻患者中,AD痴呆可能不会被识别。
在一个经神经病理学证实的年轻发病AD队列中,53%的非典型症状患者被误诊,而4%的典型症状患者被误诊。鉴于非遗忘型AD患者年龄较小且症状不常见,他们的症状可能归因于生活压力,或者新发精神疾病神经心理学评估应针对非典型AD进行个体化,并根据总体情况进行解释。例如,视觉或数字需求的记忆或执行功能测试对具有视觉/空间表型的患者提出了特殊的挑战。除了诊断延迟和部署不必要的测试,AD的非记忆症状与显著的发病率和随之而来的自主性和生活质量问题相关,通常发生在有家属的工作年龄人群中。AD服务通常是针对老年患者的需求而定制的,通常不解决需要针对其症状和生命阶段定制治疗计划的非典型AD患者的特定需求。
阿尔茨海默病病理学起因于中枢神经系统(CNS)的结构和功能损伤,包括神经系统中蛋白质的异常聚集和神经变性过程。事实上,在AD中已经确定了两种类型的病变,包括由β-淀粉样肽(Aβ)组成的淀粉样斑块,其在神经细胞外异常积累,以及由过度磷酸化的tau蛋白引起的神经原纤维缠结(NFT),其在神经元中积累。AD可被视为生化、神经生理学、神经解剖学和认知障碍的渐进过程。脑内可溶性Aβ的初始寡聚化导致树突、轴突突起和突触的局部功能障碍。阿尔茨海默病是一种遗传性复杂和异质性疾病,具有多方面的神经病理学特征,包括β-淀粉样斑块、神经原纤维缠结和神经炎症。
新出现的证据表明先天免疫基因和免疫细胞(包括外周免疫细胞,如T细胞)具有有益和病理作用,它们可以渗透到大脑中,改善或加剧AD的神经病理发生。这些发现支持了AD的神经免疫轴,其中大脑内外的适应性和先天免疫系统的相互作用对AD的病因和发病机制产生了重要影响。在过去的十年中,研究工作集中在可溶性Aβ低聚物(AβO)上,这似乎是一种毒性更大、与疾病相关的Aβ形式。AβO被认为是在AD的第一个神经病理学体征之前出现的病理因子。然后,大脑损伤逐渐形成,与大脑某些区域的神经元损失相关,但没有临床表现。随着时间的推移,AD表现为记忆力和认知能力的丧失。以靶向Aβ、Tau蛋白的单克隆抗体为代表的免疫治疗,则是AD治疗药物研发目前最热门的发展方向,其中多种靶向Aβ的单克隆抗体已取得令人欣喜的研究成果,部分在研药物未来有成为AD疾病修饰治疗药物的潜力,也期待更多更新的研究数据,一些正在进行临床试验的AD中医药治疗也值得关注。
阿尔茨海默病的最早阶段(细胞阶段)与淀粉样蛋白β的积累平行发生,诱导tau病理学的扩散。阿尔茨海默病的风险有60-80%取决于遗传因素,已经确定了40多个阿尔茨海默病相关的遗传风险位点,其中APOE等位基因与该疾病的关联最强。新的生物标记物包括PET扫描和淀粉样β蛋白和磷酸化tau蛋白的血浆分析,它们显示了临床和研究应用的巨大前景。基于多领域生活方式的预防试验表明痴呆风险增加的参与者的认知益处。生活方式因素并不直接影响阿尔茨海默病的病理,但仍然有助于阿尔茨海默病患者的积极结果。有希望的药物治疗已进入临床试验的高级阶段,包括抗β淀粉样蛋白、抗tau蛋白和抗炎策略。
虽然AD生物标志物和新的神经病理学方法已被认识多年,但它们已经完善了我们对非典型AD表型广度的理解。在临床实践中增加AD生物标志物的使用和对不同表型的更多识别可以确保早期诊断、及时治疗和适当的支持。非典型AD与年轻发病的AD重叠,越来越多的关注于确保为这些个体提供适当的资源和支持。研究AD的表型异质性是解开临床放射学和神经病理学变异机制的关键,特别是关于记忆功能和内侧颞区的相对缺失。
虽然患有非典型AD的患者在许多方面对于临床试验是理想的,例如,具有较少的共病,但是目前的AD试验强调记忆,并且患有非典型AD的患者可能不符合进入标准。类似于典型的AD研究,几乎所有的非典型AD研究都不成比例地以高加索人群为特征。未来的研究应该在更多样、更具代表性的人群中描述这些综合征。多中心研究,如纵向早发性AD研究目前正在进行中,但需要对这一重要患者群体的非典型AD进行更多研究,以确定局灶性发病背后的机制,是否与早期大脑发育有关,以及促进临床试验的适当结果措施。
阿尔茨海默病各个阶段的发展速度差异很大。阿尔茨海默病患者的平均寿命为确诊后 3 至 11 年,但有些人能活 20 年或更长时间。诊断时的损伤程度可能影响预期寿命。未经治疗的血管风险因素(如高血压)与阿尔茨海默病进展速度更快有关。多种生物标志物的应用、生活方式的改变是AD的早期干预的关键。生物标志物能够提前AD的诊断,有助于无症状期的识别。
不良生活方式可能是AD发生的危险因素,越来越多的证据发现在早期进行生活方式干预,将会改变AD的病理进程。近十年来,研究表明生物学因素和社会学因素对AD发生发展过程的影响作用明显。心脑血管危险因素、各种遗传因子、众多环境因素、超重与肥胖、营养与饮食、饮酒和吸烟、心理压力与抑郁、经济地位等都与认知功能的调节有关。在多项危险因素中,心脑血管危险因素在阿尔茨海默病的预防中占有重要位置。未来应着重关注无症状期人群,提高早期诊断的灵敏度及特异性,将观察性研究与临床试验结果相结合,以期发现阿尔茨海默病演变规律,以便于建立全方位和个体化的最优AD预防策略。
参考文献
Bondi MW, Edmonds EC, Salmon DP. Alzheimer's Disease: Past, Present, and Future. J Int Neuropsychol Soc. 2017 Oct;23(9-10):818-831. doi: 10.1017/S135561771700100X.
Brannon WL. Alois Alzheimer (1864-1915). II. Dementia before and after Alzheimer: a brief history. J S C Med Assoc. 1994 Sep;90(9):402-3.
Graff-Radford J, Yong KXX, Apostolova LG, Bouwman FH, Carrillo M, Dickerson BC, Rabinovici GD, Schott JM, Jones DT, Murray ME. New insights into atypical Alzheimer's disease in the era of biomarkers. Lancet Neurol. 2021 Mar;20(3):222-234. doi: 10.1016/S1474-4422(20)30440-3.
Passeri E, Elkhoury K, Morsink M, Broersen K, Linder M, Tamayol A, Malaplate C, Yen FT, Arab-Tehrany E. Alzheimer's Disease: Treatment Strategies and Their Limitations. Int J Mol Sci. 2022 Nov 12;23(22):13954. doi: 10.3390/ijms232213954.
Jorfi M, Maaser-Hecker A, Tanzi RE. The neuroimmune axis of Alzheimer's disease. Genome Med. 2023 Jan 26;15(1):6. doi: 10.1186/s13073-023-01155-w.
Rostagno AA. Pathogenesis of Alzheimer's Disease. Int J Mol Sci. 2022 Dec 21;24(1):107. doi: 10.3390/ijms24010107.


