针刺调节脑可塑性的机制
时间:2023-09-03 14:43:27 热度:37.1℃ 作者:网络
脑可塑性是指中枢神经系统损伤后在形态结构和功能活动上的可修饰性,最早由 BATHE 提出。
脑可塑性理论当时被称为中枢神经系统受损后替代学说,随后演变出代偿学说、侧支长芽学说、神经通路启用学说等。
经历了约100年的时间,研究者提出脑功能重组论。脑功能重组是脑可塑性的变化性反应。脑可塑性分为结构可塑性和功能可塑性。
-
结构可塑性是指大脑内部的突触、神经元之间的连接可以在学习和经验的影响下建立新的连接;
-
功能可塑性是大脑重组以适应内外界环境的变化。
研究发现,脑的可塑性与环境、个体差异、损伤程度、训练经验密切相关。
一、针灸与突触的可塑性
突触是细胞间信息传递的特异部位,也是神经可塑性变化的敏感部位。
突触可塑性主要指突触连接在形态和功能上的修饰,包括突触结构和数量的长期改变以及神经传递的强度和效能的短期改变。
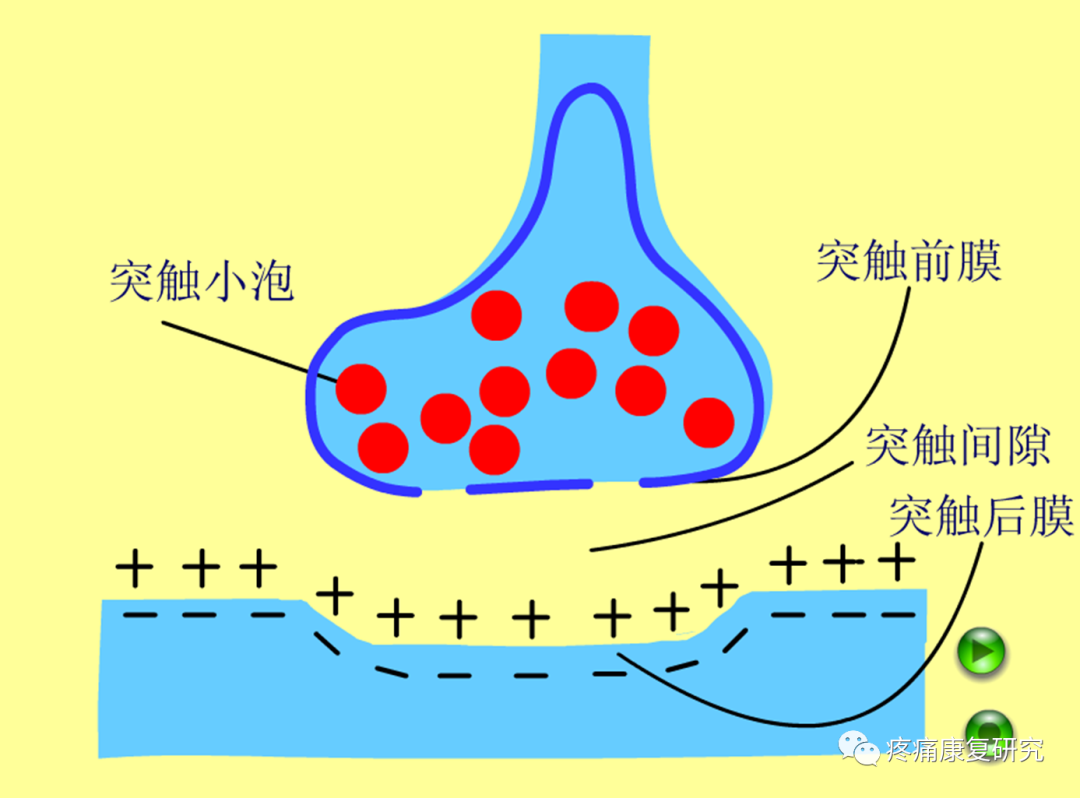
1.突触结构可塑性
突触结构的可塑性是由突触超微结构变化导致的,主要包括以下几个方面:
①突触前后面接触面积(突触的总数、突触数密度、突触面密度、单个突触平均面积);
②突触接触区域活性物质含量[突触素(SYN)等];
③突触相关亚细胞结构[突触后致密物-95(PSD-95)等];
④突触间隙宽度以及界面曲率等。
突触形态学变化是多种疾病的病理机制之一,包括阿尔茨海默病(AD)、血管性痴呆等。
黄国新基于蛋白激酶 A 信号通路证实,电针“百会”“大椎”可增加大鼠突触 PSD 厚度,缩小突触间隙,增加突触界面曲率,对突触结构进行修饰而治疗脑缺血性疾病。
有研究显示,在脑缺血早期(3d),针刺介入治疗可以提高脑梗死大鼠突触数密度、突触面密度,减轻突触超微结构的缺损,促进突触可塑性的持续形成。
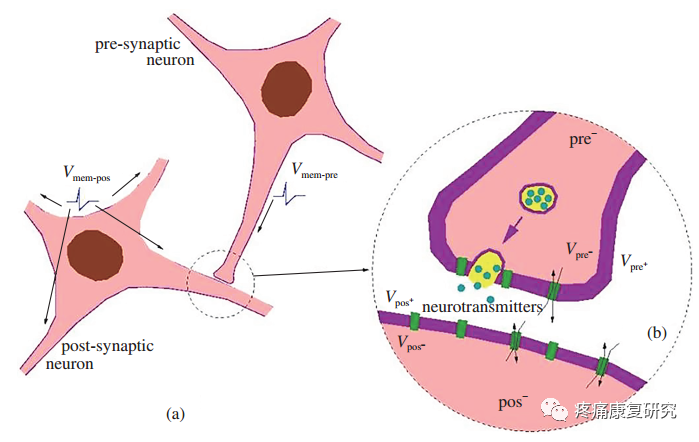
2.突触功能可塑性
突触功能可塑性是基于其结构可塑性提出的,主要是指突触传递效率,其表现形式是长时程增强(LTP)和长时程抑制(LTD)。
-
LTP 是指在高频率100Hz 刺激突触前纤维后,可诱导突触后电位幅度长时间增大;
-
LTD是指持续低频刺激后产生突触后电位幅度长时间减小,它与记忆保存和遗忘有关。
在学习记忆过程中,LTP 可以通过获得、巩固和存储等方式强化长时记忆;LTD 则核实记忆内容,对 LTP 起到调节作用。
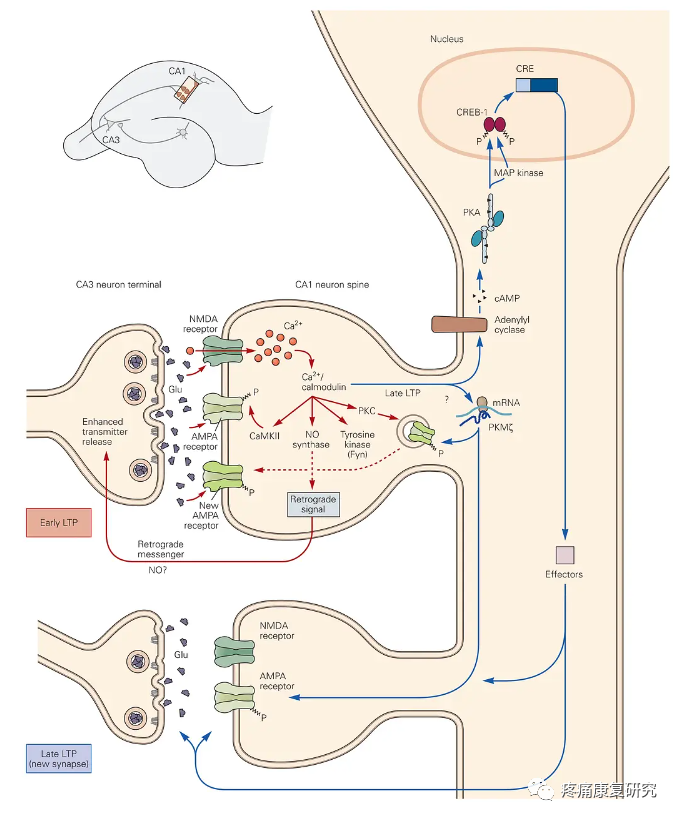
研究发现,电针可以调控N-甲基-D-天冬氨酸(NMDA)和α-氨基-3-羧基-5-甲基异恶唑-4-丙酸(AMPA)的表达,影响 LTP 的产生和维持,促进突触功能可塑性,从而起到保护神经元的作用。
3.突触可塑性相关蛋白
生长相关蛋白-43(GAP-43)是参与轴突出芽和突触重塑的标志性蛋白。其主要在神经元轴突末端生长锥中表达。
生理情况下,GAP-43 处于抑制状态,含量极低。脑损伤后启动内源性保护机制可刺激 GAP-43 的表达。
但随着损伤范围的逐步扩大和损伤修复时间的延长,GAP-43 的表达逐步回落,不足以实现完全性功能代偿,进而加重脑损伤。
研究显示,电针可以上调局灶性缺血/再灌注大鼠海马区GAP-43阳性细胞的表达,促进生长锥形成,加速单胺递质释放,产生和维持 LTP,引导轴突再生和突触重建。

二、针灸与神经胶质细胞
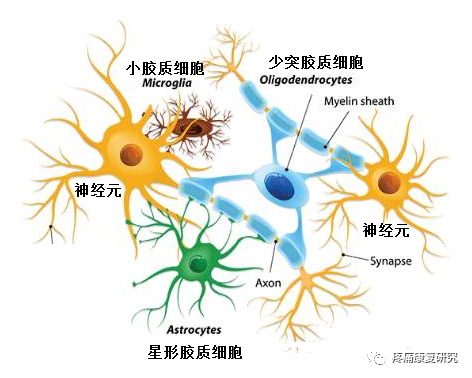
作为最庞大的神经组织,神经胶质细胞形成网状支架,连接各种神经成分,并对神经元提供营养支持,同时还调节神经递质代谢,维持中枢神经系统内稳态和参与突触的信息传递。
神经胶质细胞主要有4种类型:
-
星形胶质细胞(AS)
-
小胶质细胞
-
少突胶质细胞
-
雪旺细胞
其中 AS 与突触传递信息关系最为密切。
正常状态下,AS 能够分泌多种递质,如腺苷三磷酸、胶质纤维酸性蛋白(GFAP)等,参与突触发芽,促进突触连接和再生,保护神经元回路的完整性。
然而过度增殖的 AS 释放谷氨酸造成兴奋性氨基酸毒性、释放炎性因子及降低缝隙连接等影响突触重塑,进而加重神经细胞的损伤。
因此,如何调控 AS 的表达对突触的重塑、神经的修复极为重要。
研究发现,中枢神经系统损伤后,AS 作为“神经元-胶质网络”代表参与突触重塑、轴突再生,促进神经修复。
针刺双向调节损伤后 AS 的机制可能是:
一方面针刺下调胶质纤维酸性蛋白(GFAP)表达,减轻 AS 水肿,降低兴奋性毒性,维持细胞膜内外离子平衡,稳定缝隙连接蛋白的表达,以促进与突触的良性互动;
另一方面,针刺作用于神经元网络,上调突触界面结构参数,增强突触的传递功能,对突触进行结构与功能的修饰,促进神经损伤的再生与修复。
三、针灸与神经营养因子
神经营养因子在参与突触重塑、促进轴突再生、修复神经损伤方面起到重要作用,其主要代表有神经生长因子(NGF)和脑源性神经营养因子(BDNF)。
无论是出血性还是缺血性脑病,均可观察到损伤部位 NGF 和 BDNF的自发性上调表达。
其原因是受损组织启动内源性保护机制,但自发表达的 NGF 和 BDNF 的作用范围与持续时间有限,不能起到持久有效的神经元保护作用。
因此,诱导持续且有效的神经营养因子表达对神经损伤修复具有重要的意义。
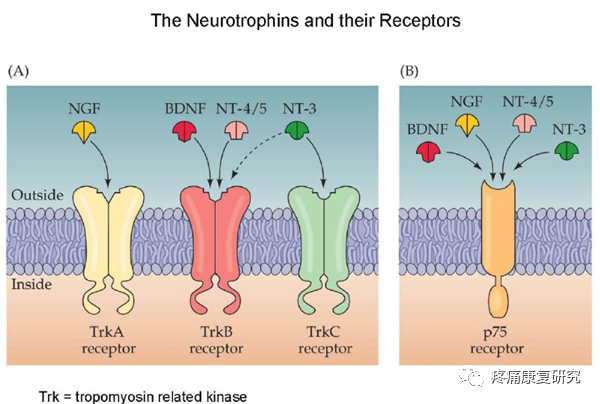
研究中发现:
①针刺诱导 NGF 的表达对神经营养和促进突触生长有生物学效应;
②针刺诱导NGF 可以参与抑制凋亡和调节 Ca2+ 超载、拮抗氨基酸兴奋性中毒而保护神经;
③针刺上调损伤区 BDNF 的表达,可刺激树突合成蛋白参与修饰突触;
④针刺诱导 BDNF 的合成,参与调节突触传递易化 LTP,强化海马学习记忆过程;
⑤针刺可诱导 BDNF 促进突触释放乙酰胆碱而改善认知。
来源
孙忠人,吕晓琳,尹洪娜等.针刺调节脑可塑性的机制研究进展[J].针刺研究,2018,43(10):674-677.DOI:10.13702/j.1000-0607.170039.


