为罕见病诊疗打开新大门!探索单细胞测序在罕见病中的应用
时间:2025-02-28 12:32:22 热度:37.1℃ 作者:网络
据统计,人类已知的罕见病已经超过7000多种,影响人数约2.4~4.5亿,但仅有不到10%的罕见病有相应的治疗方案[1]。罕见病发病率低,病症复杂,具有高度遗传异质性,这使基因检测变得复杂,特别是罕见变异和未知变异在常规基因检测中难以被准确识别。同时,罕见病通常具有高度的细胞异质性,可能只有少数细胞存在致病变异,在疾病发生发展中起关键作用。单细胞测序技术可在单细胞水平对基因组、转录组、表观基因组等进行高通量测序分析,能够揭示细胞间的异质性以及细胞动态变化,精准识别罕见变异、罕见细胞类型,从分子、细胞和系统水平深入了解罕见病背后的生物学机制,在罕见病诊断、药物选择和治疗策略的开发中发挥了关键作用,为罕见病诊疗带来了新的变革。
单细胞测序助力罕见病
生物标志物发掘
生物标志物在疾病诊断、治疗监测、新药评估等方向有着重要应用。单细胞测序能够精确地识别出特定细胞类型中的生物标志物,避免了传统的生物标志物研究可能会忽略的细胞间异质性。
多发性硬化(MS)是一种病因复杂且高度异质的疾病,以患者的免疫细胞攻击少突胶质细胞(OLs)为特征。瑞典卡罗林斯卡医学院团队利用单细胞转录组分析,发现了独特的OLs和OL前体细胞(OPCs),及其特定的选择性剪接基因[2]。同时,研究发现人类 MS大脑中也存在疾病特异性OLs,且已知的MS易感基因在该谱系细胞中表达。研究还证实OLs及其OPCs在MS中是活跃的免疫调节因子,所确定的疾病特异性细胞生物标志物或可成为MS免疫治疗的新靶点(图1)。
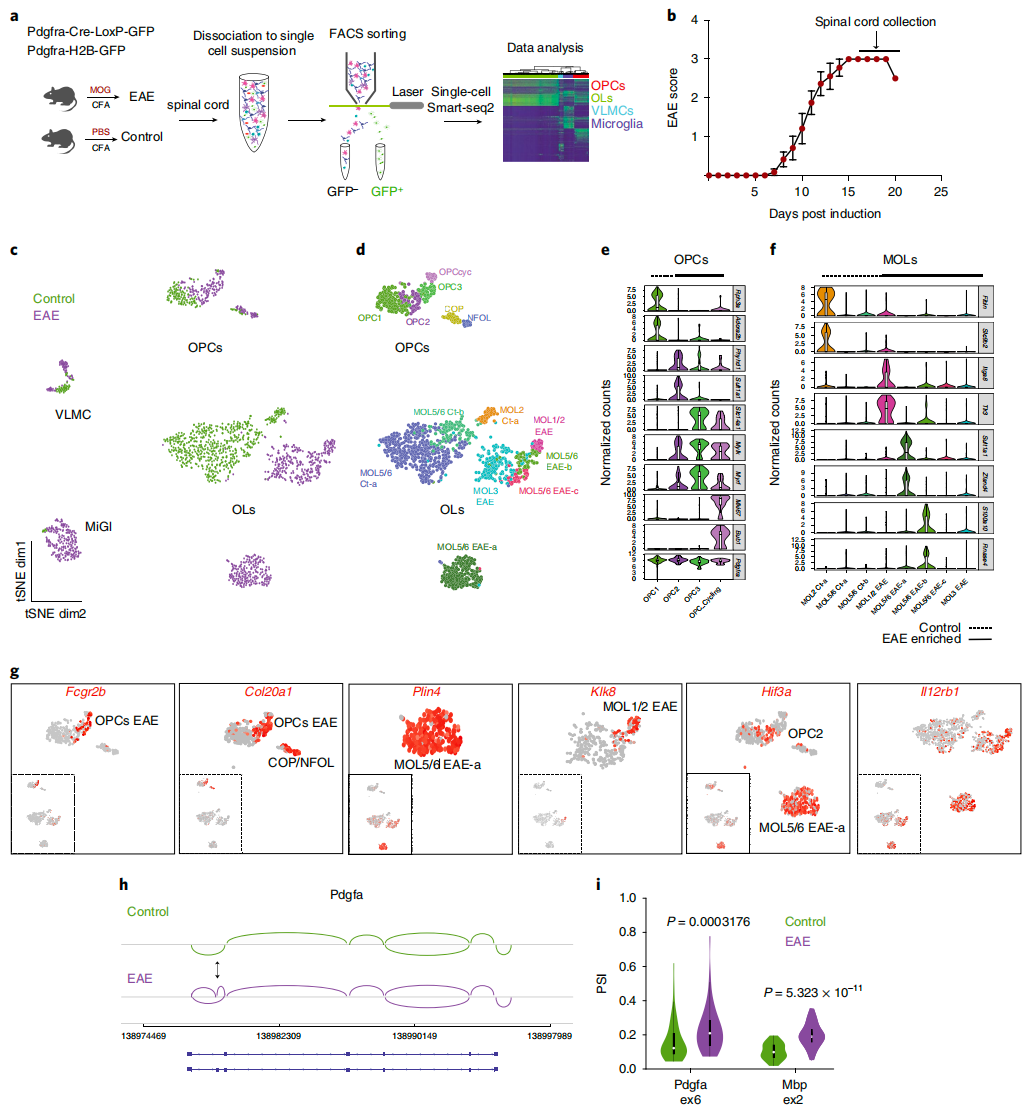
图1 OL谱系细胞单细胞RNA测序揭示新的疾病特异性细胞和标志物[2]
此外,在某些罕见自闭症谱系障碍中,采用单细胞RNA测序对大脑组织进行分析,发现了神经元细胞中与突触功能相关基因的异常表达,如Neuroligin基因家族成员的表达下调,这些基因的表达变化可以作为生物标志物用于自闭症的早期诊断和病情评估[3]。在某些罕见骨髓增生异常综合征(MDS)中,单细胞测序技术被用于分析骨髓细胞,发现了某些造血干细胞和祖细胞中与细胞分化异常相关的基因表达模式案[4]。这些基因表达的改变可以作为MDS的生物标志物,帮助医生判断疾病进展和治疗反应。
总的来说,单细胞测序有助于提高罕见变异的检出率,全面解析基因表达调控机制的变化,确定疾病相关的基因表达调控标志物,亦可对同一患者不同阶段的细胞进行纵向监测,追踪生物标志物的动态变化,为疾病的早期预警、病情评估和治疗方案调整提供参考。
单细胞测序鉴定罕见病
潜在药物靶点
在寻找罕见病药物靶点时,传统方法难以精确聚焦到病变细胞及关键分子改变,使真正在疾病发生发展中起关键作用的变化被忽略,进而难以准确锁定有效的药物靶点。单细胞测序在明确罕见病中受影响的特定细胞类型的同时,还能呈现这些病变细胞在基因表达、表观遗传修饰等方面的状态变化。
例如在罕见遗传性血液疾病中,单细胞测序能够发现与红细胞生成异常相关的基因突变。在先天性纯红细胞再生障碍性贫血(DBA)患者中,约75%的病例由单基因的杂合突变引起,包括RPS-DBA、RPL-DBA。对RPS-DBA和RPL-DBA基因型患者的造血细胞进行单细胞测序,发现这两种基因型细胞的发育轨迹完全不同(图2),且两种基因型细胞的红细胞衰竭途径不同[5]。这些发现有助于发现新的治疗靶点。
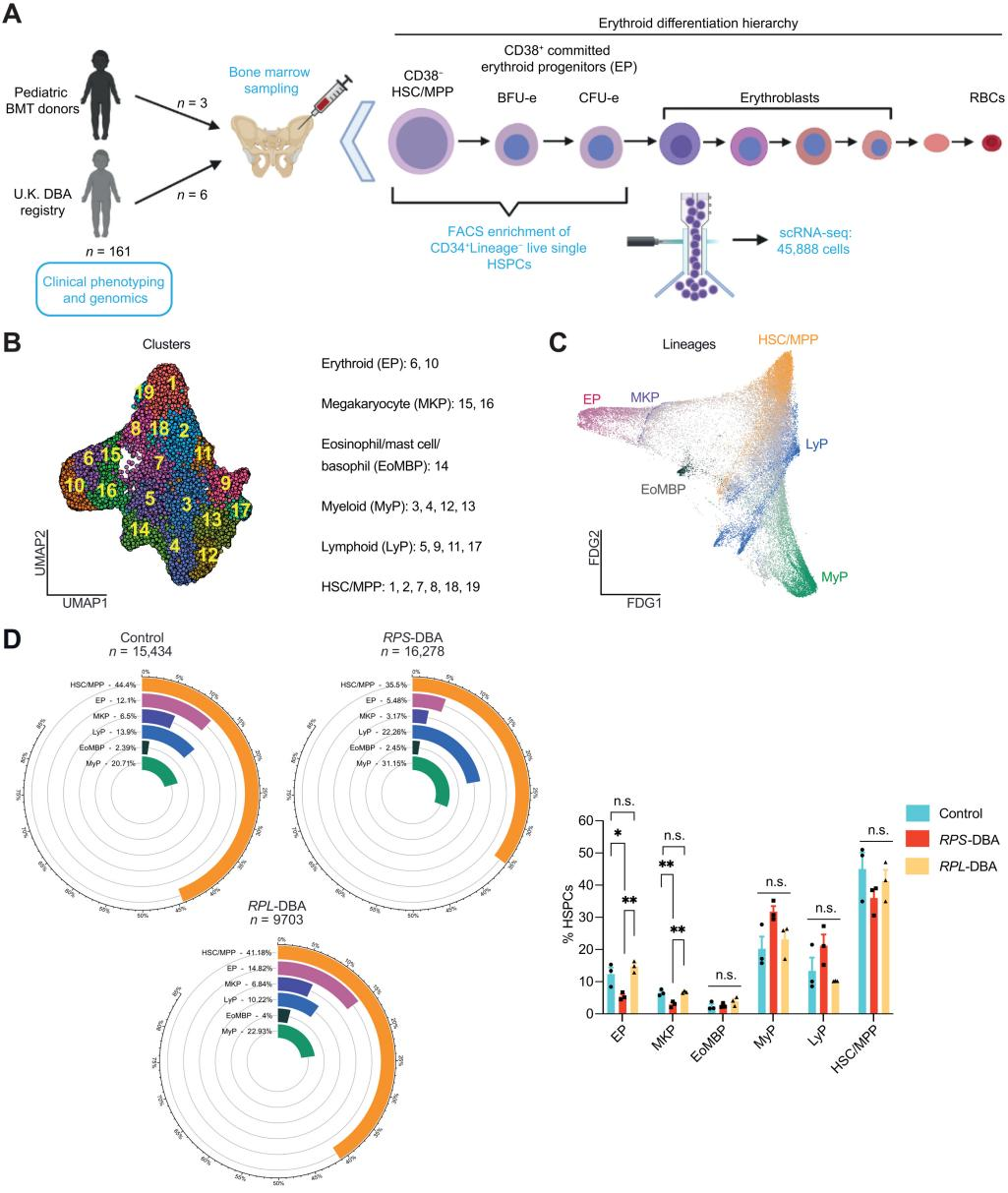
图2 单细胞测序揭示DBA红细胞谱系衰竭机制[5]
单细胞测序可以发现一系列与疾病相关的基因、蛋白和信号通路,这些都可以作为潜在的罕见病药物靶点。在高度遗传的神经发育综合征中,例如自闭症谱系障碍(ASD),因美纳的PIPseq单细胞测序平台发现了新的风险基因,为ASD的分子机制提供了新见解,并为开发遗传性疾病的治疗策略提供了一个强大的平台[6]。
此外,单细胞测序还可用于了解治疗中罕见病的细胞动态变化和靶点情况,帮助临床优化治疗时机选择。
单细胞测序监测罕见病
预后评估
罕见病的传统预后评估方法主要基于临床症状、疾病分期以及有限的生物标志物,无法充分考虑罕见病患者细胞层面的差异,难以准确预测疾病的进展和结局。
中国医学科学院北京协和医院研究团队首次利用单细胞RNA测序描述了两名自身炎症性疾病患者在接受抗TNF治疗前后外周血单个核细胞(PBMCs)和多形核中性粒细胞(PMNs)的转录组图谱[7]。结果显示,抑制巨噬细胞分化,而非炎性细胞因子的减少,是自身炎症性疾病中抗TNF治疗产生反应的潜在机制(图3)。
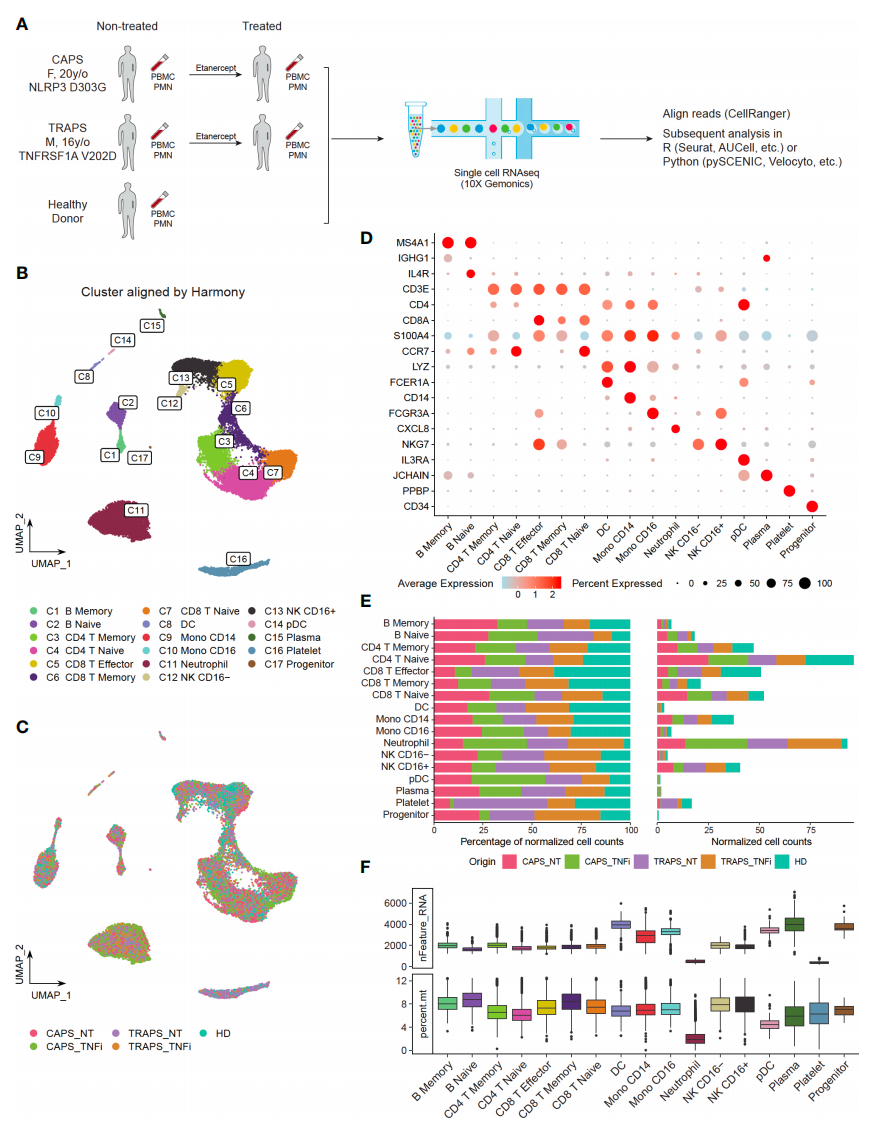
图3 自身炎症性疾病患者PBMCs和PMNs的单细胞转录谱分析[7]
上文提到,在罕见的神经疾病中,通过scRNA-seq能够区分神经元、神经胶质细胞等不同细胞亚群在疾病进展过程中的变化。如果发现某些神经元亚群的基因表达模式逐渐恶化,这可能预示着患者预后不良。在罕见病治疗期间,观察与疾病进展相关基因的表达趋势至关重要,例如在某些罕见的自身免疫性疾病中,监测免疫细胞中炎症因子相关基因的表达水平,如果这些基因表达在治疗后没有下降反而上升,可能暗示患者的病情难以控制,预后较差。
因此,单细胞测序可以精准识别疾病进展风险,发现罕见但对预后有关键影响的细胞亚群及基因表达,对罕见病疾病的预后评估具有重要意义。
结 语
单细胞测序在罕见病诊疗中的应用具有深远的现实意义和影响,在诊断方面,可提高诊断准确性,实现早期诊断;在机制研究方面,可深入了解疾病的发病机理,发现新的细胞类型和标志物,为疾病的诊断和治疗提供新的靶点和方向;在治疗方案制定方面,可为临床更精准地选择适合患者的治疗方法提供证据支撑,并预测治疗反应和耐药性;在疾病监测方面,可实时了解疾病的进展情况和治疗效果,准确预测患者的疾病预后,改善患者的生存质量。
毫无疑问,单细胞测序为罕见病诊疗打开了新的大门。其中,因美纳将其易用且灵活的创新单细胞测序方法PIPseq升级为一套全面的端到端解决方案,通过整合DRAGEN和Partek等生物信息工具,为研究人员提供了一个强大而灵活的单细胞分析平台,全方位助力科研探索。据悉,该单细胞3' RNA表达解决方案兼容所有因美纳中高通量基因测序仪,具有高灵敏度、操作简便和成本效益等特点,将加速因美纳为客户提供完整多组学解决方案的能力。
参考文献:
[1] Groft SC, Posada M, Taruscio D. Progress, challenges and global approaches to rare diseases. Acta Paediatr. 2021 Oct;110(10):2711-2716. doi: 10.1111/apa.15974. Epub 2021 Jun 19. PMID: 34105798.
[2] Falcão AM, van Bruggen D, Marques S, et al. Disease-specific oligodendrocyte lineage cells arise in multiple sclerosis. Nat Med. 2018 Dec;24(12):1837-1844. doi: 10.1038/s41591-018-0236-y. Epub 2018 Nov 12. PMID: 30420755.
[3] Uchigashima M, Leung M, Watanabe T, et al. Neuroligin3 splice isoforms shape inhibitory synaptic function in the mouse hippocampus. J Biol Chem. 2020 Jun 19;295(25):8589-8595. doi: 10.1074/jbc.AC120.012571. Epub 2020 May 7. PMID: 32381505.
[4] Zeng X, Wang Y, Dai M, Li W, Huang Q, Qin L, Li Y, Yan Y, Xue X, Yi F, Li W, He L, Liu Q, Qi L. Single-cell transcriptomics dissects the transcriptome alterations of hematopoietic stem cells in myelodysplastic neoplasms. J Transl Med. 2024 Apr 17;22(1):359. doi: 10.1186/s12967-024-05165-z. PMID: 38632656; PMCID: PMC11022353.
[5] Iskander D, Wang G, Heuston EF, et al. Single-cell profiling of human bone marrow progenitors reveals mechanisms of failing erythropoiesis in Diamond-Blackfan anemia. Sci Transl Med. 2021 Sep 8;13(610):eabf0113. doi: 10.1126/scitranslmed.abf0113. Epub 2021 Sep 8. PMID: 34516827.
[6] Belinda Wang, Rasika Vartak , Yefim Zaltsman, et al. A foundational atlas of autism protein interactions reveals molecular convergence. bioRxiv, 2023. doi: https://doi.org/10.1101/2023.12.03.569805.
[7] Hua Y, Wu N, Miao J, Shen M. Single-cell transcriptomic analysis in two patients with rare systemic autoinflammatory diseases treated with anti-TNF therapy. Front Immunol. 2023 Feb 24;14:1091336. doi: 10.3389/fimmu.2023.1091336. PMID: 36911721; PMCID: PMC9998688.


