Cell Discovery:浙江大学李学坤/舒强/马大青/朱进飘合作揭示睡眠量的调控新机制
时间:2025-02-17 12:10:09 热度:37.1℃ 作者:网络
睡眠行为受多种机制调节,包括遗传、神经调控和环境信号。然而,关于表观转录组学在调节睡眠行为中的作用仍然完全未知。
2025年2月4日,浙江大学李学坤、舒强、马大青、朱进飘共同通讯在Cell Discovery 上在线发表题为“Mettl3-m6A-NPY axis governing neuron–microglia interaction regulates sleep amount of mice”的研究论文。研究发现兴奋性神经元中RNA m6A甲基转移酶Mettl3的缺失会特异性地诱导小鼠丘脑中的小胶质细胞活化、神经炎症和神经元缺失。
Mettl3缺乏显著扰乱睡眠节律,减少非快速眼动睡眠时间。研究发现Mettl3通过m6A修饰调节神经肽Y (NPY), Mettl3条件敲除(cKO)小鼠丘脑中NPY的表达显著降低。此外,在cKO小鼠中观察到NPY在觉醒-睡眠周期中的动态分布模式。Mettl3和NPY的异位表达显著抑制了丘脑小胶质细胞的活化和神经元丢失,恢复了cKO小鼠被破坏的睡眠行为。综上所述,研究揭示了Mettl3-m6A-NPY轴在调节睡眠行为中的关键功能。

睡眠是一个基本的生物过程,可分为两种不同的状态,即快速眼动(REM)睡眠和非快速眼动(NREM)睡眠。正常的睡眠-觉醒转换对动物和人类的健康至关重要。睡眠不足会改变大脑活动、突触结构和连接,从而导致神经功能缺损,包括学习、认知、注意力和情绪调节受损。
在分子水平上,睡眠受多种机制的调节,包括遗传学、DNA和组蛋白修饰。睡眠剥夺导致组蛋白修饰失调,组蛋白脱乙酰酶抑制剂亚羟基苯胺异羟肟酸(SAHA)挽救了诱导的行为缺陷。睡眠剥夺还显着影响DNA甲基化相关基因和昼夜节律调节因子的表达。REM睡眠行为障碍(RBD)患者表现出加速的DNA甲基化。然而,RNA修饰在调节睡眠行为中的功能仍然完全未知。
N6-甲基腺苷(m6A)是最丰富和可逆的RNA修饰之一,由甲基转移酶样3 (Mettl3), Mettl14和肾母细胞瘤1相关蛋白(WTAP)等“书写者”催化,由AlkB同源物5 (Alkbh5)和脂肪质量和肥胖相关蛋白(FTO)等“橡皮”去除,并由YTH家族蛋白和HNRNPA2B1识别。在神经元系统中,mettl3介导的m6A修饰在调节神经发生和神经元发育中起重要作用,并参与神经系统疾病,但其在调节睡眠行为中的功能尚未阐明。
在本研究中发现在CamkIIα+神经元中Mettl3的缺失会特异性地导致小胶质细胞和星形胶质细胞的活化,并在小鼠丘脑中诱导神经炎症。激活的小胶质细胞显示吞噬能力,导致神经元丢失。除了食物摄入量、体重、大脑大小和存活率减少外,Mettl3条件性敲除(cKO)小鼠还表现出睡眠行为受损。机制上,发现神经肽Y(NPY)的mRNA被Mettl3 m6A修饰,并且NPY的表达在cKO小鼠中显著降低。NPY的异位表达抑制了cKO小鼠的神经炎症并恢复了被打乱的睡眠。综上所述,研究揭示了mettl3介导的m6A修饰在调节睡眠行为中的重要功能和潜在机制。
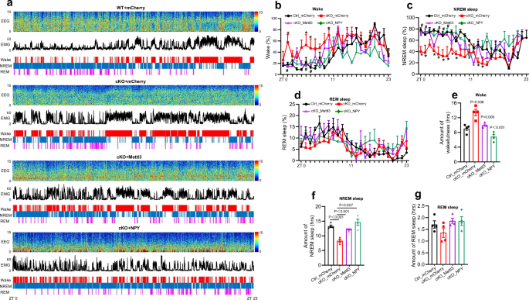
图1 Mettl3和NPY的异位表达恢复了Mettl3缺陷小鼠被破坏的睡眠行为(摘自Cell Discovery )
参考消息:
https://doi.org/10.1038/s41421-024-00756-y


