三阴性乳腺癌复发进展为“三阳性”乳腺癌,转移灶重复活检助力临床诊疗
时间:2024-07-16 16:00:19 热度:37.1℃ 作者:网络
乳腺癌是女性最常见的恶性肿瘤,严重威胁女性的健康。HER2已被确定为乳腺癌的关键致癌基因和预后因素。近来有研究报道乳腺原发性肿瘤和转移性病变中ER、PR和/或HER2表达不一致,三种生物标志物全部发生转化的报道并不多见。本文报道了一例复发转移性乳腺癌女性患者,其组织学由最初的三阴性转变为Luminal-B型(即ER、PR和HER2均阳性)。患者接受系统化疗、靶向治疗和颅部放疗,随后接受靶向治疗和内分泌治疗维持治疗。目前患者已接近完全缓解(nCR)12 个月以上。对于复发转移性乳腺癌,需要进行第二次活检以发现转移灶,这有助于精准治疗和改善预后。
背 景
根据最新的全国癌症报告,乳腺癌是中国女性最常见的恶性肿瘤和癌症死亡的第二大原因。新诊断乳腺癌的治疗策略包括手术、化疗、放疗、靶向治疗和内分泌治疗。治疗的选择取决于TNM分期、病理、分子类型和身体状况。对于复发和转移性乳腺癌,治疗策略主要基于癌症的原始病理和分子类型。最近,一些回顾性研究报道了乳腺癌原发灶和转移灶之间的生物标志物,即雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)的不一致。大多数不一致仅发生在ER、PR和HER2中的一种或两种状态上。很少有报道说三种生物标志物在原发灶和复发和转移灶之间同时发生变化。本文报道一例IIIA期乳腺癌女性患者,复发转移后由原来的三阴性乳腺癌转变为Luminal-B型(HER2阳性),接受抗HER2治疗加化疗,获得近完全缓解(nCR)。
病 例
患者女,31 岁,2018 年 3 月 2 日因左侧乳房触及肿块2个月余,血清CEA、CA153分别为 22.5 ng/ml、46.8 U/ml,后确诊为左侧乳腺癌,于九江学院附属医院行改良根治术。术后病理提示为左侧乳腺浸润性导管癌,非特异性类型,左腋窝淋巴结转移(5/23)。免疫组化检查ER(-)、PR(-)、HER2(-)、Ki-67(80%+),提示为三阴性乳腺癌(图1)。由于患者具有一定的医学知识,要求进一步通过荧光原位杂交(FISH)检查HER2,通过FISH确认HER2为阴性。
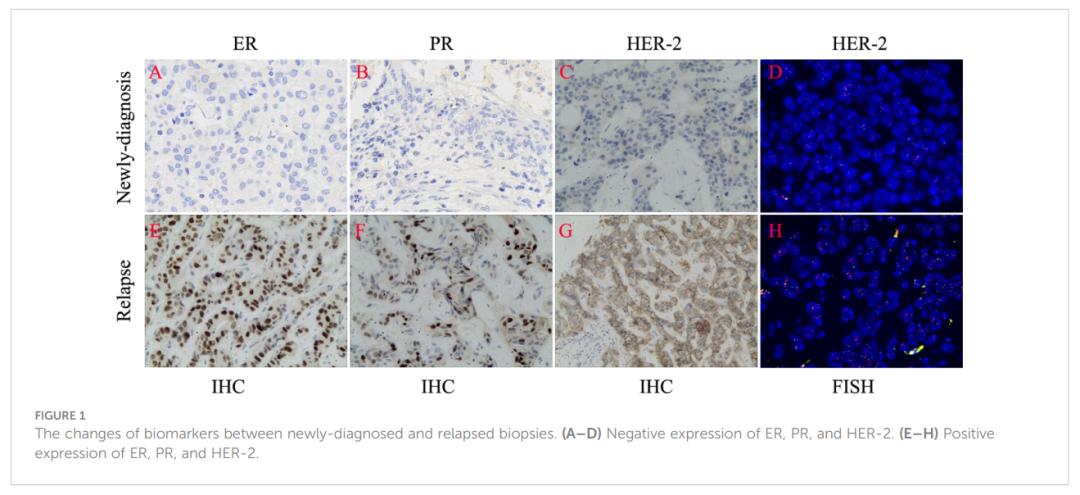
▲图1 诊断时和复发后的生物标志物变化
TNM分期为pT2N2aM0,IIIA期。因复发风险高(≥4 个腋窝淋巴结阳性),患者自 2018 年 4 月 4 日起接受辅助化疗。联合方案为表柔比星和环磷酰胺(EC),每3周1个周期,共 4 个周期。随后接受白蛋白结合型紫杉醇(T)治疗,每3周1个周期,共 4 个周期。10 月 10 日于胸壁及区域淋巴结引流区进行辅助放疗,总剂量 50 Gy,5 周一疗程。患者术后前 2 年定期随访,每 3 个月检查 1 次,包括肿瘤标志物、乳腺超声、胸腹部CT和头颅MRI检查。术后第 3 年起,每 6 个月接受一次定期评估。患者状态良好,未发现肿瘤复发的迹象。
2022 年 12 月患者主诉右上腹不适,食欲不振,偶有恶心,2022 年 12 月 22 日检查显示CEA水平为 32.86 ng/ml,CA153水平 >342.5 ng/ml,腹部CT提示肝脏多发转移性肿瘤(图2)。2023 年 1 月 4 日行脑磁共振成像(MRI),发现右额结节异常信号,提示转移。颈部淋巴结超声检查显示双侧颈部II区及左颈部V区结构性淋巴结异常,淋巴结最大直径仅 1.4 cm,体格检查未发现明显浅表淋巴结。因此,患者于 2023 年 1 月 4 日接受经皮彩色超声引导下肝穿刺活检,病理结果支持乳腺癌肝转移。免疫组化结果显示ER(70%+)、PR(40%+)、Ki-67(40%+)、HER2(2+)表达阳性,FISH检测证实HER2阳性(图1)。最终患者确诊为Luminal B型(HER2阳性),即ER、PR、HER2均阳性。患者于 2023 年 1 月 8 日因脑转移接受立体定向放疗(SRT),DT 50Gy/10F。同期患者于2023 年 1 月 11 日起接受多西他赛(D)、曲妥珠单抗(H)、帕妥珠单抗(P)(D-HP)联合治疗,共 6 个周期,每个周期 3 周。临床疗效按实体肿瘤疗效评价标准(RECIST v1.1)评估,包括完全缓解(CR)和部分缓解(PR)。CR指所有病灶完全消失,病理淋巴结全部缩小至正常大小(短径 <1 cm),持续时间 1 个月以上。PR指所有可测量病灶最大直径总和缩小 30% 以上,且持续时间超过 1 个月;近CR(nCR)指所有可测量病灶大部分消失,仅残留少量细小残留病灶。
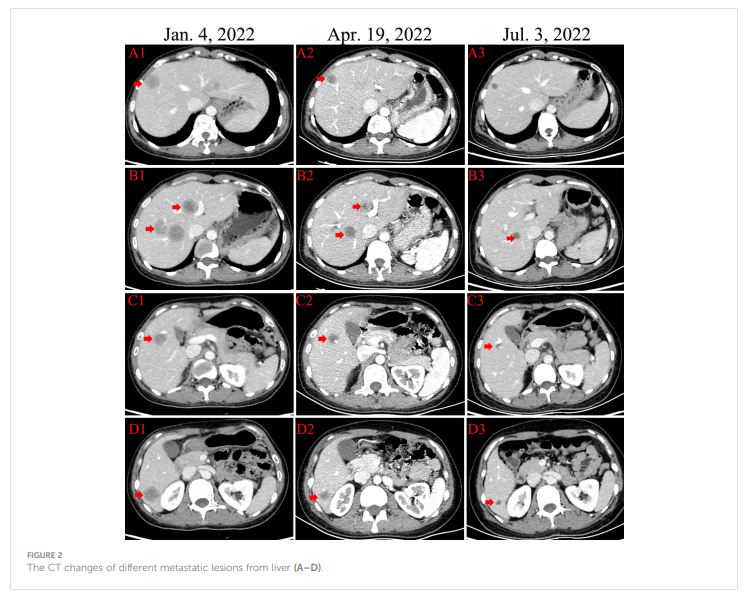
▲图2 肝脏不同转移灶的CT影像改变
自 2023 年 5 月 21 日起,患者开始接受维持治疗,包括曲妥珠单抗、亮丙瑞林、来曲唑和阿贝西利(CDK4/6抑制剂)。目前患者正在接受常规维持治疗,无明显不适。2023 年 12 月最新疗效评估显示,肝脏转移病灶几乎消失,提示nCR(图2)。截至目前,患者无进展生存期(PFS)已超过 12 个月,总生存期已达 69 个月(图4)。患者仍接受密切随访,每 6 个月接受一次定期检查。
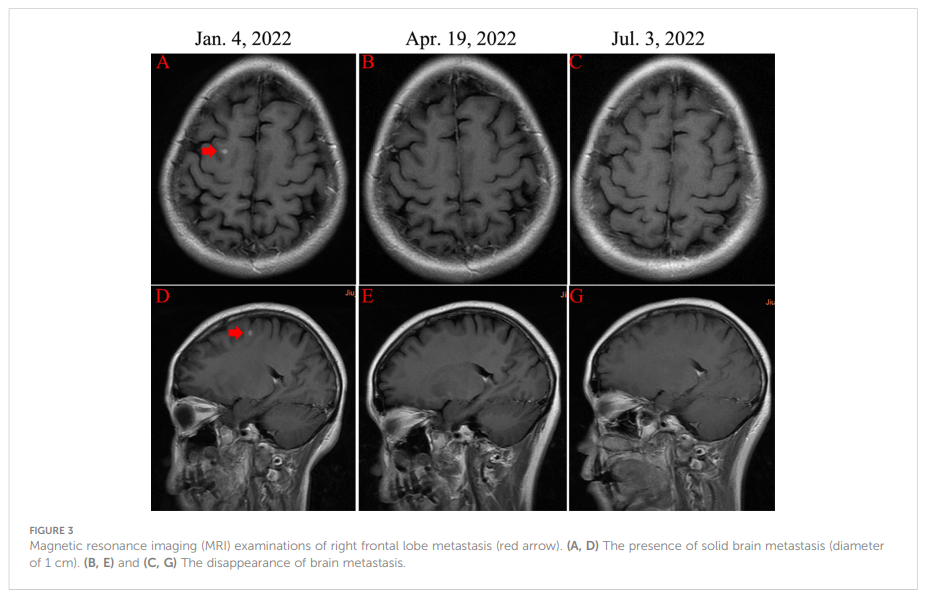
▲图3 右额叶转移瘤的磁共振成像(MRI)检查(红色箭头)
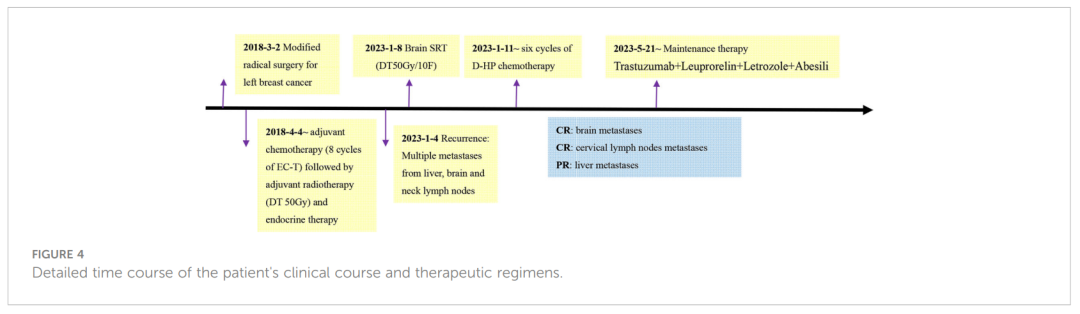
▲图4 患者临床病程和治疗方案的详细时间过程
讨 论
既往认为乳腺癌在病理上是一种静态疾病,但随着分子水平的深入研究发现,乳腺癌应被视为一种时空上的动态疾病,即原发灶与转移灶之间、初诊与复发之间,在不同时期存在异质性。原发灶与转移灶的异质性现象越来越受到乳腺癌领域临床医师的关注。Timmer M等人在 24 例乳腺癌患者中比较了原发灶与脑转移灶的ER、PR及HER-2状态,发现 25%-37.5% 的患者原发灶与脑转移灶的受体状态不一致。Nishimura R等人报道了 97 例乳腺癌患者原发灶与复发灶间ER、PR、Ki-67及HER-2状态的变化,发现复发后ER和PR表达降低,Ki-67升高。24.7% 的患者发生亚型改变。Lin M等对 1299 例乳腺癌患者原发性肿瘤与复发/转移性病变之间HER2状态的变化进行了比较,不一致的发生率为28.5%(370/1299),提示原发性到转移性HER2状态的转化。结果提示,原发性与转移性病变之间的异质性是临床上不可忽视的重要问题。
部分潜在机制归因于克隆进化,克隆进化导致恶性进展过程中的遗传异质性。Sprouffske K等人在乳腺癌患者来源的肿瘤异种移植(PDX)中模拟了转移过程的克隆进化。在克隆选择过程中,一些亚克隆保持稳定,一些亚克隆扩增,另一些亚克隆随时间推移消失。此外,克隆进化导致遗传异质性和不同的临床结果。通过下一代测序(NGS)对 37 名被归类为继发性耐药的HR阳性、HER2阴性乳腺癌患者进行了循环肿瘤DNA(ctDNA)的前瞻性分析。化疗组新突变发生率为 0%(0/9),CDK4/6抑制剂联合内分泌治疗组(CE组)新突变发生率为 42.1%(8/19),化疗序贯CE组新突变发生率为 36.3%(4/11)(p=0.024)。结果表明化疗或CDK4/6抑制剂可能影响乳腺癌患者的克隆进化。Kujala J等人通过液体活检检测到乳腺癌患者匹配的原发性肿瘤和转移部位存在 56.2±7.2% 的体细胞变异。显然,液体活检可以识别肿瘤组织DNA中缺失的新型驱动变异和治疗靶点。在临床环境中,ctDNA可能是纵向监测无法获取组织标本的乳腺癌患者遗传异质性的理想替代品。另一个可能的解释是,第二个局部病变(原位或侵袭性)可能与原发性DCIS同时发生,或在原发肿瘤和复发时发生,这可能是管腔转移的合理解释。因此,对乳腺癌患者的随访是必要且重要的。
研究表明,乳腺癌患者在初诊及复发转移,所有的转移均仅发生在三种受体(ER、PR、HER2受体)中的一种或两种上,而由三阴性转为ER、PR、HER2阳性的却很少。本报告介绍了一例初诊三阴性乳腺癌女性患者,术后 57 个月出现肝脏、脑、颈部淋巴结多处转移,肝转移灶再次活检提示为ER、PR、HER2阳性,肝脏是再次活检的最佳部位,患者因此得到了准确检测和精准治疗。令人欣慰的是,患者经过系统治疗,所有转移灶均获得nCR,这再次证实了疾病复发转移后的正确诊断。相比之下,乳腺癌患者脑转移后再次活检并不容易。在这种临床环境下,ctDNA液体活检[包括脑脊液(CSF)]可能是这类患者的替代选择。
结 论
ER、PR和HER2生物标志物状态的差异对乳腺癌患者(尤其是原发性肿瘤和转移性病变)带来了重大的临床挑战。在乳腺癌疾病进展过程中,三种生物标志物同时转换的情况很少见。本研究介绍了一名女性患者,患者原发为三阴性乳腺癌,在复发和转移后转变为ER、PR和HER2阳性状态。随后,患者接受了系统治疗,包括化疗、靶向治疗、头颅放疗和维持治疗。到目前为止,患者已获得超过 12 个月的良好完全缓解(nCR)。CLEOPATRA研究的最终结果显示,D-HP组的mOS和 8 年OS率均显著高于DH(多西他赛-曲妥珠单抗)组(mOS:57.1 vs. 40.8个月;8 年OS率:37% vs. 23%)。因此,有理由相信患者可能获得良好的预后。本研究强调了乳腺癌患者二次活检的必要性和重要性,这对乳腺癌的精准诊断和治疗具有重要意义。
参考文献:
Huang J, Liu L, Ding J. Case report: From negative to positive: a remarkable journey of ER, PR and HER2 status in a patient with metastatic breast cancer. Front Oncol. 2024 Apr 26;14:1381541. doi: 10.3389/fonc.2024.1381541. PMID: 38737908; PMCID: PMC11088233.



