中科院生物物理所彭华/清华大学傅阳心《自然·通讯》:开发肿瘤特异性anti-PD-IL12免疫治疗药物
时间:2024-06-08 06:00:40 热度:37.1℃ 作者:网络
近年来,以免疫检查点阻断为代表的免疫治疗快速发展,为癌症治疗带来新的希望。免疫检查点阻断疗法通过解除肿瘤微环境中免疫细胞受到的抑制作用,恢复免疫细胞的活性,实现对肿瘤细胞的有效杀伤和清除。尽管如此,仅有一小部分癌症患者能够真正应答免疫检查点阻断疗法。为了使更多的患者从免疫检查点阻断疗法中获益,急需探索新的治疗策略进而有效地提高治疗效率。
白细胞介素12(IL-12)是一种具有免疫激活活性的细胞因子,能够高效的激活免疫细胞,包括T细胞和NK细胞,进而增强机体的抗肿瘤免疫反应。然而IL-12在系统性使用时往往会导致严重的副作用,极大阻碍其于癌症治疗中的应用。另外,有研究表明IL-12是PD-1阻断治疗中的关键分子。因此,有效地联合IL-12和PD-1抗体将有希望更强地激活免疫系统,取得更好的肿瘤治疗效果。
2024年6月3日,中国科学院生物物理研究所彭华教授和清华大学傅阳心教授团队在《Nature Communications》在线发表了题为 “Anti-PD-1 cis-delivery of low-affinity IL-12 activates intratumoral CD8+T cells for systemic antitumor responses” 的研究成果,该研究通过构建anti-PD-1抗体和低亲和力IL-12的融合蛋白,实现对肿瘤浸润CD8+T细胞特异性地激活,在有效增强抗肿瘤免疫反应的同时避免IL-12引起的副作用。

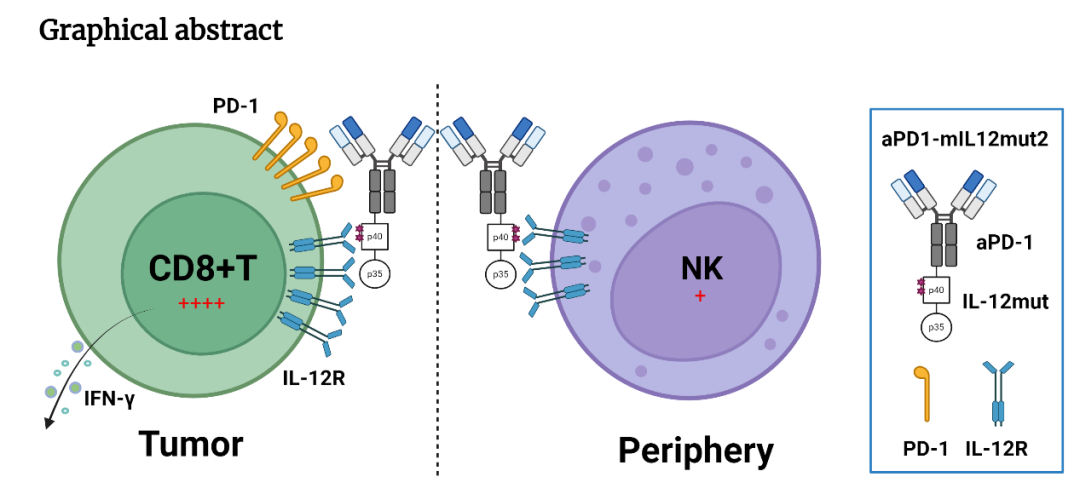
首先,为了降低IL-12因激活NK细胞而产生的副作用,研究团队构建了不同类型的IL-12突变体。这些IL-12突变体对NK细胞的刺激活性大大降低,并在小鼠肿瘤模型中使用时完全不会产生明显的副作用。但是,这些IL-12突变体对CD8+T细胞的刺激活性也明显减弱。为了使IL-12突变体特异并高效地激活CD8+T细胞,研究者构建了anti-PD-1抗体和IL-12突变体的融合蛋白,命名为aPD1-mIL12mut。
BioRender制作
该融合蛋白具有几大优势,其一,anti-PD-1抗体和IL-12的融合能够提高IL-12的血清稳定性,延长IL-12的半衰期;其二,实验表明肿瘤内浸润的CD8+T细胞高表达PD-1分子,因此使用anti-PD-1抗体能够将IL-12更多地靶向到瘤内的CD8+T细胞;其三,低亲和力的IL-12确保anti-PD-1抗体在融合蛋白中的靶向主导作用,降低原本的高亲和力IL-12对anti-PD-1抗体肿瘤靶向效应的干扰;其四,最重要的是,当anti-PD-1抗体结合到CD8+T细胞表面,能够恢复IL-12突变体对CD8+T细胞的刺激活性。综合这些特点,此融合蛋白仅对高表达PD-1分子的CD8+T细胞具有较强的刺激活性,对其他低表达PD-1分子的免疫细胞,特别是NK细胞,仍旧保持非常低的刺激活性。因而,此融合蛋白在系统性应用时,能够偏向地激活肿瘤内浸润的CD8+T细胞,介导有效的抗肿瘤反应;极弱地激活NK细胞,避免产生严重的副作用。另外,此融合蛋白能够激活全身性的免疫反应,不仅有效地抑制肿瘤的转移,还能发挥长期的免疫记忆保护。
综上所述,anti-PD-1抗体介导的靶向CD8+T细胞的IL-12递送是一种联合anti-PD-1抗体和IL-12、协同激活抗肿瘤免疫的有效策略。不仅IL-12,其他细胞因子在系统应用时,也常常伴随明显的副作用。本项研究为抗体-细胞因子的改造、细胞因子的应用提供了新的思路。
该研究的通讯作者是清华大学医学院傅阳心教授和中国科学院生物物理研究所彭华研究员(现广州国家实验室研究员)。邹壮志博士(撰稿人)、申姣博士等5位作者是本文的共同第一作者。
邹壮志博士,该文章第一作者,毕业于中国科学院生物物理研究所,现为美国密西根大学医学院博士后
申姣博士,该文章共同第一作者,毕业于中国科学院生物物理研究所,现为美国哈佛大学医学院博士后
原文链接:
https://www.nature.com/articles/s41467-024-49034-1.pdf


