想做好脊柱融合手术的麻醉管理?看完这篇就懂了
时间:2024-06-21 16:01:46 热度:37.1℃ 作者:网络
脊柱手术是麻醉医生经常接触的手术类型,涵盖了从治疗椎间盘突出的微创椎间盘切除术到治疗脊柱畸形的复杂性脊柱重建术等多种术式。
这些手术过程可能有的比较简单,如内镜下髓核摘除术,但也可能涉及到多节段的融合、经前路或后路手术,甚至伴随失血和复杂的气道管理。
那么,麻醉医生应该如何为这类复杂脊柱融合术(Spine Fusion)保驾护航呢?快来看看这篇综述总结吧~
手术类型
总体来说,大多数手术的原理就是让原来活动的脊柱节段不能再活动,融合成一个整体,主要用于少数椎间盘突出或椎管狭窄等脊柱退行性变引起的功能紊乱,这一类基本都是先对椎骨“小修小剪”,然后再将活动的节段进行固定与融合,出血较少。
而对于脊柱外伤、肿瘤、先天性后凸侧弯畸形,则需要先进行“大张旗鼓”的截骨术,然后再进行固定融合,这种往往伴随中到大量的失血,管理难度更高。
术前评估与准备
大多数脊柱融合手术都要在全身麻醉下完成,在术前评估阶段应侧重于评价病人是否存在解剖畸形及颈椎活动受限(包括疾病本身所致、牵引、颈托或其它设备导致的),注意观察一些困难气管插管的潜在风险因素(见表1),它们会使得气道管理变得复杂。如果存在这些情况,或许需要准备纤支镜辅助局麻清醒镇静插管。
然而,上述评估仍属于共性的范畴,对于一些特殊情况也需有特殊的提前考虑。比如,脊柱创伤患者可能无法进行术前筛查或合并症的优化处理。应注意评估多发伤的患者是否存在可以导致出血性或低血容量性休克的其他损伤,尤其要注意创伤性脑损伤的可能性。
脊柱创伤的患者可能会有创伤诱发的凝血障碍或急性脊髓损伤,伴或不伴神经源性休克。对于这些病人,通常建议采用高动力疗法,即通过提高血压支持脊髓灌注,改善脊髓水肿,从而减轻继发性脊髓损伤。一般认为急性损伤后至少7日内,应将平均动脉压维持在85mmHg以上。
去甲肾上腺素、多巴胺和去氧肾上腺素这些血管加压药物均可有效提高平均动脉压。但需要注意的是,多巴胺有心律失常风险,并有可能会增加鞘内压,从而阻碍脊髓灌注。去甲肾上腺素在脊髓血流研究中的结果要优于去氧肾上腺素,尤其是对有心动过缓风险的高位颈椎损伤患者来说可能更为适合。
脊柱肿瘤大多是转移而来,脊柱肿瘤手术会增加血栓栓塞性疾病、免疫抑制以及原发肿瘤或化疗相关器官功能障碍的风险。必须考虑患者的癌症治疗史和合并症,因为许多化疗药物与心、肝和肾毒性或骨髓抑制相关,骨髓抑制会增加手术风险。
术中管理
术中管理是麻醉医生的主战场,需要重点关注神经监测、液体选择以及血制品应用三个方面。
01 术中神经监测
接受复杂脊柱融合术的患者往往术后神经功能障碍的风险较高,尤其是当手术计划涉及脊柱侧后凸矫正、硬膜内部分或椎体肿瘤切除时。因此优化术中神经监测是复杂脊柱手术麻醉的主要目的之一。
在术中使用连续神经监测,可“实时”监测脊髓缺血或神经根损伤,外科医生根据信号逆转先前的手术动作或改变矢状位手术矫正量可避免神经损伤。
常用的神经监测包括体感诱发电位(SSEP)、运动诱发电位(MEP)和肌电图。
使用神经监测对于麻醉用药会有一些要求。首先为了满足神经监测的条件,肌松剂的使用会受到限制,在这种情况下,需要相应加大阿片类药物输注的剂量以达到充分镇痛,防止出现对伤害性刺激的运动反应。
挥发性麻醉药对体感诱发电位和运动诱发电位的影响都是剂量依赖性的波幅降低和潜伏期的增加,因此许多麻醉医生会选择全凭静脉麻醉。但实际上如果将吸入麻醉药(这里不包括N2O)的MAC限制在0.5或更小的范围,大多数情况下也可以保留术中神经监测的完整性。
术中静脉快速推注阿片类药物(包括瑞芬太尼)、镇静剂、催眠药和多模式镇痛的辅助药物(如氯胺酮或右美托咪定)都会一过性地影响神经监测信号,因此药物尽量是输注,如果需要静推药物,建议与外科团队沟通说明。
由于MEP的监测存在一些不良反应,包括认知障碍、惊厥、咬伤、术中知晓、头皮损伤和心律失常等。建议在MEP监测期间使用软牙垫预防舌咬伤和牙齿损伤。如果病人存在活动性癫痫、脑内血管夹和人工耳蜗植入,应避免使用MEP。
02 容量管理之液体选择
由于术中可能伴随大量出血,除了在血流动力学监测下积极容量补充与自体血回收之外,在术中液体治疗的选择上,推荐氯含量低的平衡晶体溶液,以大限度避免高氯血症性代谢性酸中毒,降低术后急性肾损伤的风险。
虽然乳酸林格液也是一种平衡晶体溶液,但张力较低,对于长时间俯卧位手术大量液体复苏的患者,可能会导致有害的软组织肿胀和脊髓水肿。
术后视力丧失(POVL)是复杂脊柱手术的一种罕见并发症,已确定的独立危险因素包括男性、肥胖、使用Wilson框架进行俯卧位体位固定、估计失血量较大、手术持续时间以及使用晶体液进行液体管理而非使用某些非血液胶体液。因此,有研究支持在长时间脊柱手术(持续超过6小时)中应使用胶体补充容量复苏,以降低术后视力丧失的风险。
03 血液及血制品应用
复杂脊柱融合术的失血量往往较大,以脊柱畸形矫正手术为例,简单的1 -2个节段融合失血量<500ml,复杂的多节段截骨内固定手术失血可>2000ml。如果不能预先预测和积极处理急性出血,则有严重贫血和稀释性凝血障碍的风险。
因此患者的血液管理需要采取积极的策略,以尽量减少围手术期出血和对异体红细胞输注的需求。
术前已经诊断贫血的应预先补充铁剂和促红细胞生成素,术中应注意保温并使用自体血回收。由于术中往往有活动性失血,应留置动脉导管,每1-2小时就要采血进行血红蛋白的评估,并进行容量复苏和输血。
无需控制性降压,因为它与术后主要心脏不良事件和神经系统并发症(如术后视力丧失)相关。
纤溶抑制剂如氨甲环酸可有效减少总失血量,减少围手术期红细胞输注需求。虽然氨甲环酸的最佳剂量尚未达成明确共识,但对于接受≥3个椎体开放脊柱内固定的成人患者,一种常用的可行的方案是切皮前静脉给予15 mg/kg负荷剂量,术中以1mg·kg-1·h-1的速度输注,直至手术结束。
常规的凝血检验(包括凝血酶原时间、活化部分凝血活酶时间、血小板计数、纤维蛋白原浓度等)已经足够指导血制品的应用,但对于包含截骨术和严重角度矫正的复杂脊柱畸形矫正手术,可能需要血栓弹力图(TEG)的检测。
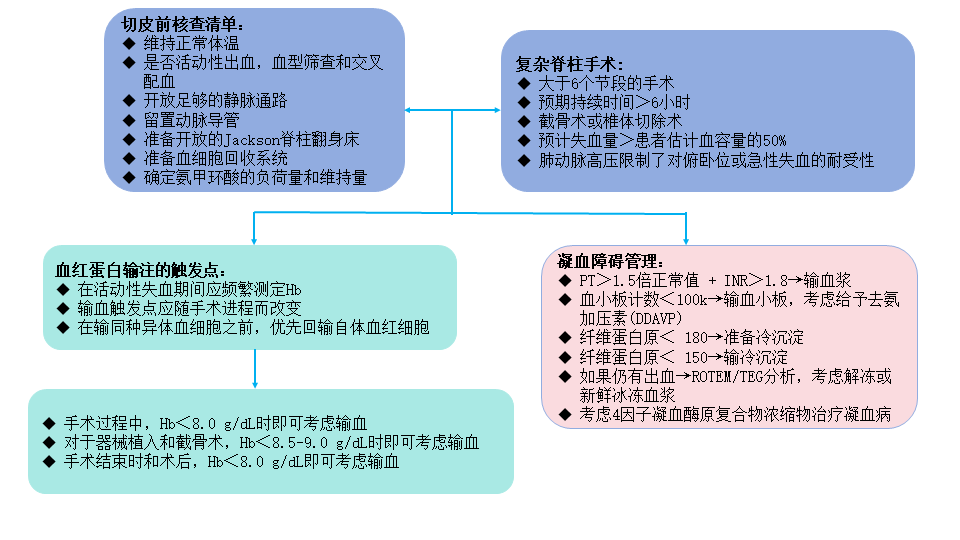
图1为脊柱手术期间患者血液管理的算法图,我们可以看到在脊柱手术中何时、如何输注血制品都有各自的“触发点”,以Hb为例,不同的阶段就有不同的阈值。需要注意的是,不能只顾补充红细胞,满足一定的指征后,就需要考虑血浆、冷沉淀及凝血酶原复合物浓缩物等其它血制品了。
围术期镇痛
复杂脊柱融合术的围术期镇痛还是比较复杂的,因为许多患者在术前由于疼痛就开始服药了,46%的患者术前存在一系列阿片类药物依赖,61%的患者每天使用超过50mg当量吗啡的镇痛药,23%的患者甚至每天需要超过100mg当量吗啡的镇痛药。
术前麻醉性镇痛药物的使用,年龄、焦虑或抑郁史、当前吸烟和手术复杂性,都是脊柱手术后疼痛的危险因素,可能会增加术后镇痛的需求量。
围术期多模式镇痛包括合理使用阿片类药物或“减少阿片类药物”技术,使用非甾体抗炎药便是减少阿片类药物的途径之一。塞来昔布是COX-2特异性拮抗剂,是脊柱手术临床试验中应用最广泛的非甾体抗炎药,已被证明可减少术后24 ~ 48小时内阿片类药物的需求量,且无相关出血风险或手术并发症。
但需要注意的是,应将NSAID限制在术前单次给药或最多将其使用时间限制在2周以内,这样可以降低出血和骨愈合不良的总体风险。
一些抗癫痫类药物如加巴喷丁和普瑞巴林也可以用于脊柱术后镇痛以减少阿片类药物用量。但这种情况下,会增加过度镇静的风险,尤其是与长效阿片类药物合用时,甚至需要纳洛酮拮抗呼吸抑制。因此,加巴喷丁和普瑞巴林并不作为脊柱术后的常规镇痛药物,应非常谨慎地使用,并将术前的剂量也限制在较低水平。
研究发现氯胺酮与长效阿片类药物联用时可显著改善术后疼痛评分,还可减轻瑞芬太尼相关的痛觉过敏。一般从麻醉诱导至术后即刻,常以小剂量输注(例如3µg·kg−1·h−1)的方式给药,但最佳的使用剂量还需要进一步研究。
合理使用阿片类药物加多模式镇痛仍然是复杂脊柱手术术中镇痛的主要手段。舒芬太尼、瑞芬太尼和芬太尼均可用于全身麻醉或全静脉麻醉,而不影响术中神经监测。最近也有试验表明,手术开始时静脉注射0.2-0.3mg/kg剂量的美沙酮可改善疼痛管理,且与不良结局无关。
在区域镇痛方面,不太推荐硬膜外镇痛,因为硬膜外麻醉与手术部位过近,操作不便,且鞘内注射药物有较大的延迟性呼吸抑制的风险。而局部麻醉药浸润伤口简单有效,推荐使用。目前已经有较多关于脂质体布比卡因的临床研究在进行中,未来超长效局麻药伤口浸润会体现明显的优势。
作为越来越多的一种手术类型,脊柱融合术围术期精细化的管理对麻醉医生提出了更多挑战,让我们一起在学习和实践中不断加油!
参考文献
【1】Carabini LM, Koski TR, Bebawy JF. Perioperative Management for Complex Spine Fusion Surgery. Anesthesiology. 2024;140(2):293-303.
【2】Veeravagu A, Li A, Swinney C, et al. Predicting complication risk in spine surgery: a prospective analysis of a novel risk assessment tool. J Neurosurg Spine. 2017;27(1):81-91.
【3】《摩根临床麻醉学》神经外科手术的麻醉,脊柱手术的麻醉
【4】《米勒麻醉学》第7版 矫形外科手术的麻醉,脊柱手术


