Nature子刊:新研究为儿童实体瘤挖掘潜在CAR-T疗法靶点
时间:2024-06-08 06:00:37 热度:37.1℃ 作者:网络
高危或复发性儿童实体瘤和脑瘤,治疗选择非常有限。免疫疗法,特别是嵌合抗原受体T细胞(CAR-T 细胞)疗法,为治疗癌症带来了新的希望。CAR-T细胞疗法使用基因工程技术改造患者自身的T细胞,使其能够识别并杀死癌细胞。开发该细胞疗法的关键在于找到合适的靶点,即癌细胞表面特异表达的蛋白质。然而,目前可用的靶点数量有限,而且很多靶点在正常细胞上也有表达,导致治疗出现脱靶毒性。
近日,由美国St. Jude儿童研究医院的 Jinghui Zhang 博士和 Stephen Gottschalk 博士共同领导的跨学科的团队,在 Nature Communications 上发表的题为 Discovery of immunotherapy targets for pediatric solid and brain tumors by exon-level expression 的文章,通过运用计算生物学方法,对患儿的测序数据进行分析,发现了一系列潜在的免疫治疗靶点,为治疗儿童实体瘤和脑瘤提供了新的可能性。
这些靶点具有高度的癌症特异性,这意味着它们在正常组织中表达水平很低,可以减少治疗的副作用。研究人员为这些靶点信息,开发了一个名为CSE-miner的交互式网络数据库(https://cseminer.stjude.org/),为其他研究人员提供了宝贵的资源。这项研究为开发更安全、更有效的儿童癌症免疫疗法奠定了基础。

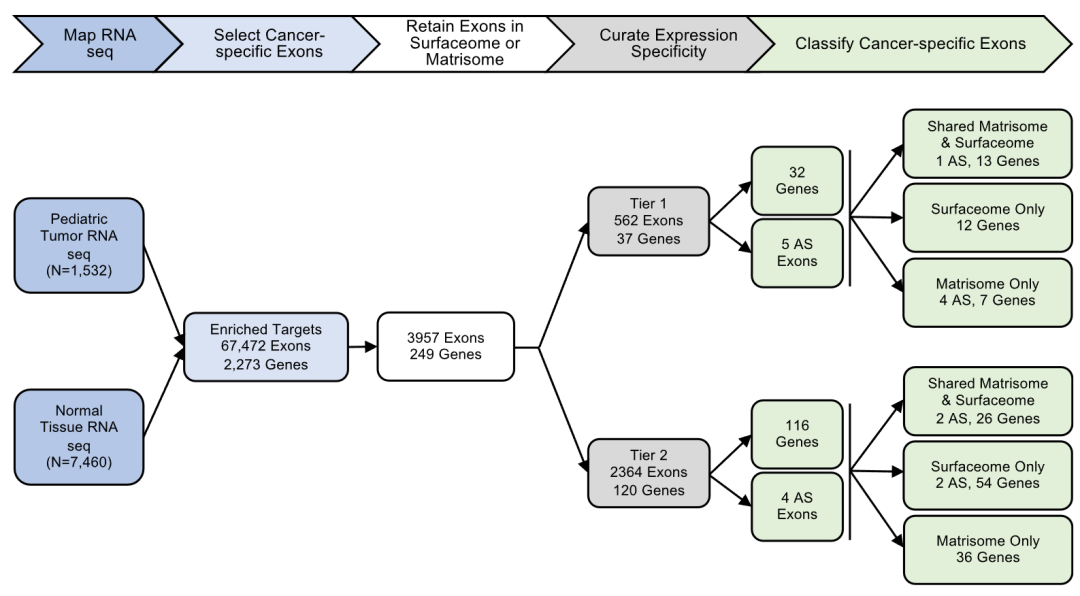
研究团队从海量RNA测序数据中,精准高效地筛选出那些在肿瘤细胞中高表达、但在正常组织中低表达的癌症特异性外显子(CSE)。 研究团队从16种儿童实体瘤和脑瘤中,识别出157个基因的2,933个癌症特异性外显子(CSE)。这些基因编码的蛋白质存在于细胞表面或细胞外基质中,可以被免疫系统识别。大部分(93%)被识别的CSE都是从未被报道过的新靶点,为免疫治疗提供了更广阔的选择。研究团队之所以能发现如此多的潜在靶点,主要归功于以下几个方面:
外显子级别的分析精度:与传统方法只关注基因整体表达水平不同,该研究的计算生物学方法能深入到外显子层面,分析每个外显子的表达情况。这使得研究人员能够发现那些由于可变剪接等机制导致的在肿瘤细胞中特异性表达的外显子,从而找到更多潜在的靶点。
大规模数据集的整合分析:研究团队整合了来自多个数据库的大规模RNA测序数据集,包括来自St. Jude儿童医院、华盛顿大学和美国国家癌症研究所等大型研究机构的数据。这为研究提供了充足的样本量,保证了分析结果的可靠性和全面性。
严格的筛选标准:为了确保找到的CSE靶点具有高度的癌症特异性,研究团队制定了非常严格的筛选步骤,包括:
-
要求CSE在肿瘤样本中的表达水平明显高于正常组织。
-
排除那些在重要器官(如脑、肝、肺、骨髓等)中高表达的CSE。
利用蛋白质组学数据,验证候选CSE在蛋白质水平上的表达情况。
验证部分靶点的表达和功能
研究人员选择了三个在一系列儿童肿瘤中高表达的CSE靶点,在人源小鼠模型中验证了它们的表达。这些靶点在肿瘤细胞表面的表达量很高,说明它们具有作为 CAR-T细胞疗法靶点的潜力。研究人员还开发了针对EDB和COL11A1的CAR-T细胞,并在体外和体内实验中验证了它们的抗肿瘤活性。结果表明,这些CAR-T细胞能够有效地识别和杀死表达EDB或COL11A1的肿瘤细胞,证实了这些CSE靶点的有效性。
虽然从这些潜在CSE靶点的发现道临床应用,仍需要进一步验证其安全性,并评估脱靶毒性,这项研究为开发更安全、更有效的儿童实体瘤和脑瘤免疫疗法奠定了基础。新发现的CSE靶点有望为更多患有高危或复发性肿瘤的儿童带来希望。


