NBE:浙江大学顾臻/王金强:长效智能胰岛素
时间:2023-12-10 12:37:16 热度:37.1℃ 作者:网络
葡萄糖反应型胰岛素制剂可提高其治疗指数,减轻给药负担。然而,很难开发出能够以持续和葡萄糖反应的方式释放胰岛素的单剂量制剂。
2023年12月6日,浙江大学顾臻及王金强共同通讯在Nature Biomedical Engineering在线发表题为“Week-long norm glycaemia in diabetic mice and minipigs via a subcutaneous dose of a glucose-responsive insulin complex”的研究论文,该研究报告了一种皮下注射葡萄糖反应制剂的发展,该制剂几乎不会触发纤维胶囊的形成,并导致1型糖尿病小鼠和小型猪持续一周的正常血糖和可忽略的低血糖。
该制剂由葡萄糖酸修饰的重组人胰岛素与4-羧基-3-氟苯硼酸修饰的聚赖氨酸通过葡萄糖响应苯硼酸-二醇络合和静电吸引紧密结合而成。当胰岛素复合物暴露于高葡萄糖浓度时,聚合物的苯硼酸部分迅速与葡萄糖结合,破坏络合并降低聚合物的正电荷密度,从而促进胰岛素的释放。这种长效单剂量制剂的治疗效果支持其进一步评估和临床转化研究。

糖尿病是一种慢性疾病,影响着全世界超过5.37亿成年人。超过20%的糖尿病患者需要胰岛素替代治疗来维持血糖水平在正常范围内。许多不同的胰岛素配方和输送方式已被开发,以改善血糖管理。例如,将长效“基础”胰岛素与速效胰岛素随餐结合使用是一种有效的方案,可将空腹和餐后血糖维持在正常范围内。然而,胰岛素治疗是负担沉重的,因为它需要每天多次皮下注射。此外,胰岛素受一系列生理和环境因素影响的;因此,对糖尿病患者来说,准确地给胰岛素剂量是一项挑战,而胰岛素治疗可能与白天和夜间大量的高血糖和低血糖有关。迫切需要新的胰岛素递送策略,有效调节血糖,但减少注射频率。
葡萄糖反应性胰岛素(GRI)可以模拟β细胞的功能,通过动态释放胰岛素来响应血糖的变化;因此,这种胰岛素治疗方法代表了目前可用的胰岛素制剂的一个有希望的替代方案。GRI感知血糖波动,动态调节胰岛素释放率,调节血液胰岛素水平,实时调节血糖。GRI的动态成分可以扩大胰岛素的治疗指数,减少在不合理的胰岛素给药剂量下发生的高血糖和低血糖发作。三种葡萄糖反应机制,苯硼酸(PBA)衍生物、葡萄糖结合分子和葡萄糖氧化酶,已被广泛探索构建GRI。其中,基于PBA的GRI进展迅速,并且基于快速且稳健的体外和体内GRI释放性能,具有临床应用潜力。然而,研制一种能够在单次给药后将血糖调节在正常范围内一周以上的GRI仍然是一个挑战,这需要胰岛素制剂同时具备餐后快速胰岛素释放和持续、持续的“基础”胰岛素释放的能力。
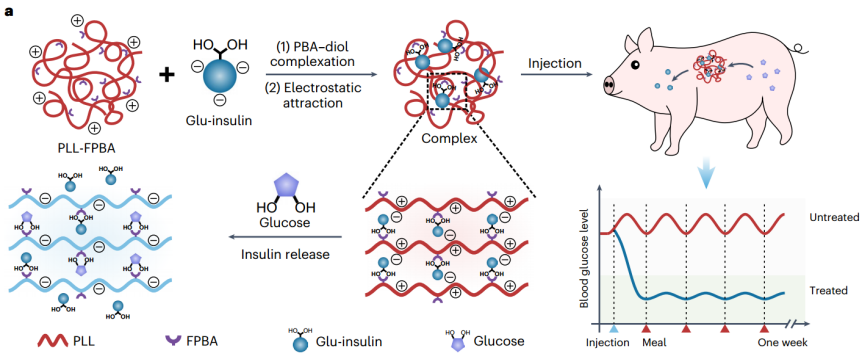
机理模式图(图源自Nature Biomedical Engineering )
该研究描述了一种葡萄糖反应型胰岛素方案,既能释放GRI,又能发挥长效作用。在这个方案里,重组人胰岛素与葡萄糖酸共价修饰,产生具有二醇部分的胰岛素类似物(葡萄糖胰岛素)。葡萄糖-胰岛素可与4-羧基3-氟苯硼酸(FPBA)-改性聚-L-赖氨酸(PLL-FPBA)通过动态静电吸引和PBA-二醇络合形成稳定的配合物。在血糖正常的情况下,强静电力和PBA-二醇络合作用使得复合制剂在游离状态下释放超少量的胰岛素,提供缓慢而持续的胰岛素释放,并允许高剂量。在高血糖状态下,葡萄糖与FPBA基团的结合瞬间降低了PLL-FPBA的正电荷密度,并解构了苯硼酸酯键,从而降低了葡萄糖-胰岛素与聚合物之间的静电吸引力和苯硼酸酯键的密度,最终促进胰岛素释放。
在化学诱导的1型糖尿病小鼠模型中,皮下注射的胰岛素复合物在皮肤下形成一个仓库,将血液胰岛素水平维持在稳定的“基础”水平和正常范围内的BG水平。在葡萄糖管理,升高的BG触发快速胰岛素释放从复杂的仓库,纠正升高的BG水平。当BG恢复到正常范围时,降低的BG向复合物提供负反馈信号,降低胰岛素释放速率。该GRI可在给药后达到一周的正常血糖,低血糖发生率最低。此外,抗高血糖作用持续超过20天,即使在治疗后一周,皮下胰岛素储存量的稳步减少不足以将BG维持在正常水平以下。这种长效单剂量制剂的治疗效果支持其进一步评估和临床转化研究。
原文链接:
https://www.nature.com/articles/s41551-023-01138-7


