Mol Ther:鲜人参能逆转冷肿瘤,增强肿瘤免疫治疗的作用
时间:2021-09-19 20:22:08 热度:37.1℃ 作者:网络
以低效应T细胞浸润为标志的冷肿瘤微环境 (TME) 导致对免疫检查点抑制剂 (ICI) 治疗的反应较弱。因此,将冷热TME转换为改善有效ICI治疗的关键。
南京中医药大学曹鹏、曹萌等发现人参衍生纳米颗粒通过重编程冷肿瘤微环境来增强免疫检查点抗体的功效。研究发表在近日的Mol Ther上。
此前,作者报道了一种细胞外囊泡 (EVs) 样人参衍生纳米粒子 (GDNPs),它从人参中分离出来,可以改变 M2 极化以延迟热肿瘤 B16F10 的进展。研究结果发表在2019年J Immunother Cancer上。
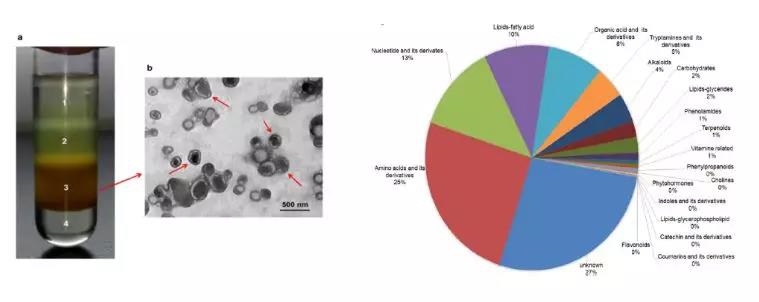
细胞外囊泡(extracellular vesicles,EVs)是由细胞分泌的纳米尺寸的脂质膜封闭结构。EVs作为细胞间通讯的重要介质,影响生理和病理状况。鉴于其转移生物活性成分和克服生物屏障的能力,EVs越来越多地被探索为潜在的治疗剂。目前对于细胞外囊泡的研究,主要集中在哺乳动物细胞上清液和体液,而植物,特别是药用植物囊泡领域的研究十分有限。 曹鹏研究团队从2016年开始开展了中药鲜药的研究,发现从新鲜人参的汁液中可以提取到类似于动物细胞分泌的胞外囊泡,并将这种囊泡命名为Ginseng-derived nanoparticles(GDNPs)。研究人员发现这种人参来源的植物囊泡的直径为300 nm左右。多组学分析显示,GDNPs富含多种人参来源的蛋白、脂类、核酸和小分子。
研究发现GDNPs对单核-巨噬细胞有着很强的亲嗜性,能够被巨噬细胞有效地吞噬,同时促进巨噬细胞向具有抗肿瘤作用的M1型巨噬细胞极化,并且极化的巨噬细胞分泌大量ROS杀伤肿瘤。经过进一步的分析,证实GDNPs极化巨噬细胞的主要机制是通过其含有的神经酰胺(Ceramide)活化巨噬细胞表面的Toll样受体4(TLR4)。荷瘤小鼠实验结果表明GDNPs的治疗有效促进肿瘤微环境中的肿瘤相关巨噬细胞(tumor associated macrophage,TAM)向抗肿瘤的M1型巨噬细胞极化,解除肿瘤微环境免疫抑制状态,活化CD8+T淋巴细胞和NK细胞,抑制黑色素瘤的生长。
然而,冷肿瘤在现实世界中更为常见和具有挑战性。该研究探索了GDNPs和PD-1(程序性死亡-1)mAb 的组合策略,该策略表现出改变冷TME 的能力,随后在多个小鼠肿瘤模型中诱导持久的全身抗肿瘤免疫。 GDNPs增强了PD-1 mAb激活肿瘤浸润T淋巴细胞的抗肿瘤功效。研究结果表明,GDNPs 可以重编程肿瘤相关巨噬细胞 (TAMs) 以增加CCL5和CXCL9的分泌,以将CD8+T细胞募集到肿瘤床中,这与PD-1 mAb治疗具有协同作用,且未检测到全身毒性。GDNPs原位激活TAMs可以广泛地作为一个简单的平台来调节抑制性冷TME并在未来的临床应用中优化PD-1 mAb 免疫治疗。
该研究发现囊泡是鲜药人参发挥药效的重要物质基础,加深了对中药的科学认识,为拓展鲜药利用途径带来新的启示; 同时也是首次发现药用植物来源的囊泡具有重编程肿瘤相关巨噬细胞的功能,GDNPs对于肿瘤的免疫治疗可能带来新的希望。
原始出处:
Han X, Wei Q, Lv Y, Weng L, Huang H, Wei Q, Li M, Mao Y, Hua D, Cai X, Cao M, Cao P.Ginseng-derived nanoparticles potentiate immune checkpoint antibody efficacy by reprogramming the cold tumor microenvironment.Mol Ther. 2021 Aug 25:S1525-0016(21)00422-6
Cao M, Yan H, Han X, Weng L, Wei Q, Sun X, Lu W, Wei Q, Ye J, Cai X, Hu C, Yin X, Cao P.Ginseng-derived nanoparticles alter macrophage polarization to inhibit melanoma growth.J Immunother Cancer. 2019 Nov 27;7(1):326

