闫创业团队《自然-通讯》:揭示甲状腺激素转运蛋白MCT8的结构之谜
时间:2025-04-03 12:09:37 热度:37.1℃ 作者:网络
甲状腺激素(Thyroid hormones,THs)是由甲状腺分泌的碘化氨基酸类激素,主要包括T4(3,5,3′,5′-tetraiodo-L-thyronine,四碘甲状腺原氨酸)和T3(3,5,3′-triiodo-L-thyronine,三碘甲状腺原氨酸)。它们是人体内至关重要的信号分子,不仅调控着从胚胎发育到成年的几乎所有组织的生长分化,还持续调节着机体的基础代谢率。其代谢异常经常导致多种疾病,如甲状腺功能亢进(甲亢)与减退(甲减)。
在众多介导THs跨膜转运的膜蛋白中,单羧酸转运蛋白MCT8(monocarboxylate transporter 8)因其对TH分子独特的选择性识别能力和高效的转运效率而成为研究热点。值得注意的是,MCT8是目前在人类中发现的唯一与THs遗传性疾病直接相关的转运蛋白,其功能缺陷会影响THs通过血脑屏障进入中枢神经系统,进而导致Allan-Herndon-Dudley综合征(AHDS)——一种以严重智力障碍和运动功能障碍为主要临床表现的X连锁遗传病。尽管全球科学家对MCT8已开展多年深入研究,但其致病的分子机制和潜在治疗策略仍有许多未解之谜。
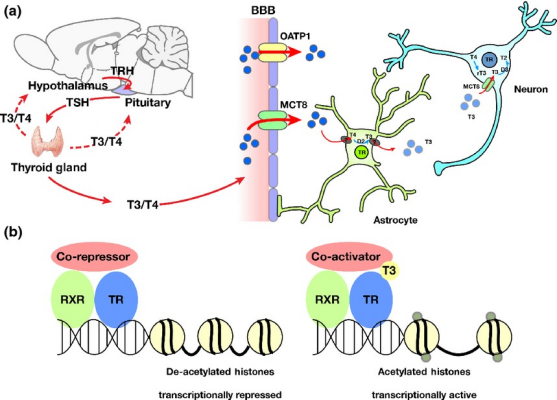
图1 MCT8是血脑屏障中负责运输THs的主要转运体(Richa Kapoor, et al. 2015)
在THs代谢过程中,甲状腺滤泡细胞主要分泌T4,而具有更高生物活性的T3则通过外周组织中T4的脱碘转化产生,同时伴随着无活性代谢物rT3(reverse T3, 3,3′,5′-triiodo-L-thyronine)和T2(3,3′-diiodo-L-thyronine)的生成。此前研究发现,MCT8对不同TH分子表现出明显的结合偏好性:T3>T4»rT3≈T2,这种选择性与其生理功能高度匹配。同时,已有研究表明MCT8可能以同源二聚体形式发挥功能,但其精确的二聚化调控机制仍有待揭示。此外,目前仅有少数化合物被证实能够调节MCT8活性,其中水飞蓟素(silychristin)作为具有抗氧化和抗炎特性的天然产物,虽在肝病治疗中表现出色,但其对甲状腺激素系统的潜在干扰效应也引起了研究者的高度关注。因此,获得MCT8与底物或抑制剂的高分辨率三维结构,对于阐明其转运机制和底物特异性具有重要意义,对开发针对MCT8相关疾病的新型治疗策略也具有重要意义。
清华大学闫创业课题组长期专注于重要疾病相关的溶质转运体(Solute carrier,SLC)超家族蛋白的结构与功能研究,在冷冻电镜方法学和应用研究方面取得系列突破。该团队已成功解析了包括单羧酸转运蛋白MCT1(Cell, 2021)、葡萄糖转运蛋白GLUT4(Nat Commun, 2022)、γ-氨基丁酸转运蛋白GAT1(NSMB, 2023)和去甲肾上腺素转运蛋白NET(Nature, 2024)在内的多个重要SLC成员的高分辨率结构,为理解这类膜转运蛋白的工作机制与药物作用机制奠定了坚实基础。
2025年3月26日,清华大学生命科学学院/北京生物结构前沿研究中心闫创业课题组在《自然通讯》(Nature Communications)上发表了题为“甲状腺激素转运蛋白MCT8的结构与功能研究”( Structural insights into thyroid hormone transporter MCT8)的科研论文。这项研究解析了MCT8与底物T3及抑制剂水飞蓟素结合的高分率结构,揭示了MCT8二聚化和不同THs选择性的结构基础,为理解 THs 转运及其相关疾病的治疗策略开发提供了新的视角(图2)。
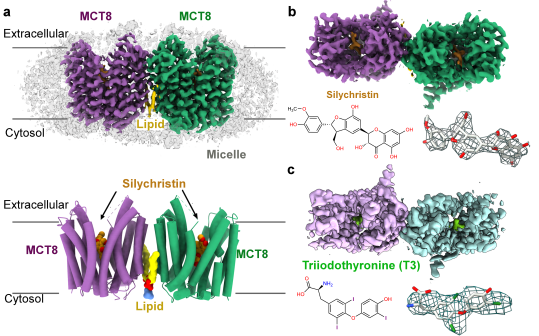
图 2 底物与抑制剂结合的MCT8同源二聚体结构
研究团队采用冷冻电镜技术成功解析了人源MCT8蛋白的两种高分辨率结构,分别捕获了其与底物T3及高亲和力抑制剂水飞蓟素结合的状态。两种结构中,MCT8均以向外开放构象的同源二聚体形式存在(图2)。其中,MCT8 对 TH 的识别和转运长期以来一直受到关注,其结构解析揭示了MCT8对不同THs的选择性差异背后的分子机制。MCT8具有三个特异的疏水碘结合口袋, T3的3-、5-和3'-碘原子分别嵌入其中,而T4的5'-碘原子将处于一个额外的半疏水性口袋,导致其结合亲和力低于T3。对于代谢产物T2和rT3,其3-或5-碘原子的缺失导致关键疏水作用减少,且rT3的5'-碘原子与T4类似,被置于半疏水性口袋(图3)。这些结构差异合理解释了MCT8对T3/T4的优先转运特性。研究还进一步揭示了作为肝病治疗药物水飞蓟素对MCT8抑制的分子机制,为优化水飞蓟素使其避免干扰甲状腺激素稳态提供了结构基础。此外,AHDS 缺陷表型的严重程度与每个突变体的残余 T3 运输能力相关。通过将临床疾病遗传突变映射至结构模型并结合AlphaFold预测,研究揭示了不同突变导致T3转运能力丧失的潜在分子机制。
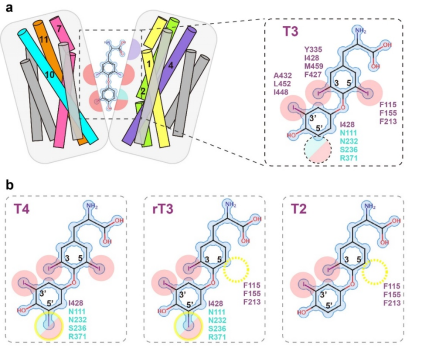
图 3 甲状腺激素T3、T4、rT3及T2的潜在结合模式分析
研究还进一步揭示了MCT8二聚化的分子机制,其界面主要由跨膜螺旋TM3和TM6构成。值得注意的是,在二聚化界面处还存在一个脂质分子介导其相互作用(图1a)。通过定点突变(Phe182、His186或Phe271突变为Ala)及生化实验验证,团队证实这些残基对二聚体形成具有关键作用。尽管体外转运实验表明二聚化破坏未显著影响T3摄取,但研究者猜测二聚化可能通过稳定跨膜区亲水残基,促进MCT8在细胞膜上的定位与功能。
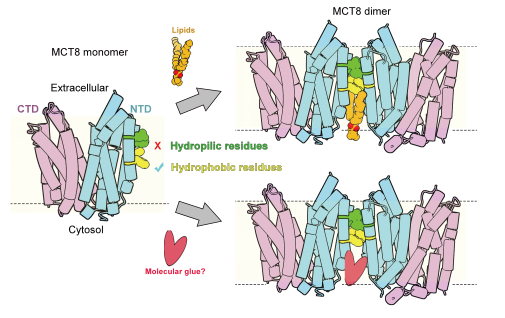
图 4 脂质可能作为分子胶促进MCT8二聚体的形成及稳定
本研究为靶向甲状腺轴转运蛋白MCT8的新型抑制剂开发提供了结构基础,有助于促进发展治疗甲状腺激素代谢异常疾病的新型药物。同时,在二聚体界面发现的脂质“锚定”现象也为设计模拟脂质分子的“分子胶”以促进MCT8二聚体形成,增强其在血脑屏障细胞中的定位与功能,为治疗AHDS提供了新思路(图4)。
清华大学生命科学学院/北京生物结构前沿研究中心副教授闫创业为本文唯一通讯作者;清华大学生命学院水木学者谭佳鑫,2021级博士生肖媛和孔方为本文的共同第一作者。实验室成员钱嘉威和朱盎岐博士对本研究提供了重要帮助。实验的电镜数据采集受到清华大学冷冻电镜平台的支持,实验的计算工作得到清华大学高性能计算平台、国家蛋白质设施实验技术中心(北京)的支持。本研究获得了北京生物结构前沿研究中心、清华-北大生命科学联合中心、国家自然科学基金面上项目及生物膜国家重点实验室的经费支持。
[1] Kapoor, R. et al. Perspectives on thyroid hormone action in adult neurogenesis. J Neurochem 133, 599-616. 10.1111/jnc.13093 (2015).
[2] Wang, N. et al. Structural basis of human monocarboxylate transporter 1 inhibition by anti-cancer drug candidates. Cell 184, 370–383.e13 (2021).
[3] Yuan, Y. et al. Cryo-EM structure of human glucose transporter GLUT4. Nat. Commun. 13, 2671 (2022).
[4] Zhu, A., Huang, J., Kong, F. et al. Molecular basis for substrate recognition and transport of human GABA transporter GAT1. Nat Struct Mol Biol 30, 1012–1022 (2023).
[5] Tan, J., Xiao, Y., Kong, F. et al. Molecular basis of human noradrenaline transporter reuptake and inhibition. Nature 632, 921–929 (2024).


