ATVB 山东大学齐鲁医院郝盼盼教授团队揭示MrgD调控肺动脉高压的新机制
时间:2025-04-02 12:08:46 热度:37.1℃ 作者:网络
肺动脉高压(Pulmonary Arterial Hypertension, PAH)是以肺血管阻力进行性升高为特征的致死性疾病,其病理核心为肺动脉平滑肌细胞(Pulmonary artery smooth muscle cells, PASMCs)异常增殖和肺血管重塑。尽管现有血管扩张剂可短暂缓解症状,但无法逆转疾病进程,终末期患者依赖肺移植。因此,探索PAH发病新机制及干预靶点具有重要临床意义。
关于Mas相关G蛋白偶联受体D (MrgD)最早的研究集中于神经系统,近年被证实在心血管系统中高表达,并具有抑制炎症反应、促进血管舒张、改善纤维化等保护作用。然而,MrgD在PAH发病和病程进展中的功能和作用机制尚不明确。
2025年3月27日,山东大学齐鲁医院心内科和络病理论创新转化全国重点实验室郝盼盼教授团队在Arteriosclerosis, Thrombosis, and Vascular Biology上发表了题为“MrgD as a novel modeling and treatment target for pulmonary hypertension”的研究论文。该研究利用MrgD敲除小鼠构建了全新的PAH动物模型,并通过多维度研究首次阐明MrgD通过AKT-MAZ-PIM1信号轴调控缺氧性PAH的分子机制,为PAH提供一个新的预防和治疗靶点。

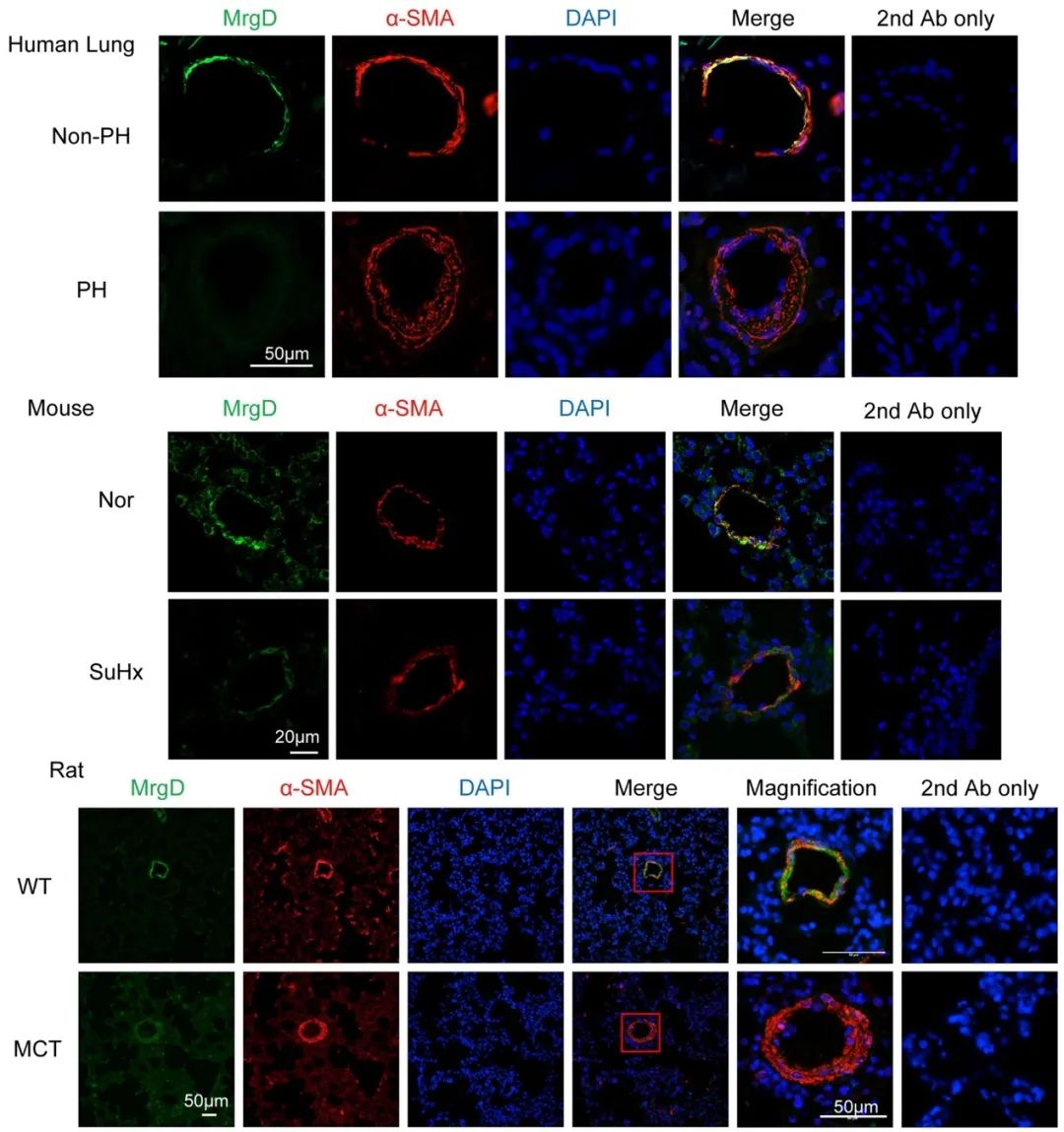
首先,研究团队通过临床样本分析、低氧培养的人源PASMCs、野百合碱(MCT)诱导的PAH大鼠、SU5416联合缺氧(SuHx)诱导的PAH小鼠证实:在PAH患者肺组织及多种PAH模型中,MrgD表达均显著下降,提示其可能参与疾病进展。
为了探究MrgD在PAH中的作用,作者构建了MrgD全身敲除(MrgD KO)小鼠。MrgD KO小鼠表现出右心室压力升高、右心室肥厚及肺动脉重塑等PAH表型。与SuHx诱导的PAH小鼠模型相比,MrgD KO诱导的PAH模型的上述各项指标无显著性差异。SuHx联合MrgD KO小鼠则呈现出比单纯SuHx诱导PAH模型或单纯MrgD KO小鼠更为严重的PAH表型。上述结果表明,MrgD缺失会诱导和加剧缺氧性PAH的病理变化,为探索该疾病的发病机制提供了新线索。
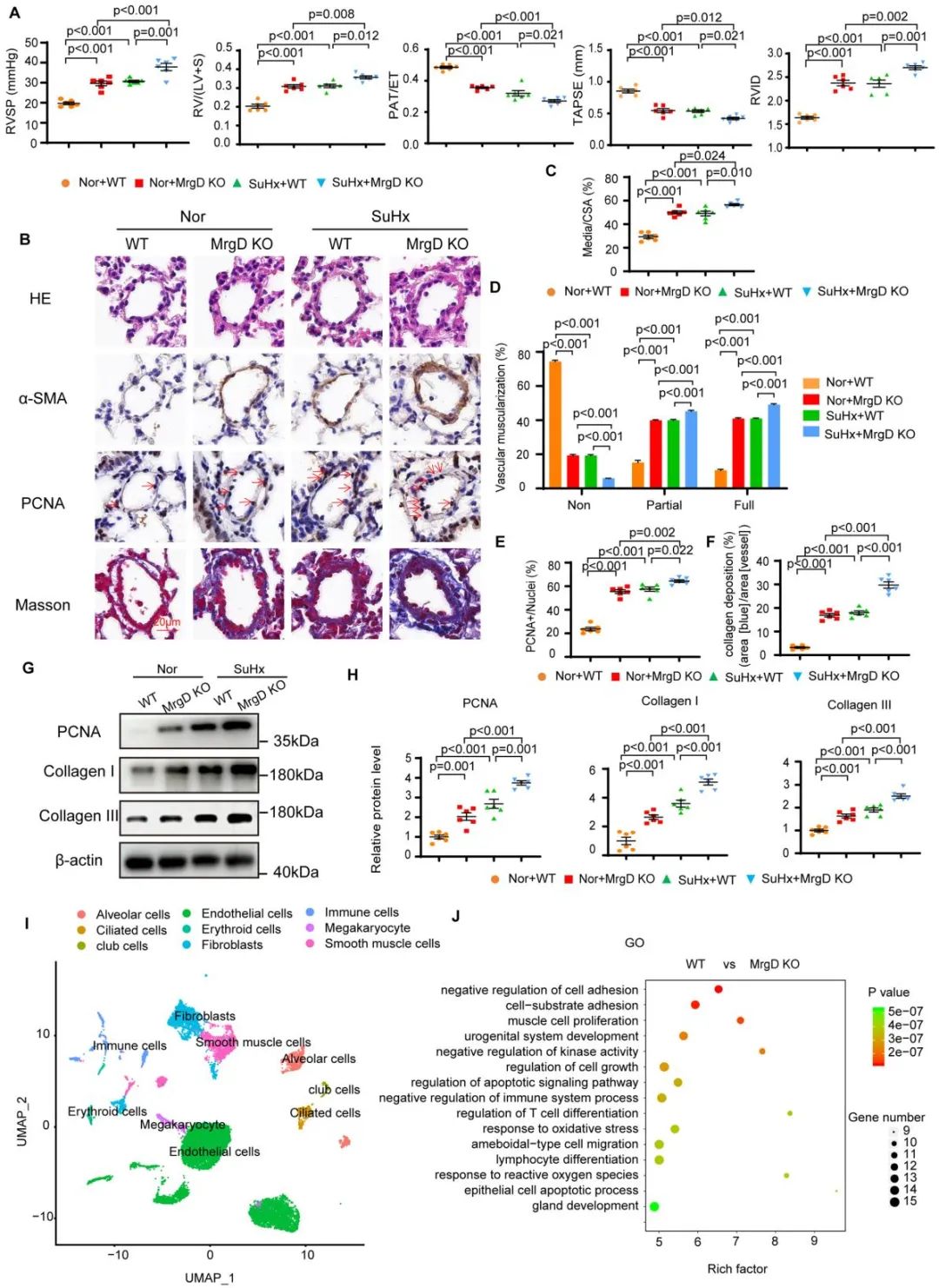
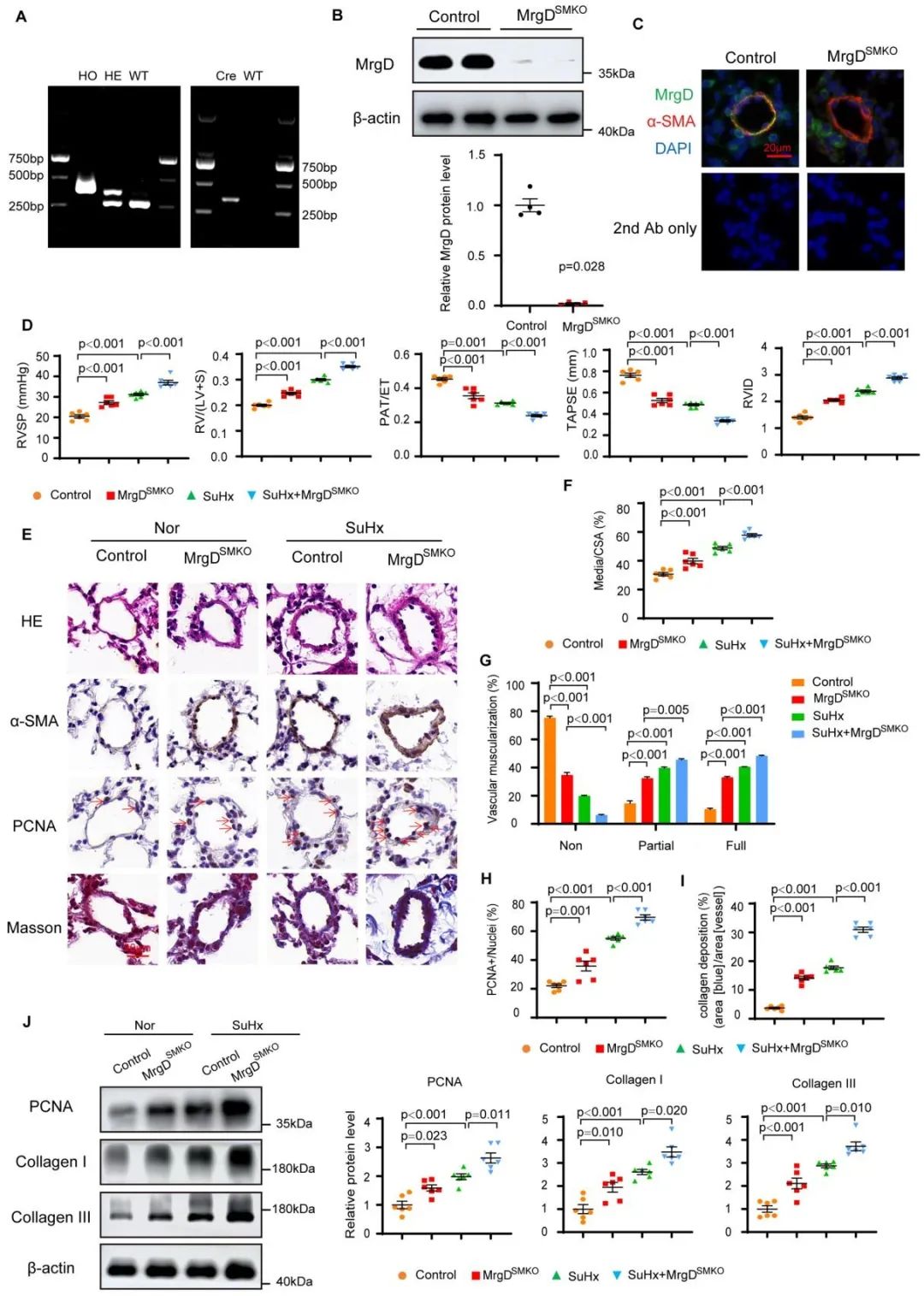
单细胞测序结果显示,平滑肌细胞增殖在MrgD KO诱导PAH中起到至关重要的作用。为了在平滑肌细胞中探究MrgD如何调控PAH进展,作者构建了MrgD平滑肌细胞特异性敲除(MrgDSMKO)小鼠模型。与全身敲除小鼠相比,MrgDSMKO小鼠呈现出类似的PAH表型,且平滑肌细胞特异性MrgD缺失可加剧SuHx诱导的右心室压力升高、右心室肥厚和肺动脉重塑。
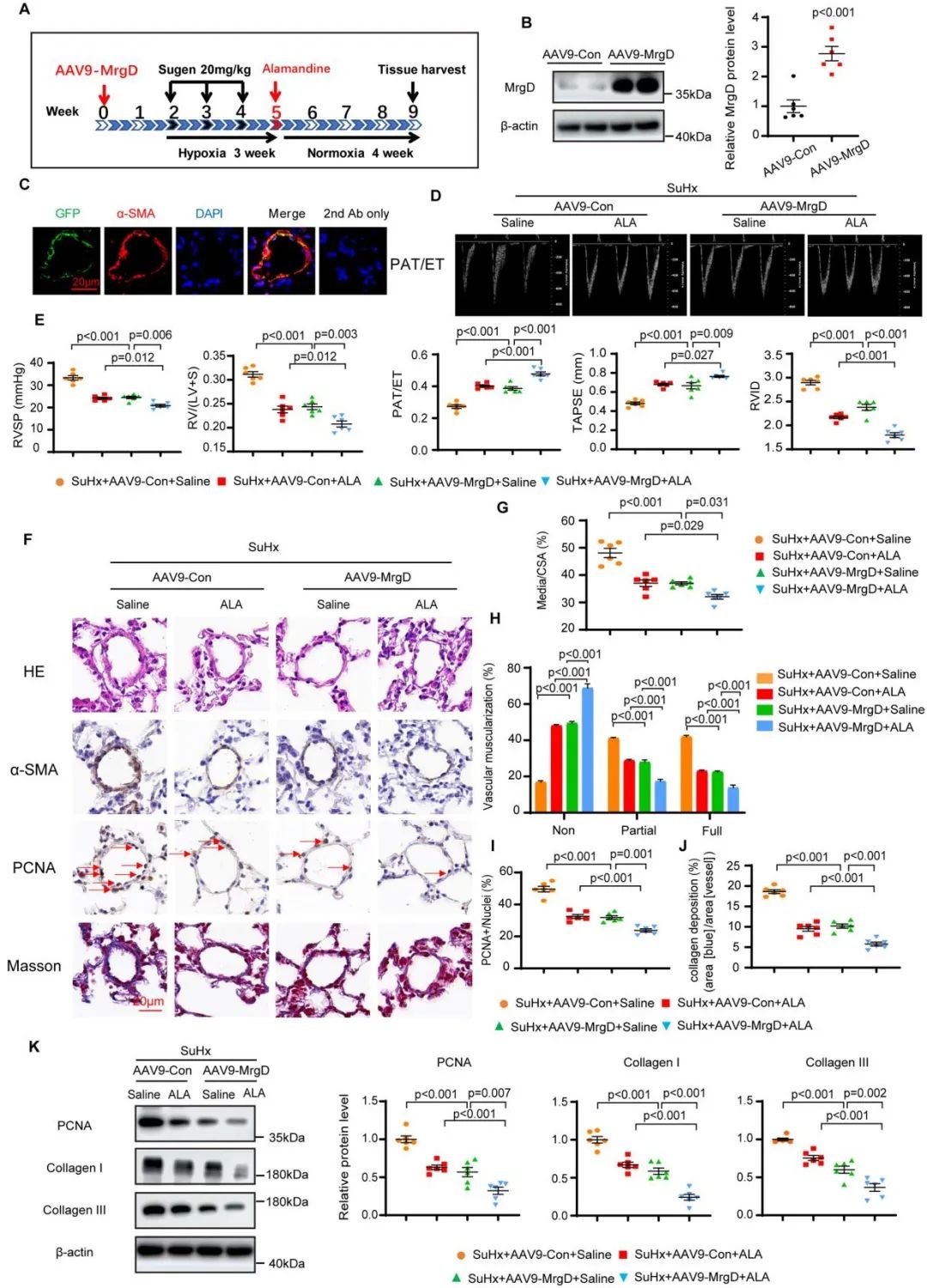
随后,作者分别利用平滑肌特异性过表达MrgD的腺相关病毒(AAV9-SM22α-MrgD)和MrgD激动剂Alamandine干预SuHx诱导的PAH小鼠模型。平滑肌过表达MrgD或Alamandine干预均可明显减轻缺氧PAH小鼠模型的右心室腔扩张、右心室压力升高、右心室肥厚以及肺血管重塑,而Alamandine联合AAV9-SM22α-MrgD干预可以进一步改善小鼠的PAH表型。
此外,作者利用MrgD激动剂Alamandine干预MCT诱导的PAH大鼠模型。结果显示,Alamandine干预明显减轻PAH大鼠的右心室腔扩张、右心室压力升高、右心室肥厚以及肺血管重塑。为了证明Alamandine是否通过MrgD发挥作用,作者利用Alamandine干预MrgD KO小鼠。右心导管检测、RV/(LV+S)分析以及超声检测结果显示,Alamandine干预没有减轻MrgD KO小鼠的PAH表型。同时,体外实验也证明,Alamandine通过激活MrgD改善低氧刺激对人源PASMCs的促增殖及胶原产生作用。上述结果表明,肺动脉平滑肌中MrgD缺失会诱导和加剧PAH的病理变化;反之,过表达MrgD或给予其天然配体Alamandine可有效缓解上述表型,且该效应依赖MrgD受体存在。

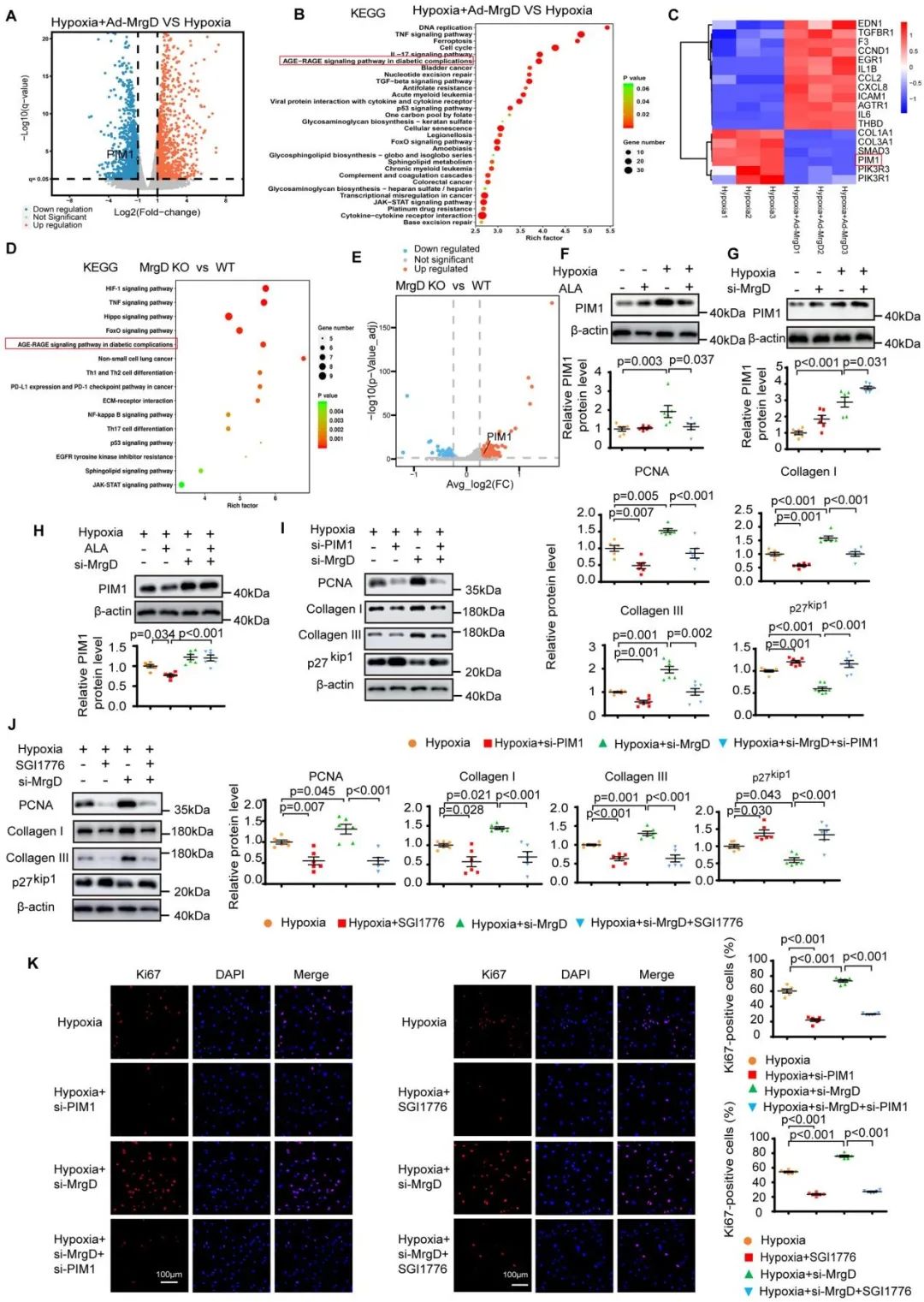
为了探讨MrgD调控PASMCs增殖和胶原分泌的作用机制,作者首先利用单细胞测序分析与转录组学锁定PIM1为MrgD下游关键靶基因,并通过Western Blot和RT-PCR证实MrgD下调PIM1表达。分别利用si-MrgD、si-PIM1和PIM1抑制剂SGI1776干预PASMCs,Western Blot、Ki67免疫荧光染色、EdU等实验结果显示,PIM1小干扰或抑制剂可挽救MrgD缺失诱导/加剧的PASMCs增殖和胶原表达,表明MrgD通过靶向下调PIM1抑制PASMCs增殖及胶原表达。
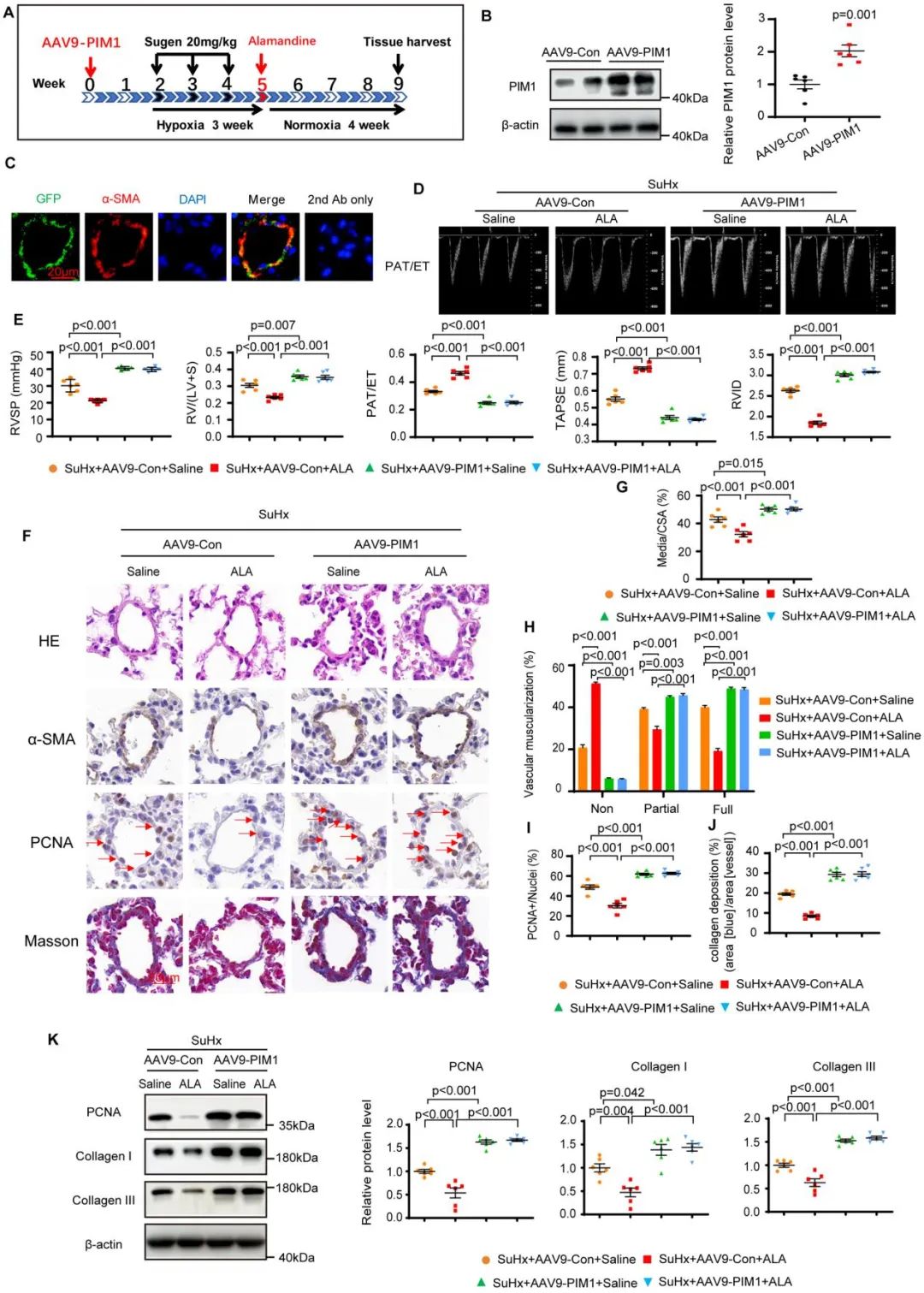
为了在动物实验中探究MrgD是否通过PIM1发挥作用,作者构建了携带SM22α启动子驱动PIM1的腺相关病毒(AAV9-SM22α-PIM1),尾静脉注射以过表达PIM1。结果显示,过表达PIM1可抵消MrgD激动剂Alamandine改善缺氧PAH小鼠模型的右心室压力升高、右心室肥厚及肺血管重塑的作用。为了增强其临床转化价值,作者利用PIM1抑制剂SGI1776干预MrgD KO小鼠,结果显示,SGI1776抑制PIM1可挽救MrgD KO小鼠的PAH表型。同时,在体外实验中,PIM1过表达干预可阻断Alamandine在低氧PASMCs 中的抗增殖和抗胶原表达作用。
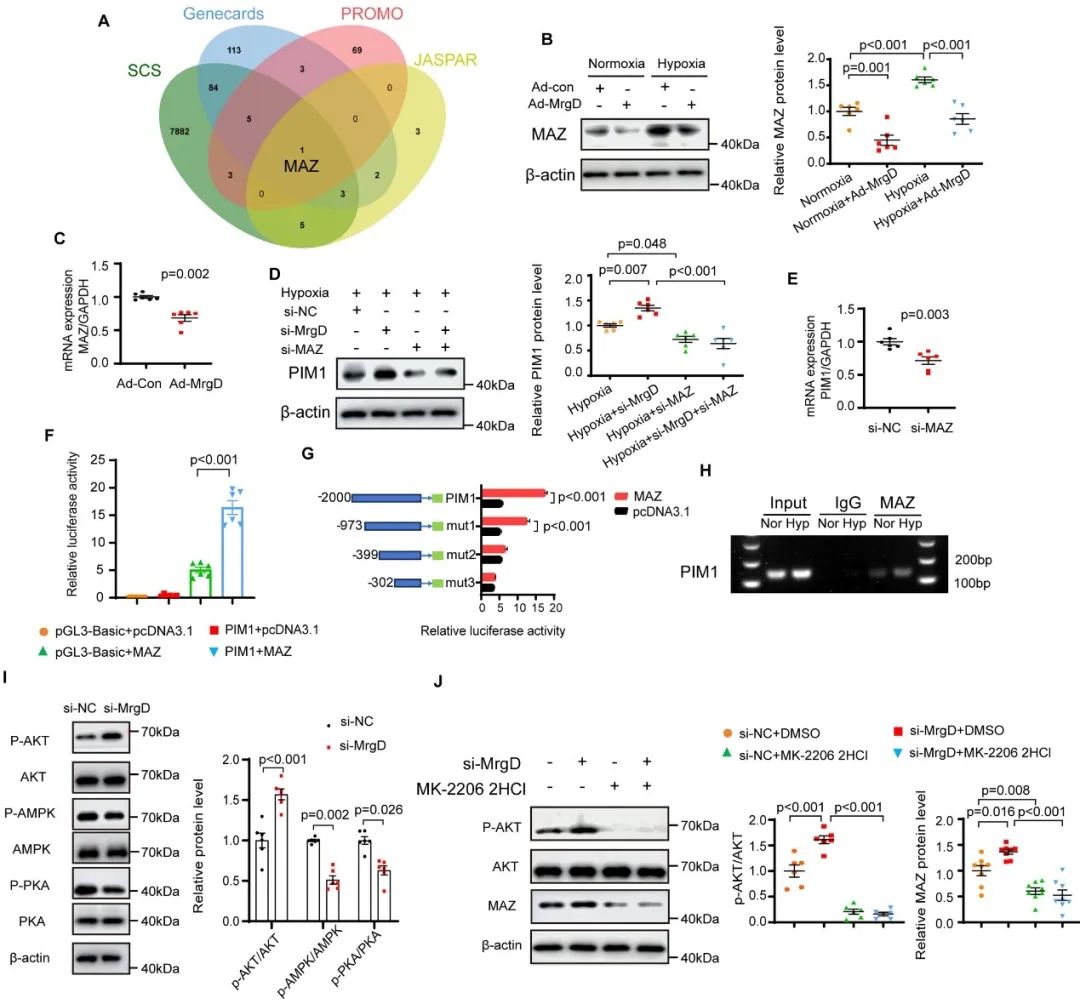
为了进一步探究MrgD调控PIM1的具体机制,作者利用Genecards、JASPAR、PROMO数据库和MrgD KO小鼠肺组织单细胞测序交集预测出PIM1启动子序列的转录因子MAZ,并通过Western Blot和RT-PCR检测证实MrgD下调MAZ表达。为了明确PIM1启动子中MAZ结合的靶序列,作者进行双荧光素酶和染色质免疫沉淀实验,确定MAZ直接与PASMCs中PIM1启动子的-973至-399bp区域结合。为了确定MrgD调节MAZ的特定信号途径,作者针对MrgD下游信号通路进行初步筛选和验证。结果显示,MrgD敲低可明显改变AKT、AMPK和PKA的磷酸化水平。AMPK或PKA激动剂不会改变MAZ蛋白的表达,然而使用AKT抑制剂MK-2206 2HCl处理后,MAZ蛋白水平显著降低。AKT抑制剂MK-2206 2HCl可挽救PASMCs中MrgD敲低引起的MAZ蛋白表达增加。研究结果表明,MrgD通过AKT-MAZ信号通路调节PIM1转录。
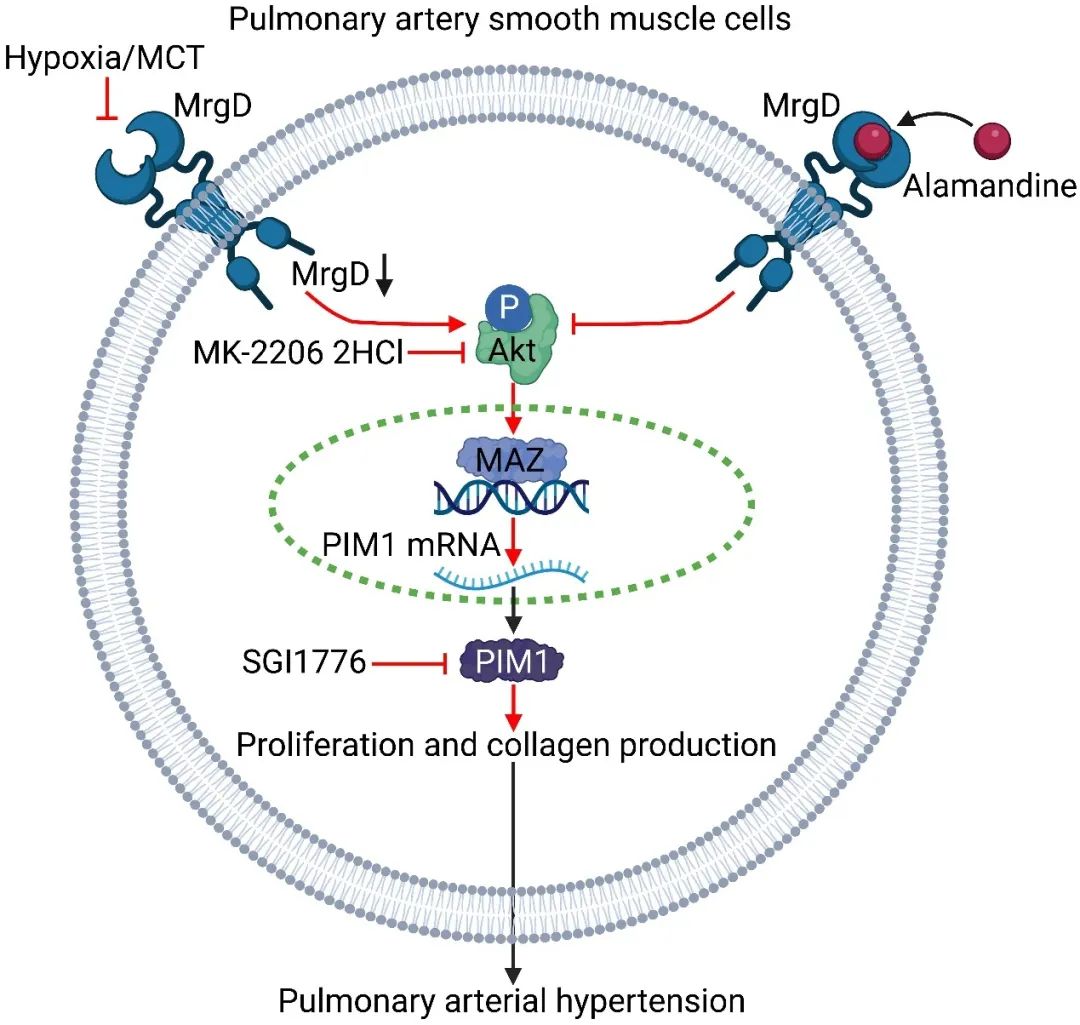
综上,这项研究表明:MrgD缺失通过激活AKT磷酸化,上调转录因子MAZ表达;MAZ直接结合PIM1启动子(-973至-399 bp区域),驱动PASMCs增殖与胶原沉积;使用PIM1抑制剂SGI1776或敲低PIM1可挽救MrgD缺失导致的病理表型,证实MrgD-PIM1轴的核心调控作用。本研究首次揭示MrgD通过AKT-MAZ-PIM1信号轴调控缺氧性PAH的核心机制,不仅为理解PAH病理进程提供了新视角,更奠定了MrgD作为治疗靶点的理论基础。基于Alamandine的受体激动策略及PIM1抑制剂的联合应用,有望开发出逆转肺血管重塑的创新疗法。
本论文第一作者为山东大学齐鲁医院心内科博士研究生钟鸿钰,通讯作者为郝盼盼教授。研究工作依托山东大学齐鲁医院心内科和络病理论创新转化全国重点实验室完成。
原文链接:
https://www.ahajournals.org/doi/10.1161/ATVBAHA.124.322337


