ctDNA预测EGFR突变肺癌埃克替尼治疗疗效,4周时转阴患者生存预后显著较优
时间:2024-11-17 15:00:21 热度:37.1℃ 作者:网络
血浆表皮生长因子受体突变(EGFRm)循环肿瘤 DNA(ctDNA)动力学在预测 EGFRm 晚期非小细胞肺癌(NSCLC)患者的预后方面显示出前景。然而,将 ctDNA 监测整合到临床实践中的试验水平的数据仍然有限。我们进行了一项前瞻性、多中心试验,探索 EGFRm ctDNA 动态变化与 EGFRm NSCLC 患者临床结局之间的关系。招募了 98 例初治 EGFRm 晚期 NSCLC 患者,接受埃克替尼治疗直至疾病进展。在基线和埃克替尼给药后 4 周收集血浆样本。使用微滴式数字聚合酶链反应(ddPCR)分析 ctDNA。基线时,71.4% 的患者 EGFRm ctDNA 阳性。其中,45.9% 的患者在治疗 4 周内 ctDNA 转阴。这些患者的无进展生存期(PFS)和总生存期(OS)显著长于治疗后 ctDNA 保持阳性的患者(P 分别为 0.004 和 < 0.001),与基线和 4 周时 ctDNA 均阴性的患者相似。4 周时 ctDNA 阳性是 PFS 和 OS 较差的独立危险因素。治疗后 ctDNA 转阴的患者与最初 ctDNA 阴性的患者结局相似,强调了 ctDNA 动力学对治疗疗效的预测价值。
研究背景
表皮生长因子受体突变(EGFRm)是晚期非小细胞肺癌(NSCLC)中最常见的可靶向致癌驱动突变。在过去的二十年里,敏感 EGFRm 晚期 NSCLC 的治疗格局发生了重大变化。多种 EGFR 酪氨酸激酶抑制剂(TKI)已获批用于临床,包括第一代抑制剂厄洛替尼、吉非替尼和埃克替尼,第二代抑制剂阿法替尼和达可替尼,第三代抑制剂 奥希替尼。此外,还探索了 EGFR-TKI 与其他抗癌药物(如化疗或血管生成抑制剂)的联合策略,用于延长患者生存期。Flaura 2 试验表明,与奥希替尼单药治疗相比,奥希替尼联合化疗提供了具有统计学意义和临床意义的无进展生存期(PFS)获益。
尽管最初 EGFR-TKI 的缓解率很有希望(50-80%),但观察到临床获益持续时间和进展模式的显著异质性。因此,寻找预测性生物标志物是改善患者预后的主要问题之一。此外,靶向治疗的最佳顺序仍不清楚。目前,没有临床或分子预测标志物可用于识别可能从不同治疗方法中获益的患者。最后,联合治疗需要进一步探索。
循环肿瘤 DNA(ctDNA)由恶性肿瘤患者癌细胞脱落到血浆中的 DNA 片段组成,占循环游离 DNA 的一小部分。ctDNA 的显著优势包括与组织活检相比,具有非侵入性,可以更好地体现肿瘤异质性。使用特异和灵敏的技术检测 ctDNA,例如微滴式数字聚合酶链反应(ddPCR)和下一代测序(NGS),显示出纵向监测治疗结果、检测微小残留病(MRD)、预后和选择适当治疗的潜力。连续血浆分析显示,治疗 3 至 6 周后检测不到 EGFRm ctDNA 的晚期 NSCLC 患者的中位 PFS 比检测到 ctDNA 的患者长。然而,尽管这些应用显示出前景,但其与临床实践的常规整合需要进一步的证据。在晚期 NSCLC 中,ctDNA 动态变化与 EGFR-TKI 治疗结局相关性的试验水平的数据仍然有限。
ddPCR 是一种经过充分验证的针对特定靶基因的 ctDNA 检测方法,比 NGS 提供更高的时间和成本效益。本文报道了我们的真实世界、前瞻性、多中心 II 期试验,试验纳入了一组接受埃克替尼一线治疗的 EGFRm 晚期 NSCLC 患者。连续采集血浆样本使用 ddPCR 进行 EGFRm ctDNA 分析。本研究在试验水平探索了基线和治疗期间 EGFRm ctDNA 动力学与临床结局的相关性。
研究结果
患者特征
从 2017 年 1 月到 2018 年 11 月,共招募了 100 例符合条件的患者。关键的资格标准包括:(1)年龄在 18 至 80 岁之间;(2)组织学或细胞学证实 IIIB/C 或 IV 期 NSCLC;(3)东部肿瘤协作组体能状态(ECOG PS)评分在 0 到 2 之间;(4)肿瘤组织检出常见激活 EGFRm(Ex 19del 或 L858R 突变)。排除诊断为晚期 NSCLC 后接受过全身治疗的患者。此外,携带罕见 EGFR 突变或具有其他可靶向基因共突变(如ALK、ROS1 或 BRAF V600E)的患者被排除在外。患者接受埃克替尼 125 mg,每日 3 次治疗,直至疾病进展(PD)或不可接受的毒性。在治疗前(基线)和治疗 4 周时收集血浆样本,使用微滴式数字聚合酶链反应(ddPCR)定量评估 EGFRm ctDNA 动力学。采用定制的 ddPCR 检测来检测血浆激活 EGFRm(Ex 19del 或 L858R)和 EGFR T790M 耐药突变。定制 ddPCR 检测的检出限为 ≤ 0.10% 的变异丰度(VAF)。在评估血浆 EGFRm 的检出和清除情况时,只包括血浆 EGFR Ex 19del 或 L858R 突变 ctDNA,不包括血浆 EGFR T790M 耐药突变。2 例患者撤回了知情同意。最后,98 例患者被纳入分析。图 1 展示了研究流程。所有患者均接受埃克替尼作为初始治疗。58 例患者(59.2%)为女性,患者中位年龄为 61 岁(四分位距,IQR 53-69)。86% 的患者从未吸烟。81 例患者(82.7%)为腺癌组织学亚型。大多数患者为 IV 期 NSCLC(93.9%)。40 例患者(40.8%)发生脑转移。39 例(39.8%)患者发生骨转移。EGFR Ex 19del 见于 50 例(51%)患者,EGFR L858R 突变见于 48 例(49%)患者。7 例(7.1%)患者基线时血浆 EGFR T790M 突变阳性。在一线治疗进展时,36 例(36.7%)患者检测到获得性耐药 T790M,45 例(45.9%)患者没有获得性耐药 T790M。17 例(17.3%)患者没有接受后续基因检测。一线治疗进展后,32 例患者接受了奥希替尼治疗,2 例患者接受了伏美替尼治疗,16 例患者未接受第三代 EGFR-TKIs 治疗,48 例患者不清楚是否接受了第三代 EGFR-TKIs 治疗。表 1 总结了关键的人口统计学和基线临床特征。
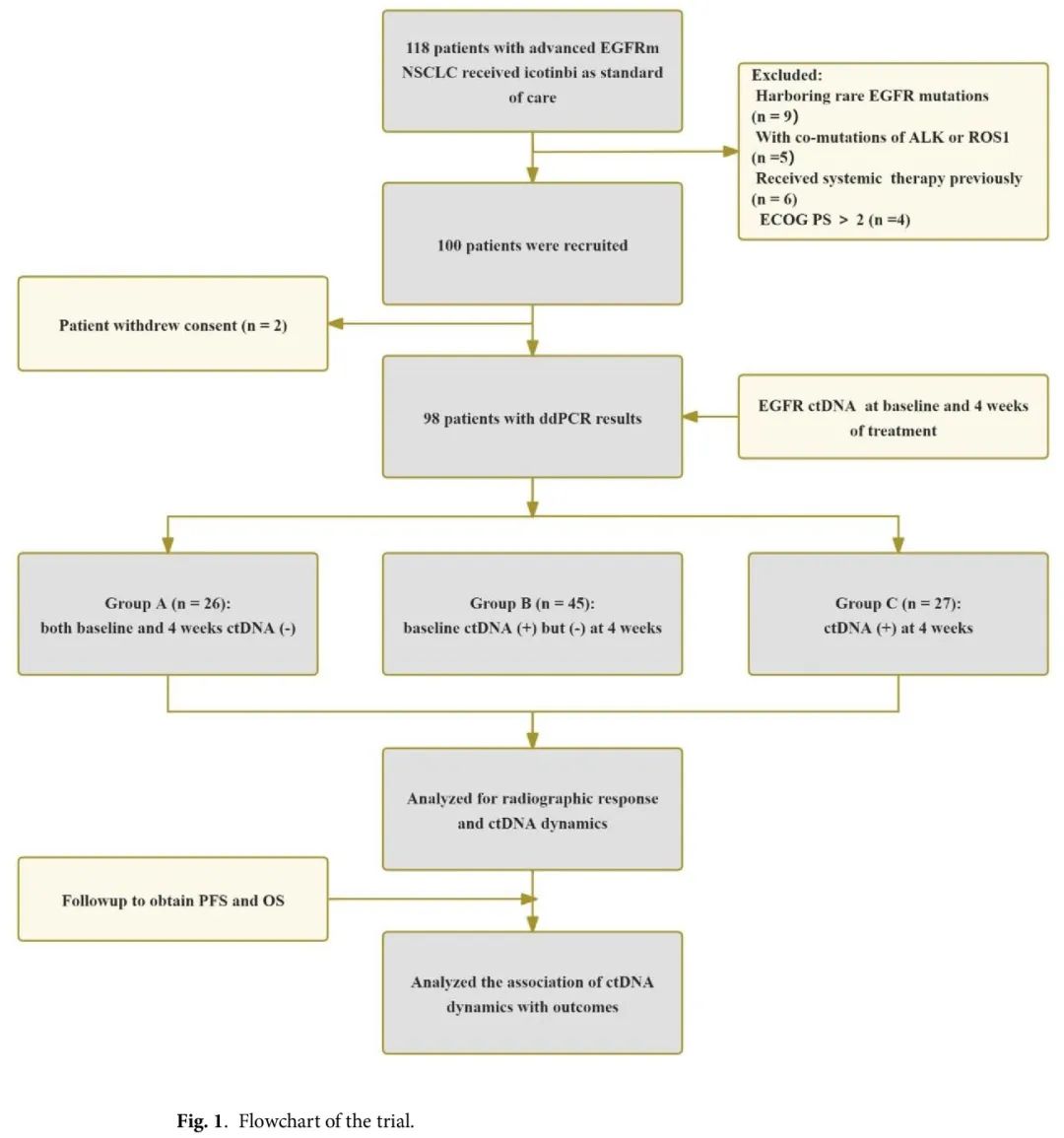
图1
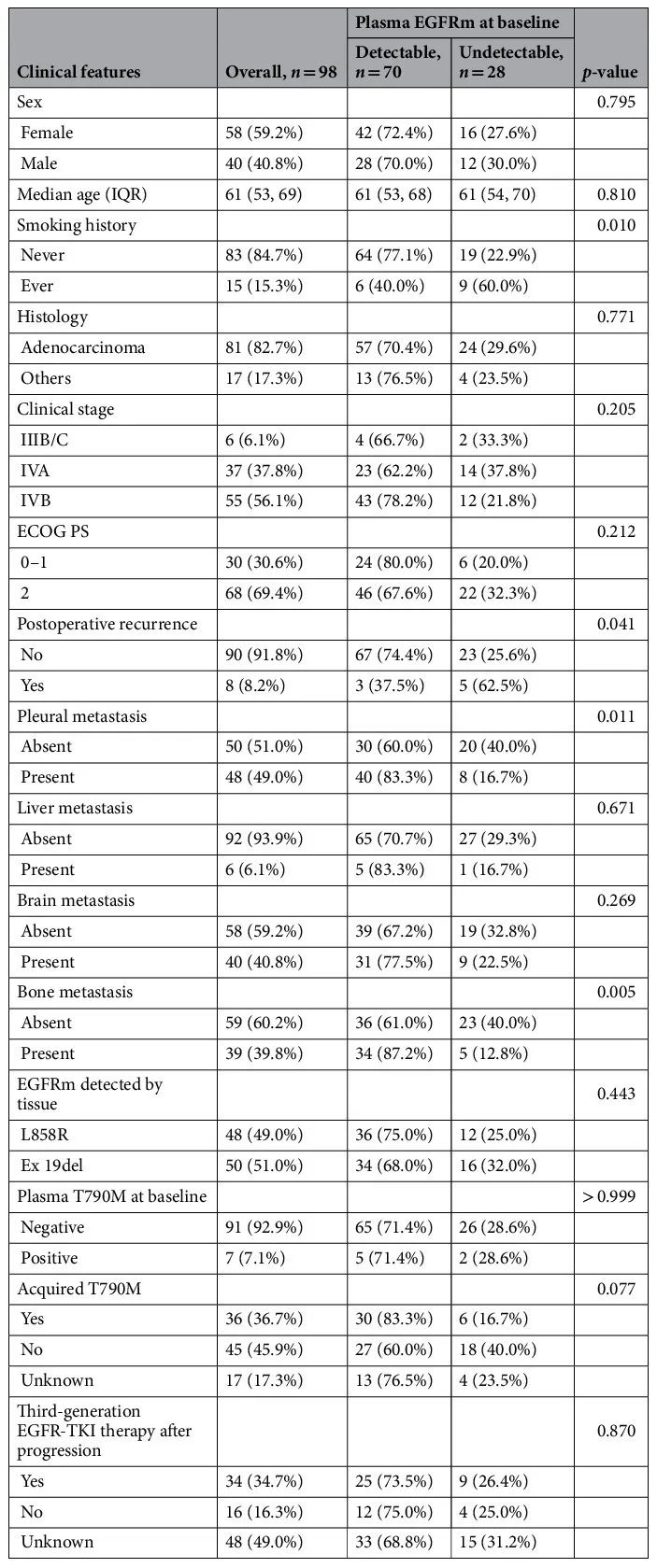

表1
临床结局
数据截止日期为 2023 年 1 月 2 日。中位随访 57.5(95% CI 49.2-65.8)个月后,78 例患者(79.6%)出现疾病进展,60 例患者(61.2%)死亡。没有患者达到完全缓解(CR),67 例患者部分缓解(PR),24 例疾病稳定(SD),7 例疾病进展(PD)。客观缓解率(ORR)为 68%(95% CI 58-77%),疾病控制率(DCR)为 93%(95% CI 85-97%)。中位 PFS 为 10.7 个月(95% CI 8.9-12.6),12 个月 PFS 率为 43.9%(95% CI 34.4-55.9%),24 个月 PFS 率为 9.6%(95% CI 4.6-20.0%)。此外,中位 OS 为 29.9 个月(95% CI 23.6-36.2 个月),1 年 OS 率为 76.2%(95% CI 67.8-85.7%),2 年 OS 率为 58.4%(95% CI 48.5-70.5%),3 年 OS 率为 40.1%(95% CI 30.1-53.3%)。
基线ctDNA阳性率和治疗后ctDNA清除率
在 98 例患者中,70 例(71.4%)基线检测到 EGFRm ctDNA,中位 VAF 为 4.1%(IQR 1.2-16.8)。从不吸烟者的基线 EGFRm ctDNA 阳性率为 77.1%(64/83),而曾经吸烟者为 40.0%(6/15)(P = 0.010)(表 1)。胸膜或骨转移患者的 EGFRm ctDNA 阳性率高于无转移患者,非术后复发患者的阳性率高于术后复发患者(P 分别为 0.011,0.005 和 0.041)。不同临床分期或 EGFR 突变之间的基线 ctDNA 阳性率无显著差异(P 分别为 0.205 和 0.443)。Spearman 秩相关系数分析显示患者基线 EGFRm ctDNA VAF 与靶病灶大小总和呈正相关(r = 0.238,P = 0.0183)。
埃克替尼给药 4 周后,45 例(45.9%)基线血浆 EGFRm 阳性的患者转阴,25 例(25.5%)基线血浆 EGFRm 阳性的患者仍保持阳性,26 例(26.5%)基线血浆 EGFRm 阴性的患者仍保持阴性,2 例(2.0%)基线血浆 EGFRm 阴性的患者转阳。
临床反应与血浆EGFRm ctDNA的相关性
基线检测到和未检测到 EGFRm ctDNA 的患者的 ORR 无显著差异(66 vs. 44%,P = 0.372)。基线检测到和未检测到 EGFRm ctDNA 的患者的缓解持续时间(DOR)也没有差异(91 vs. 96%,P = 0.385)。在 70 例基线血浆检测到 EGFRm 的患者中,基线血浆 EGFRm VAF 分布在不同最佳总体疗效的患者中无显著差异(分别为 4.4、3.8 和 13.1%;P = 0.495)。
我们将患者分为三组:A 组,ctDNA 在基线和治疗 4 周时均未检测到(n = 26);B 组,ctDNA 在基线检测到但在 4 周时未检测到(n = 45)(清除);C 组,4 周时检测到 ctDNA(n = 27)(未清除)。A 组和 B 组患者的最佳总体疗效、疾病控制和客观缓解率没有差异(P = 0.787、> 0.999 和 0.501)。B 组患者的 ORR 高于 C 组患者(80.0 vs. 44.4%,P = 0.002),但 DOR 没有更高(95.6 vs. 85.2%,P = 0.188)。
无进展生存期与血浆EGFRm ctDNA的相关性
基线血浆检测到 EGFRm 的患者的中位 PFS 为 10.1 个月(95% CI 7.4-12.8 个月),未检测到 EGFRm 的患者为 11.4 个月(95% CI 7.4-12.8 个月)(P = 0.384)(图 2A)。在达到 PR 的患者中,基线检测到和未检测到 EGFRm 的患者的中位 PFS 无显著差异(12.3 vs. 11.4 个月,P = 0.985)。在 SD 或 PD 患者中观察到类似的结果(P = 0.240 和 0.432)。
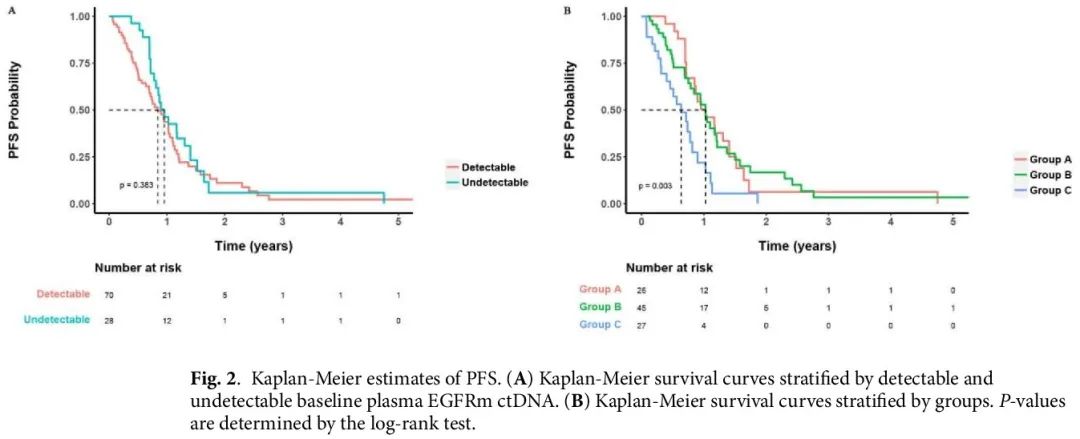
图2
生存分析显示,A 组、B 组和 C 组的中位 PFS 分别为 12.3 个月(95% CI 10.2-18.2 个月)、12.3 个月(95% CI 9.4-16.4 个月)和 7.6 个月(95% CI 4.8-12.3 个月)(P = 0.003)(图 2B)。A 组和 B 组的 PFS 没有显著差异(HR 1.01 [95% CI 0.59–1.74],P = 0.958)。A 组或 B 组的 PFS 显著优于 C 组(HR 0.42 [95% CI 0.22–0.78],P = 0.006;HR 0.43 [95% CI 0.25–0.76],P = 0.004)。在单变量分析中,组别(A/B 组 vs. C 组)以及胸膜转移或骨转移和最佳总体疗效(PR vs. PD)是 PFS 的预后因素(表2)。多变量分析显示,最佳总体疗效(PR vs. PD)、EGFR 突变(ex19del vs. L858R)、年龄(< 61 vs. ≥ 61)和组别(A/B 组 vs. C 组)是 PFS 的独立预后因素。图 3 展示了PFS HR 森林图。
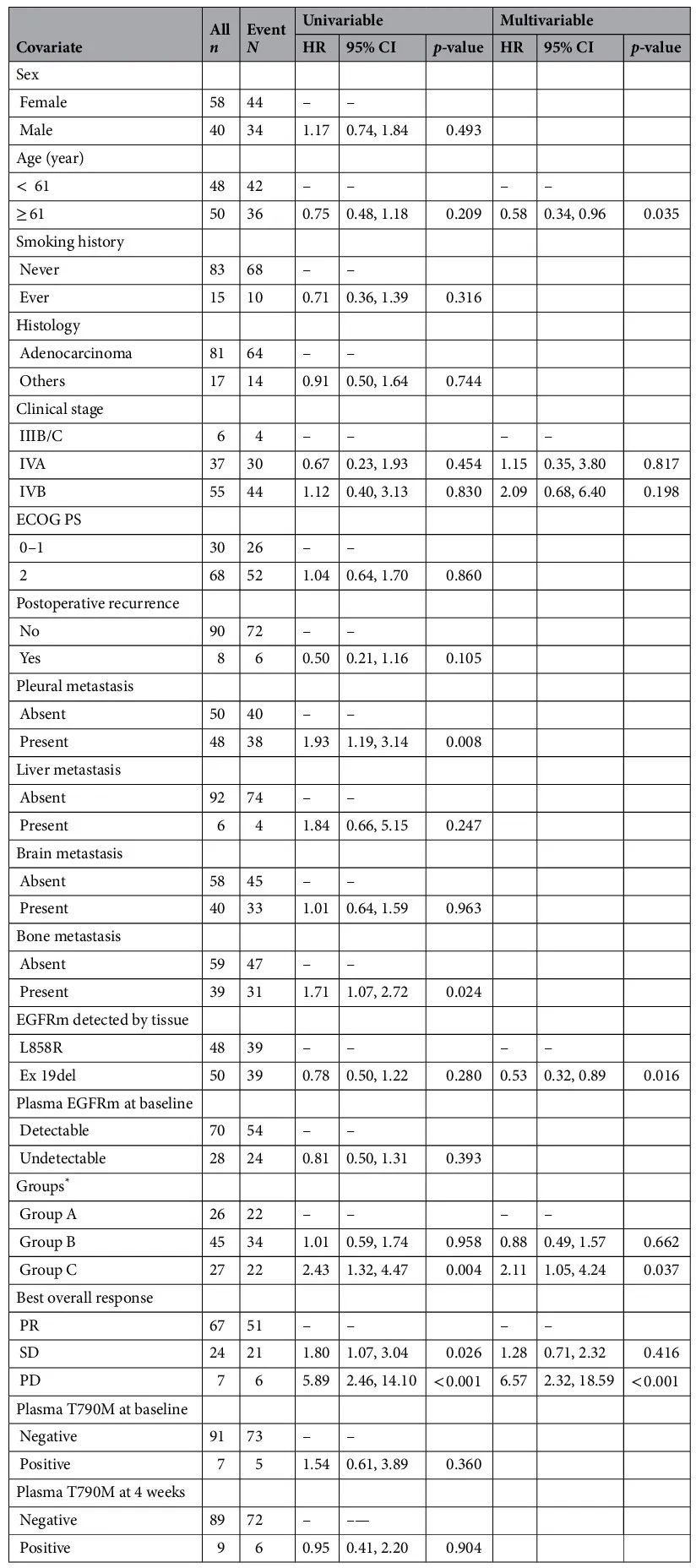

表2
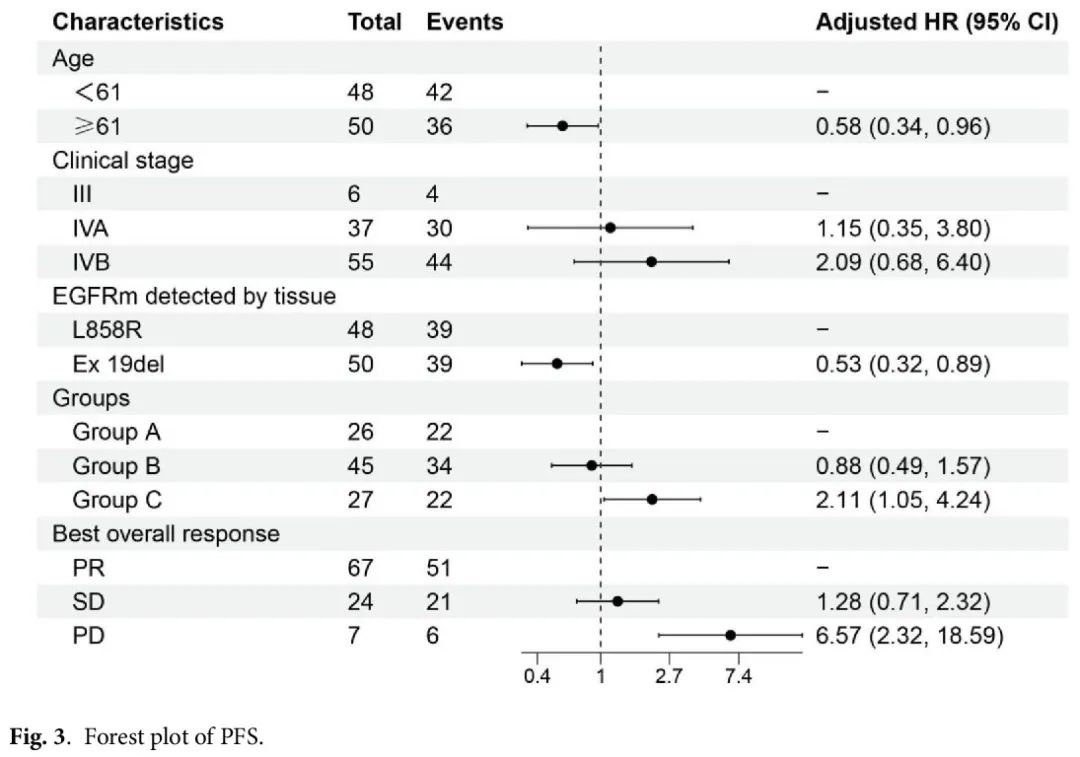
图3
总生存期与血浆EGFRm ctDNA的相关性
Kaplan-Meier 分析显示,基线血浆未检测到 EGFRm 的患者的中位 OS 为 34.0 个月(95% CI 26.3-41.7 个月),基线血浆检测到 EGFRm 的患者为 28.5 个月(95% CI 19.5-37.6 个月)(图 4A)。然而,基线检测到和未检测到 EGFRm 的亚组之间的生存结局差异不显著(风险比(HR)0.85;95% CI 0.48-1.49;P = 0.573)。在达到 PR 的患者中,基线检测到和未检测到 EGFRm 的亚组之间的中位 OS 没有差异(37.0 vs. 34.0 个月,P = 0.550)。SD 或 PD 患者获得相似的结果(P = 0.221 和 0.247)。
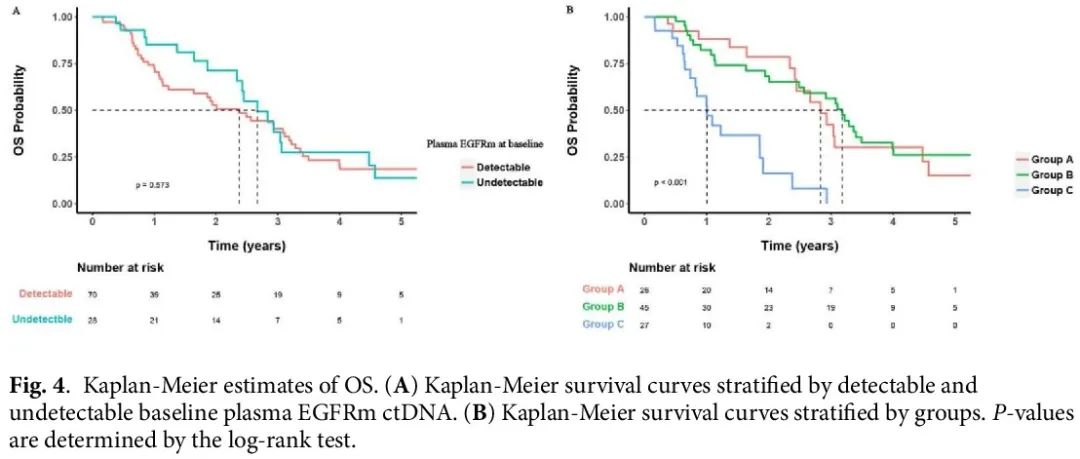
图4
A 组和 B 组的总生存期没有差异(HR 0.87 [95% CI 0.46–1.65],P = 0.664)。A 组或 B 组患者的生存期比 C 组长(34.0 个月 [95% CI 29.1-NA 个月],38.2 个月 [95% CI 29.9-47.9 个月] vs. 12.1 个月 [95% CI 9.9-28.5 个月] P < 0.001)(图 4B)。基于组别的 OS Kaplan-Meier 曲线如图 4B 所示。单变量分析显示,组别(A/B 组 vs. C)、肝转移、骨转移、EGFR 突变(ex19del vs. L858R)和最佳总体疗效(PR vs. PD)是 OS 的显著预测因子(表3)。多变量分析显示,组别(A/B 组 vs. C 组)、EGFR 突变(ex19del vs. L858R)和最佳总体疗效(PR vs. PD)仍然是预测 OS 较好的独立预后因素。肝转移、骨转移和未知获得性 T790M 状态是预测 OS 较差的独立因素(表 3)。图 5 展示了OS HR 森林图。
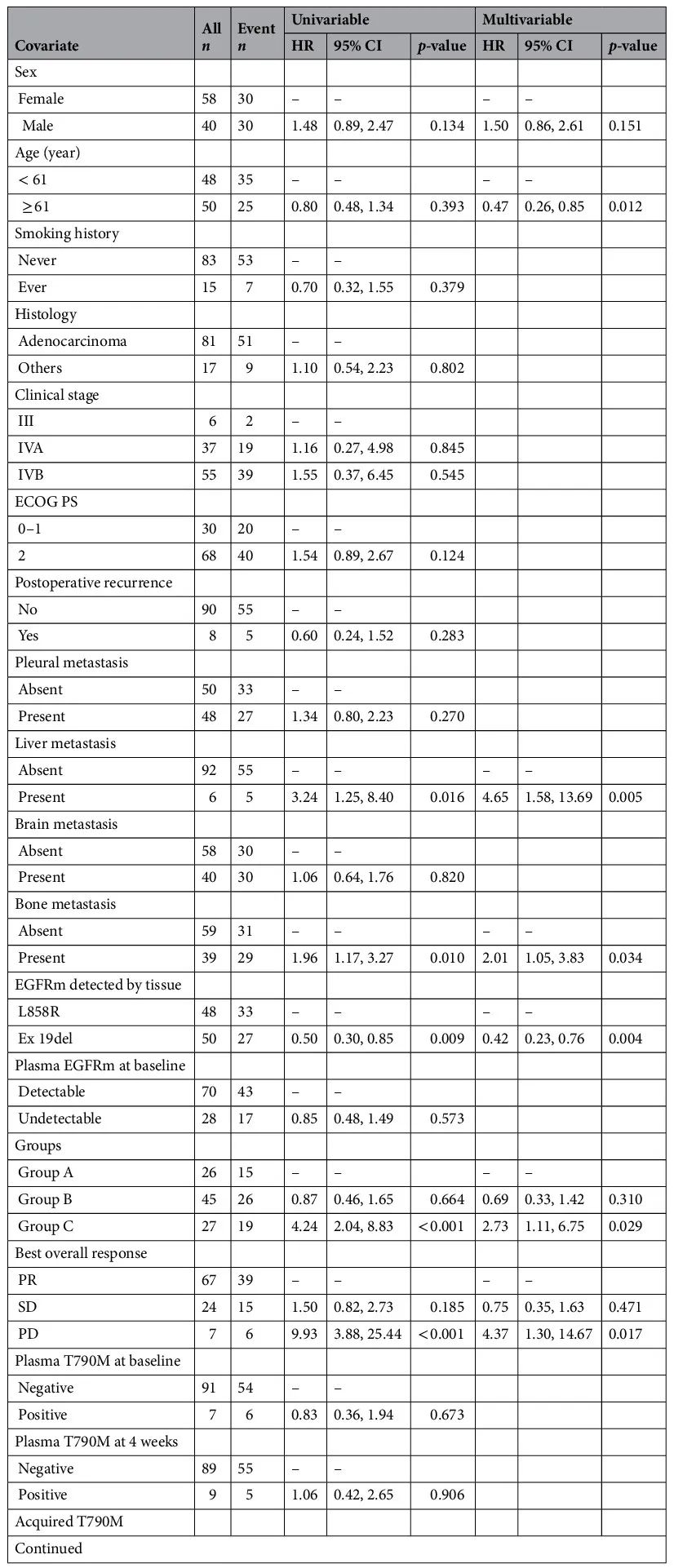
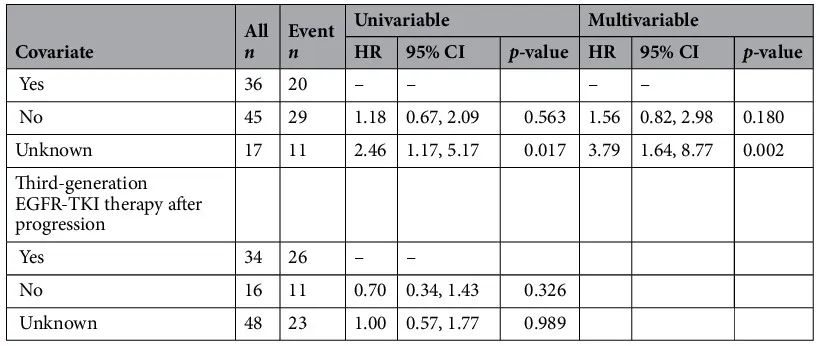

表3
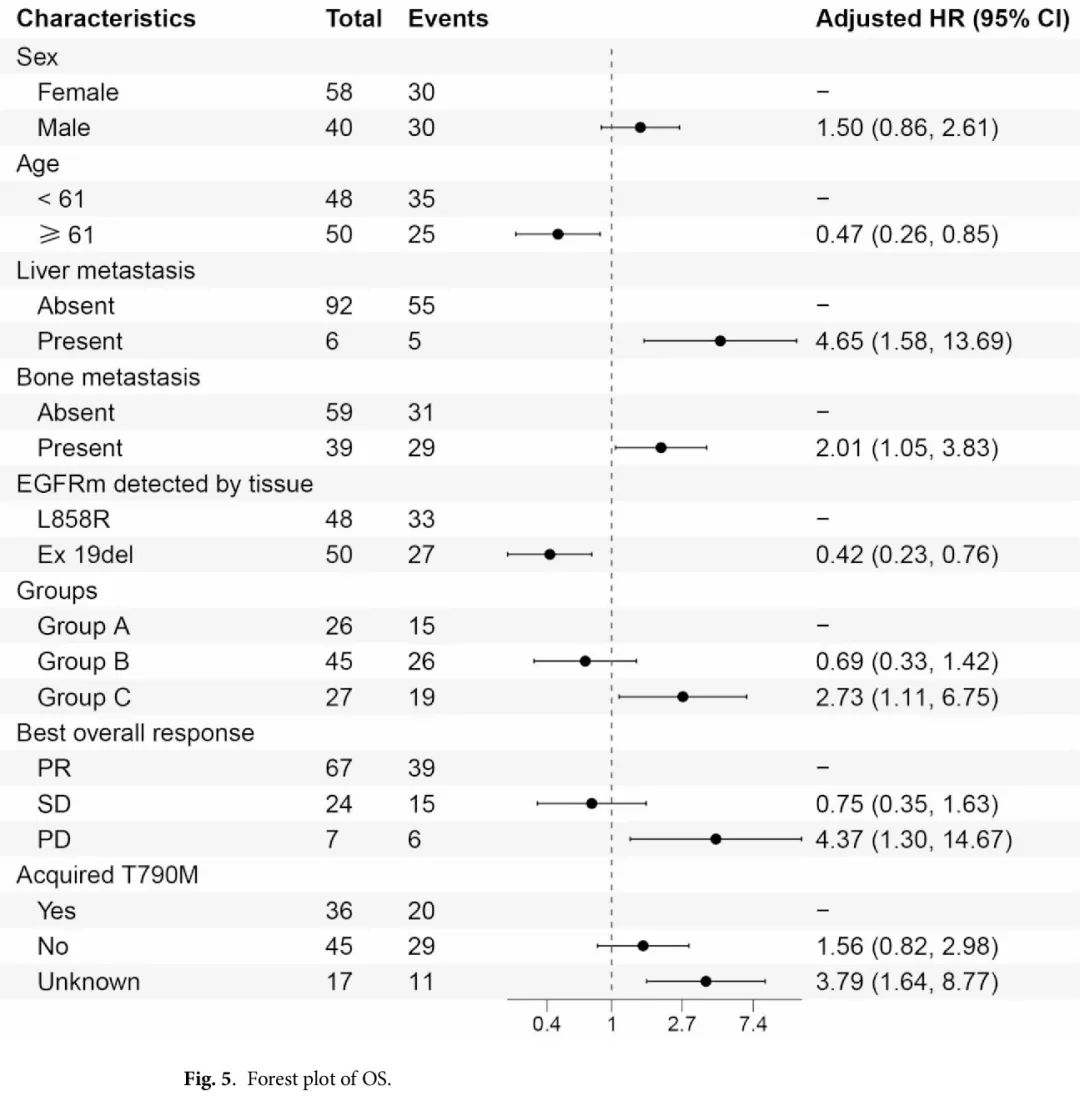
图5
讨 论
需要进一步的研究来理解 EGFRm ctDNA 监测的潜在意义。在这项前瞻性、多中心试验中,我们在真实世界接受埃克替尼治疗的 NSCLC 患者群体中探索了基线和治疗 4 周时血浆 EGFRm ctDNA 动力学与临床结果之间的关系。基线血浆 EGFRm 检出情况、客观缓解、疾病控制或最佳总体疗效之间没有显著相关性。生存分析显示,基线血浆检测到 EGFRm ctDNA 不会导致 PFS 或 OS 较短。值得注意的是,基线血浆检测到 EGFRm 但在治疗 4 周后清除的患者(B 组)的 PFS 和 OS 与基线和 4 周时均未检测到 EGFRm 的患者(A 组)相似。这两组的 PFS 和 OS 长于 4 周时检测到 EGFRm 的患者(C 组)。4 周血浆检测到 EGFRm 是 PFS 和 OS 较差的独立预测因子。连续血浆 EGFRm ctDNA 检测可能有助于预测接受埃克替尼治疗的晚期 EGFRm 患者的临床结局。
既往研究主要比较了基线时检测到和未检测到 EGFR ctDNA 的患者,或治疗后 ctDNA 清除组和未清除组的 PFS 和 OS 差异。WJOG8114LTR研究是一项前瞻性研究,纳入了 57 例接受阿法替尼治疗的 EGFRm NSCLC 患者。结果显示,4 周内 ctDNA 清除患者的 PFS 长于未清除患者。Gray 等人分析了来自 AURA3 和 FLAURA 试验的数据,评估血浆 EGFRm 的早期清除(3/6 周)作为晚期 NSCLC 奥希替尼治疗结局的预测标志物的潜力,获得了类似的结果。少数研究比较了基线检测到 ctDNA 但治疗后实现早期 ctDNA 清除的患者与基线未检测到 ctDNA 的患者之间的临床结局。本研究探索了基线和治疗 4 周时血浆 EGFRm ctDNA 均阴性的患者、基线时 EGFRm ctDNA 阳性但治疗后阴性的患者以及治疗后 EGFRm ctDNA 未清除的患者之间的临床结局的差异。有趣的是,基线 EGFRm 阳性但治疗后清除的患者的临床结局与基线和治疗 4 周时 EGFRm ctDNA 均阴性的患者相似,与未实现 ctDNA 清除的患者相比,PFS 和 OS 更长。这些结果表明,实现早期 ctDNA 清除的患者可能会从 EGFR-TKI 治疗中取得更多临床获益。
在调整临床因素后,治疗 4 周时检测到 ctDNA 仍然是 PFS 和 OS 的不良预后因素。这部分患者可能是早期改用第三代抑制剂或联合治疗的最佳候选者。需要在未来的临床研究中确认。
埃克替尼是某些国家和地区(尤其是中国)广泛使用的 EGFR-TKI。然而,关于晚期 NSCLC 患者 ctDNA 动态变化的试验水平的研究很少。大多数研究集中在使用血浆 EGFR ctDNA 检测来指导埃克替尼治疗。不同的 EGFR-TKI 可能具有细微的药代动力学差异,这可能会影响 ctDNA 清除的动力学。本研究是一项前瞻性、多中心、生物标志物导向的观察试验,评估 EGFRm 晚期 NSCLC 患者中血浆 EGFRm ctDNA 动态变化对埃克替尼治疗的预测价值。ctDNA 的 4 周时间点与常规临床随访和影像学评估一致,便于在实际临床实践中实施。我们认为本研究结果为接受埃克替尼治疗的患者的个体化检测提供了新的视角和潜在的方法。
大多数患者(71.4%)在埃克替尼治疗开始前血浆 EGFRm ctDNA 阳性。cfDNA 的检出可能受许多因素的影响,例如年龄或吸烟状况。一般来说,年长患者的 cfDNA 阳性率高于年轻患者。在肿瘤患者中,ctDNA 的浓度可能因癌症类型、疾病分期(尤其是肿瘤大小)、基因型以及局部或远处转移的存在而异。我们的研究结果表明,吸烟史、非术后复发、基线胸膜转移和骨转移的存在与 EGFRm ctDNA 阳性率相关,并且 EGFRm ctDNA VAF 与肿瘤大小存在较小但具有统计学意义的相关性。这些数据与既往研究一致。
血浆 ctDNA 浓度与肿瘤负荷和转移负荷相关,提示它是预后生物标志物。血浆 EGFRm 的早期动态变化或可预测 NSCLC 患者 EGFR-TKI 治疗的临床结局。在 AURA 研究中,奥希替尼治疗 6 周后血浆检测不到 EGFRm 的患者具有更好的 ORR 和中位 PFS。血浆 EGFRm 分析最早在奥希替尼治疗后 3 周也可以预测结果。本研究发现,治疗 4 周后血浆检测到 EGFRm ctDNA 的患者比未检测到 EGFRm ctDNA 的患者预后更差。监测血浆 ctDNA 随时间的变化可能有助于了解 EGFRm NSCLC 患者的治疗效果。
本研究的优势在于前瞻性、多中心、生物标志物导向试验,定义了在基线时和之后在治疗期间明确定义的时间点收集血浆样本。本研究存在一些局限性。首先,由于预算限制,当患者在 TKI 治疗期间出现进展时,我们的研究没有纳入血浆 EGFRm ctDNA 检测。其次,ctDNA 检测仅评估 EGFRm。未研究共突变,如 TP53 或其他突变,即使这些亚克隆突变是已知的 NSCLC 预后因素。鉴于本研究的观察性质,根据 ctDNA 状态的临床治疗策略数据不可及,需要进一步探索。
总之,本研究结果表明,基线血浆 EGFRm ctDNA 阳性但埃克替尼治疗 4 周时转阴的患者的预后与基线和 4 周时血浆 EGFRm 均阴性的患者相似。治疗 4 周时血浆 EGFRm 阳性是 PFS 和 OS 较差的独立危险因素。这些生物标志物可以指导日常临床实践中的治疗决策和随访方法。
参考文献:
Hong Y, Zhuang W, Lai J, Xu H, He Y, Lin J, Shi Q, Chen S, Huang Z, Chen S, Lu D, Lin G, Huang Y. Plasma EGFR mutation ctDNA dynamics in patients with advanced EGFR-mutated NSCLC treated with Icotinib: phase 2 multicenter trial result. Sci Rep. 2024 Oct 4;14(1):23115. doi: 10.1038/s41598-024-73749-2. PMID: 39367090; PMCID: PMC11452669.



