STTT | 新突破:术前信迪利单抗、安罗替尼和化疗,术后辅助信迪利单抗治疗可切除非小细胞肺癌:疗效显著,安全性良好
时间:2024-10-31 17:01:49 热度:37.1℃ 作者:网络
肺癌是全球癌症相关死亡的主要原因,中国肺癌死亡率占全球的40%,其中,非小细胞肺癌(NSCLC)是最常见的类型,约20-25%的患者在确诊时处于可切除阶段,尽管手术是主要的治疗方法,但术后复发率仍然较高,因此,术前新辅助化疗成为重要的治疗策略,但效果有限,近年来,免疫治疗和抗血管生成治疗在NSCLC的治疗中展现出巨大潜力,免疫检查点抑制剂(如PD-1抑制剂)和抗血管生成药物(如安罗替尼)能够分别通过激活免疫系统和抑制肿瘤血管生成来发挥抗肿瘤作用,多项研究表明,术前新辅助免疫治疗和抗血管生成治疗联合化疗能够显著提高患者的病理完全缓解(pCR)率,降低复发风险,改善生存预后,改研究旨在评估术前新辅助信迪利单抗联合安罗替尼和化疗,术后辅助信迪利单抗治疗可切除NSCLC的疗效和安全性,并探索肿瘤微环境变化作为预测治疗效果的潜在生物标志物。

方法
研究是一项开放标签、单臂、II期临床试验,纳入了可切除IIA-IIIB期NSCLC患者,患者接受前新辅助信迪利单抗联合安罗替尼和化疗,术后辅助信迪利单抗治疗。术前新辅助治疗:安罗替尼:10mg,每日一次,口服,第1-14天;信迪利单抗:200mg,静脉注射,第1天化疗:含铂双药方案,每3周一次,共3个周期;手术:术后4-6周内进行。术后辅助治疗:信迪利单抗:200mg,静脉注射,每3周一次,持续1年。主要终点为病理完全缓解(pCR)次要终点为主要病理缓解(MPR)事件、无进展生存期(EFS)。生物标志物为采用多重免疫组化技术检测肿瘤组织中相关细胞标记物的表达,评估血管正常化程度和免疫细胞浸润情况,包括VEGF+ 细胞、CD31+/NG2+ 细胞、周围血管 CD4+ T 细胞、CD39+CD8+ T 细胞、M1 巨噬细胞。
研究结果
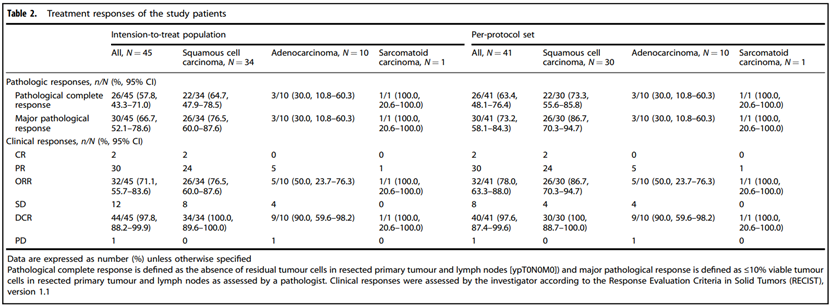
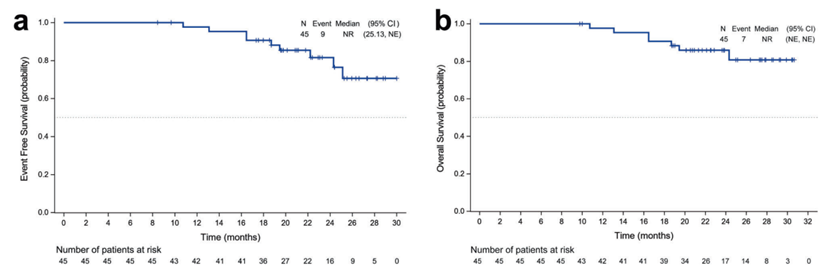
ITT人群:pCR率:57.8%;MPR率:66.7%;客观缓解率(ORR):71.1%;疾病控制率(DCR):97.8%;1年无事件生存率(EFS):81.5%。
PP人群:pCR率:63.4%;MPR率:73.2%;87.8%的患者肿瘤降期;1年无事件生存率(EFS):81.5%。
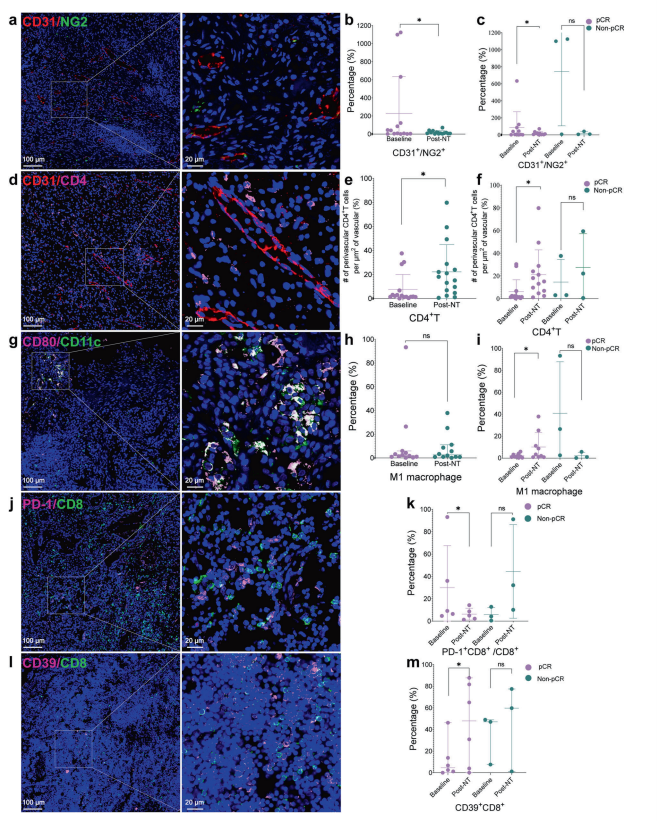
肿瘤微环境变化:与非pCR组相比,pCR组患者的VEGF+细胞、CD4+Foxp3+ Treg 细胞数量显著减少,周围血管 CD4+ T 细胞、CD39+CD8+ T 细胞和M1巨噬细胞数量显著增加。
安全性
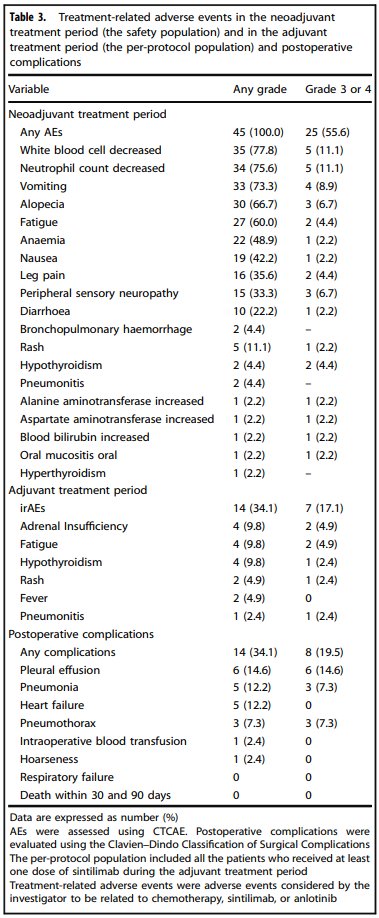
新辅助治疗期间,100%的患者出现TRAEs,其中55.6%的患者出现3/4级TRAEs,15.6%的患者出现irAEs。辅助治疗期间,34.1%的患者出现irAEs,其中17.1%的患者出现3级irAEs,34.1%的患者出现术后并发症,其中19.5%的患者出现3级并发症。
结论
研究结果表明,术前新辅助信迪利单抗联合安罗替尼和化疗,术后辅助信迪利单抗治疗可切除NSCLC具有良好的疗效和安全性,能够显著提高pCR率和肿瘤降期率,并改变肿瘤微环境,为可切除NSCLC患者提供了一种新的治疗选择。
原始出处
Duan, H., Shao, C., Luo, Z. et al. Perioperative sintilimab and neoadjuvant anlotinib plus chemotherapy for resectable non-small-cell lung cancer: a multicentre, open-label, single-arm, phase 2 trial (TD-NeoFOUR trial). Sig Transduct Target Ther 9, 296 (2024). https://doi.org/10.1038/s41392-024-01992-0.


