读书报告丨ARDS患者呼吸力学的划分及其与预后的关系:一项多中心临床研究
时间:2024-08-15 20:00:37 热度:37.1℃ 作者:网络

一、概念
气道驱动压(driving pressure,△P)是整个呼吸系统扩张的直接动力,△P=Pplat-PEEP(仅适用无自主呼吸时),与呼吸系统弹性阻力(respiratory system elastic resistance,ERS)大小相等,方向相反,ERS由胸壁弹性阻力(Ecw)和肺弹性阻力(EL)组成,气道驱动压中仅对抗肺的弹性阻力扩张肺组织的驱动压称为跨肺驱动压(lung drving pressure,△PL),△PL=△P×EL/ERS,跨肺驱动压=吸气末跨肺压-呼气末跨肺压,跨肺压=肺内压-胸腔压,胸腔压常用易于测定的食道压(esophageal pressure,Pes)来替代,所以△pl=(Pplat -吸气末Pes)-(PEEP-呼气末Pes)。当机械通气患者存在自主呼吸时,驱动压将在呼吸机驱动压的基础上增加呼吸肌带来的驱动压。
2015年Amato等在ARDS患者机械通气领域的研究成果再次引起重大轰动,该研究显示一系列呼吸参数设置对患者生存率影响的核心是驱动压的改变,只有伴随驱动压降低的小潮气量和PEEP的增加才能起到肺保护作用,只有伴随驱动压增高的平台压增高才会导致肺损伤。
二、研究背景
机械通气虽可挽救生命,但可引起呼吸机相关性肺损伤(VILI)。在急性呼吸窘迫综合征(ARDS)中,与预后相关的生理参数可能有助于确定机械通气的目标。
Amato等提出气道驱动压(DPaw)在生理上比VT/PBW更适合用于限制VILI。他们的回顾性分析显示,与VT/PBW或Pplat相比,DPaw与结局的相关性更好。因此,DPaw是一个重要的监测参数,是肺保护性通气策略的潜在靶点。
VILI与呼吸系统顺应性有关,因此理论上,通过消除胸壁对DPaw的影响,跨肺驱动压(DPL)或与之相关的潮气量是比DPaw更好的评估潜在VILI的可能。其他与跨肺压(PL)相关的计算指标可能代表了限制VILI的生理学意义。
我们的最终目标是找出可以作为限制VILI风险的通气目标的最重要的变量。然而,由于没有直接、可靠的方法(包括生物标志物)来评估床旁VILI,我们决定将力学与死亡率之间的关系作为一种间接的方法来看待。
其假设主要有两个:主要假设是跨肺驱动压(DPL)是比气道驱动压(DPaw)更好的结局预测指标。第二个假设是氧合拉伸指数-PaO2/(FiO2×DPaw),可以增强对60天结局的预测能力。文章中计算了氧合拉伸指数:PaO2/(PaO2×DPaw ),为氧合和力学的综合指数。使用公式计算机械功率:0.098×RR× [VT2×[0.5×Ers+RR×(1+I:E)/(60×I:E)×Rrs]+ VT×PEEP]。其中I:E比,通过计算吸气时间(Ti)和呼气时间(Te)进行估计。通过VT/Flow + 0.3计算Ti,其中VT以升为单位,流量以L/sec为单位,0.3表示吸气末暂停时间0.3秒。通过总呼吸时间减去Ti计算Te,其中总呼吸时间等于RR/60。
三、目的
这项研究旨在探讨PL,包括DPL、弹性衍生跨肺压和呼气末跨肺压,是否比DPaw更能预测与60天预后相关联。
四、方法
对ARDS患者进行前瞻性、观察性、多中心研究。在机械通气早期,6 kg/ml潮气量条件下测量呼吸力学相关参数。通过观测者操作特性(ROC)曲线,比较这些参数对60天死亡率的预测能力,并通过未校正和校正的Cox回归评估了其与60天病死率率的相关性。最后,对每个参数进行二分类,并比较Kaplan-Meier生存曲线。
五、纳排标准
纳入标准:①年龄>18岁;②根据柏林定义的 ARDS;③接受镇静、辅助/控制通气;④插管第1周内。
排除标准:①已知食管病变、活动性上消化道出血或其他胃管插入禁忌证;② 严重的血流动力学不稳定(前6小时血管升压药增加>30%,或去甲肾上腺素>0.5 mcg/(kg·min)。
六、研究流程
本研究共有385例患者参与,其中8例患者因在俯卧位或ECMO下进行测量而被排除在分析之外,最终分析的样本量为377例患者。测量是在插管后的2天内进行的,测量时的临床PEEP中位数为12 cmH2O。在302例患者中(子集A:样本总数的80%),测量了食道压(Pes),计算得出跨肺压。测量方法包括使用Pes测量导管和Lanteris修改的Baydurs阻塞测试来验证导管的位置。对Pes波形进行了中央检查,并计算了氧合伸展指数和呼吸功。
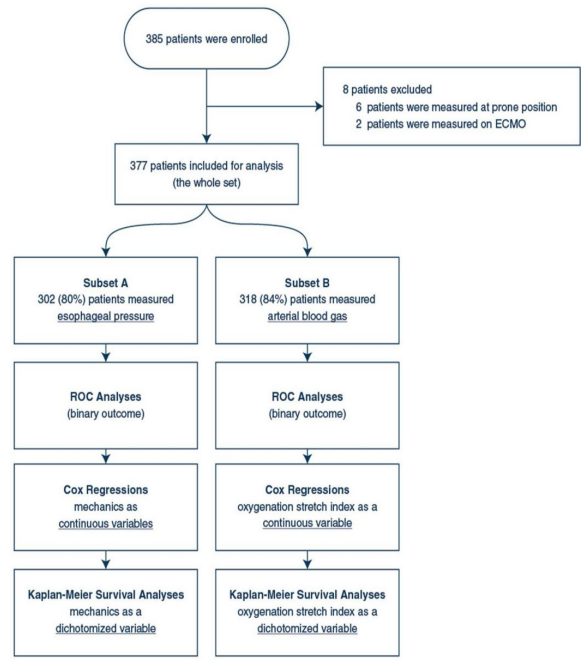
图1 研究流程图
七、研究结果
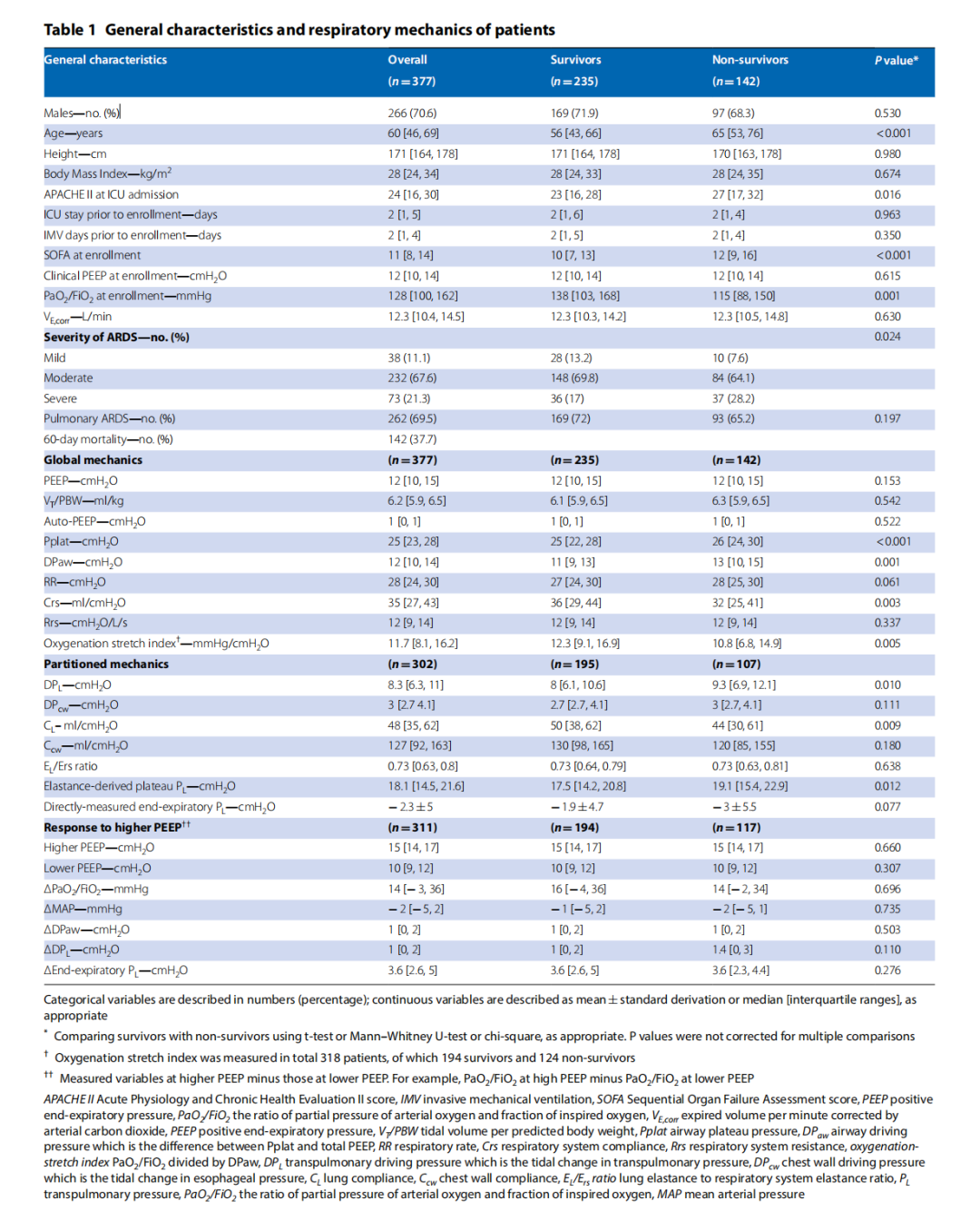
患者的一般特征见表1。第60天的死亡率为37.7%。在插管后2天(IQR 1~4)天内进行测量,平均临床呼气末正压为12(IQR 10~14)cmH2O。在单因素分析中,非幸存者的年龄更高,ICU入院时拥有较高的APACHE II,较高的SOFA和登记时的较低的PaO2/FiO2。呼吸力学报告见表1。单因素分析显示,非幸存者有较高的Pplat、DPaw、DPL、弹性衍生跨肺压、呼吸频率和较低的氧合拉伸指数。在幸存者和非幸存者中,我们在氧合、血压和DPaw对较高的呼气末正压的反应方面没有发现任何统计学差异。
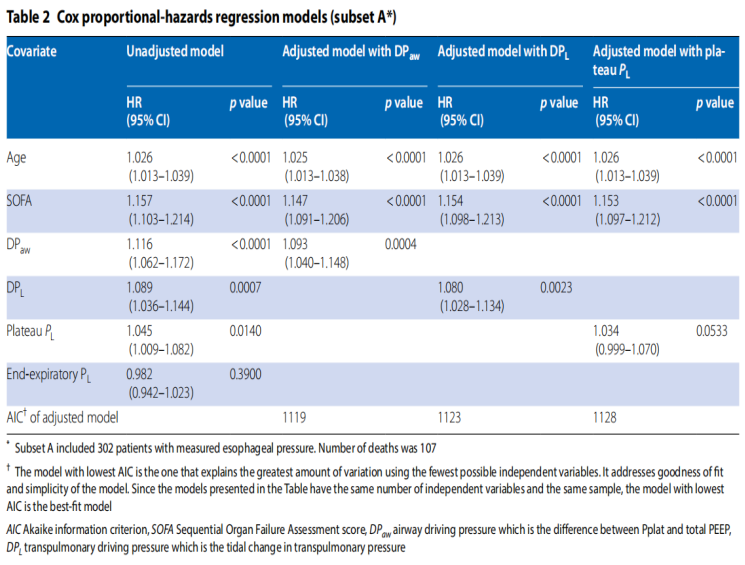
在校正年龄和SOFA评估后,DPaw、DPL和氧合拉伸指数被证实与60天病死率相关,而弹性衍生跨肺压与之不相关。DPaw和DPL在ROC分析中的表现相同(P=0.0835)。DPaw具有最佳拟合Cox回归模型。
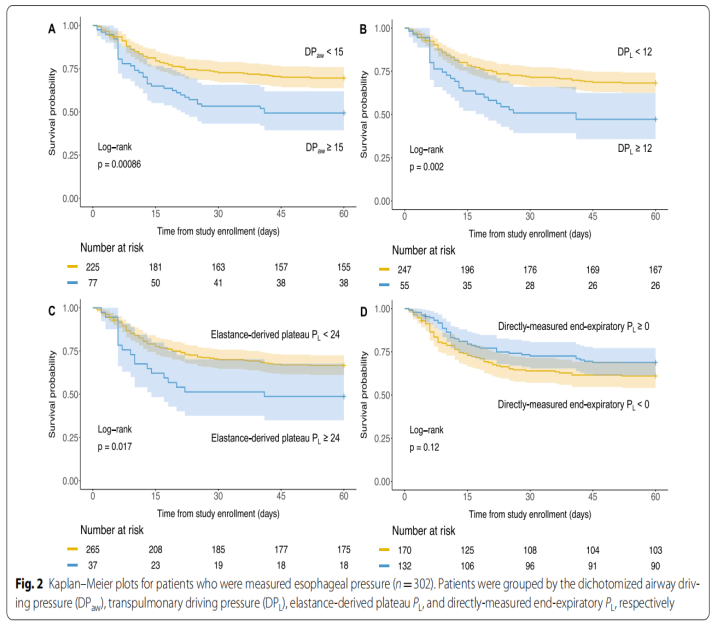
如下图:当将这些参数进行二分法分析时,DPaw≥15 cmH2O、DPL≥12 cmH2O、弹性衍生跨肺压≥24 cmH2O和氧合伸展指数<10的患者预后较差。在肥胖患者中,直接测量的呼气末PL≥0与更好的预后相关。
如下图:我们对进行食管压测量的患者 (n=302)进行了事后分析,发现直接测量的呼气末跨肺压与肥胖之间存在相互作用(身体质量指数≥30 kg/m2)关于调整后的Cox回归模型中的60天死亡率(交互项的HR:0.904,95%CI 0.832~0.982,P=0.0175)。DPaw、DPL、弹性衍生跨肺压与肥胖没有显著的相互作用。呼气末跨肺压阳性(≥0)的肥胖患者的生存概率高于呼气末跨肺压阴性的患者(图3,Log-Rank检验:0.0042)。
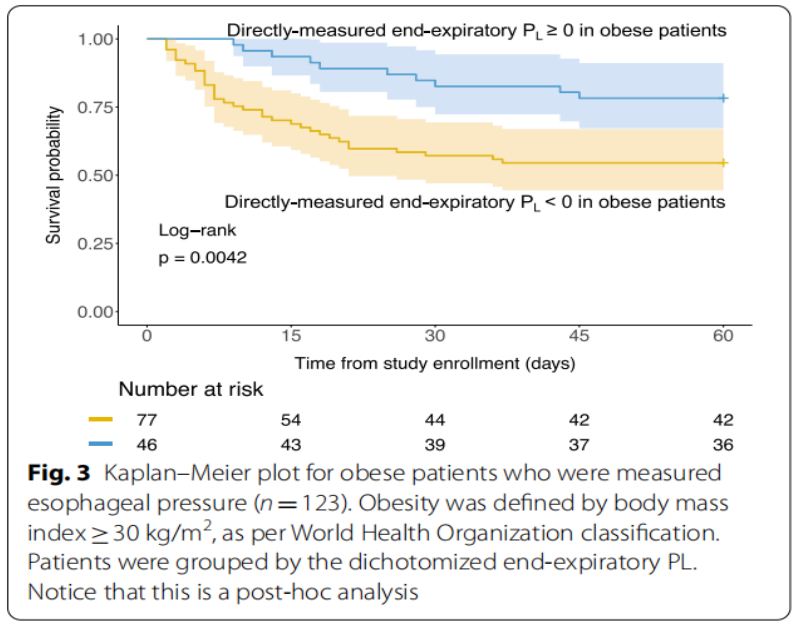
肥胖患者食管测压(n=123)的Kaplan-Meier图。根据世界卫生组织分类标准,肥胖定义为体重指数≥30 kg/m2。根据呼气末PL二分法对患者进行分组。这是一个事后分析。
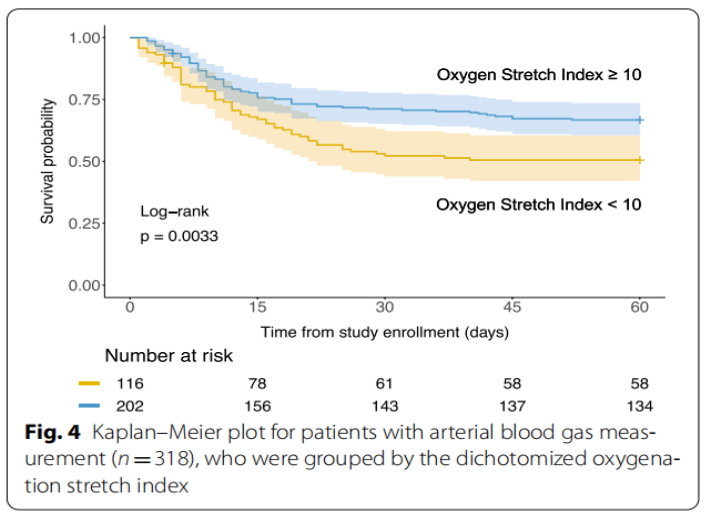
如下图:我们获得了318例患者的动脉血气(子集 B:84%的队列)。氧合拉伸指数在预测第60天死亡率(二元结果)方面没有显著高于DPaw(0.59 vs. 0.58,P=0.6483,见图4)。
八、研究讨论
研究发现,在ROC分析中,DPaw和DPL对第60天死亡率具有相似的预测能力。DPL与结果的相关性并不比DPaw强,这可能部分是因为胸壁驱动压与疾病严重程度和结果相关。
研究发现,肥胖患者具有更高的脂肪负荷,这可以通过胸壁的弹性回缩力来平衡。但是,当由于镇静或麻痹而导致呼吸肌肉松弛时,可能需要较高的外部PEEP来平衡这种负荷并维持呼气末肺容积。因此,保持肥胖患者的正呼气末压与更有利的结果相关联,这是研究支持限制肺和气道驱动压力以及维持正的呼气末正压对肥胖患者有益的原因之一。氧合拉伸指数[PaO2/(FiO2)×DPaw)]未能比DPaw拥有更强对60天结局的预测能力。
九、研究局限性
局限性表现在与之前旨在将力学与结果联系起来的研究一样,测量是在机械通气早期开始时的单个时间点进行的。由于在 ARDS过程中力学可能会发生变化,因此理想情况下,应该每天重复测量。然而,重复测量实际上具有挑战性,因为患者通常在插管几天后会产生自主呼吸努力,这将使测量结果的解释变得非常复杂。
几乎1/3的ARDS患者会发生完全气道关闭,这会影响弹性测量的准确性,从而影响弹性衍生跨肺压。患者的测量时间不均匀。我们有缺失的数据,处理这些丢失的数据可能很困难,最好的方法是有争议的。虽然多元插补是一种具有优势和劣势的替代选择,我们决定使用传统的方法——完整的案例分析。
有54例受2019年冠状病毒病 (COVID-19) 影响的患者登记在册,但由于感染控制预防措施,这些COVID-19患者均未测量食管压力。换句话说,我们的结果表明,在非COVID-19患者中发现跨肺压与结果的相关性不强于DPaw。
我们没有收集整个住院期间ARDS关键联合干预措施的数据,例如俯卧位、神经肌肉阻滞剂的剂量和持续时间、类固醇和ECMO。特别是,测量前的俯卧位可能会影响呼吸力学。
十、结 论
DPL和DPaw对ARDS患者60天结局预测能力相同。该研究印证了在肥胖患者中限制肺和气道驱动压以及维持呼气末正压通气的合理性。


