Nature:特洛伊木马策略:精准打击癌细胞的新希望
时间:2024-07-14 18:00:37 热度:37.1℃ 作者:网络
引言
癌症细胞的“饮水机”策略,一种利用肿瘤对蛋白质的自然摄取机制,催生了强效的抗癌疗法。这正是纽约大学格罗斯曼医学院(NYU Grossman School of Medicine)的达夫娜·巴尔-萨吉(Dafna Bar-Sagi)癌症生物学实验室的成员克雷格·拉米雷斯(Craig Ramirez)和安德鲁·豪瑟(Andrew Hauser)共同努力的成果。通过结合他们在细胞生物学和生物化学领域的专业知识,这两位研究人员揭示了癌症细胞利用巨胞饮作用(macropinocytosis)满足其代谢需求的机制。
巨胞饮作用是一种使肿瘤细胞能够“饮用”周围液体,从而吸收大量蛋白质和脂肪以支持其生长的机制。拉米雷斯和豪瑟特别关注RAS蛋白的突变,这种突变在大约三分之一的癌症中起关键作用。然而,他们在发表研究结果前需要完成一系列验证实验。拉米雷斯和豪瑟考虑了开发靶向巨胞饮作用途径的药物,以切断RAS突变肿瘤细胞的重要生存途径。然而,考虑到癌症对这种抑制策略可能产生抗药性,他们设想了一种更创新的策略——利用而非简单阻断肿瘤的营养摄取方式。
最终,他们在NYU蛋白质工程师小出祥平(Shohei Koide)的实验室中找到了一个有前景的载体,这是一种合成蛋白框架,称为单体(monobody)。实验显示,RAS突变癌细胞通过巨胞饮作用容易吸收这些单体。与纳米科学家纳森·比尔斯(Nathan Beals)合作,拉米雷斯和豪瑟设计了一种药物候选物,将小出的单体与一种源自海洋软体动物的防御肽毒素连接起来,形成一种蛋白质-药物结合物(protein–drug conjugate)。
自成立以来,Tezcat公司获得了数百万美元的研究资金,用于测试其主要药物候选物TZT-102在RAS突变的胰腺癌、肺癌和多发性骨髓瘤小鼠模型中的效果。实验结果显示,这种治疗方法在每种癌症类型中均表现出优异的效果,显著优于标准治疗选项。更重要的是,TZT-102表现出一系列有利的药理特性,表明它可能比其他药物递送平台更安全有效。
Tezcat公司的技术不仅适用于癌症治疗,还可能应用于神经退行性疾病、炎症状况和心血管疾病等受巨胞饮作用影响的疾病。此外,该平台还可以用于诊断领域,帮助实时可视化肿瘤或在影像扫描中监测疾病进展。(7月11日Nature “A Trojan horse for thirsty tumours”)
癌症细胞的生存和增长需要大量的营养,而巨胞饮作用(macropinocytosis)正是其获取这些营养的关键机制。通过巨胞饮作用,肿瘤细胞能够“饮用”周围的液体,从而吸收大量的蛋白质和脂肪,以满足其代谢需求。这一机制的研究为开发新型抗癌疗法提供了重要启示。纽约大学格罗斯曼医学院(NYU Grossman School of Medicine)的达夫娜·巴尔-萨吉(Dafna Bar-Sagi)癌症生物学实验室的研究人员克雷格·拉米雷斯(Craig Ramirez)和安德鲁·豪瑟(Andrew Hauser)通过结合他们在细胞生物学和生物化学领域的专业知识,揭示了这一机制,并以此为基础,开发出了一种创新的抗癌疗法。
巨胞饮作用的发现与研究
巨胞饮作用是一种细胞通过吞饮周围液体以摄取营养的过程。对于癌细胞而言,巨胞饮作用尤为重要,因为它们需要大量的营养来支持其快速增殖。拉米雷斯和豪瑟的研究聚焦于RAS蛋白的突变,这种突变在大约三分之一的癌症中起关键作用。他们发现,RAS突变的肿瘤细胞通过巨胞饮作用吸收大量的蛋白质和脂肪,以满足其生长需求。然而,在他们正式发表研究结果前,还需要完成一系列的验证实验。
为了找到更有效的抗癌方法,拉米雷斯和豪瑟与NYU蛋白质工程师小出祥平(Shohei Koide)合作,利用他发明的单体(monobody),这种合成蛋白框架可以被RAS突变的癌细胞通过巨胞饮作用吸收。这个发现为开发新型抗癌疗法提供了基础。
创新抗癌疗法的诞生
在工作之余,拉米雷斯和豪瑟常在纽约基普湾(Kips Bay)社区的Albion酒吧一边喝着精酿啤酒,一边讨论如何将他们的科学发现转化为实际治疗方法。他们考虑了开发靶向巨胞饮作用途径的药物,以切断RAS突变肿瘤细胞的重要生存途径。然而,考虑到癌症对这种抑制策略可能产生抗药性,他们设想了一种更创新的策略——利用而非简单阻断肿瘤的营养摄取方式。
拉米雷斯回忆说:“如果这些癌症细胞已经在为了生存和增长而吸收蛋白质,那么与其尝试切断信号,不如利用一种蛋白质载体并将毒素附着在上面,就像特洛伊木马一样。”
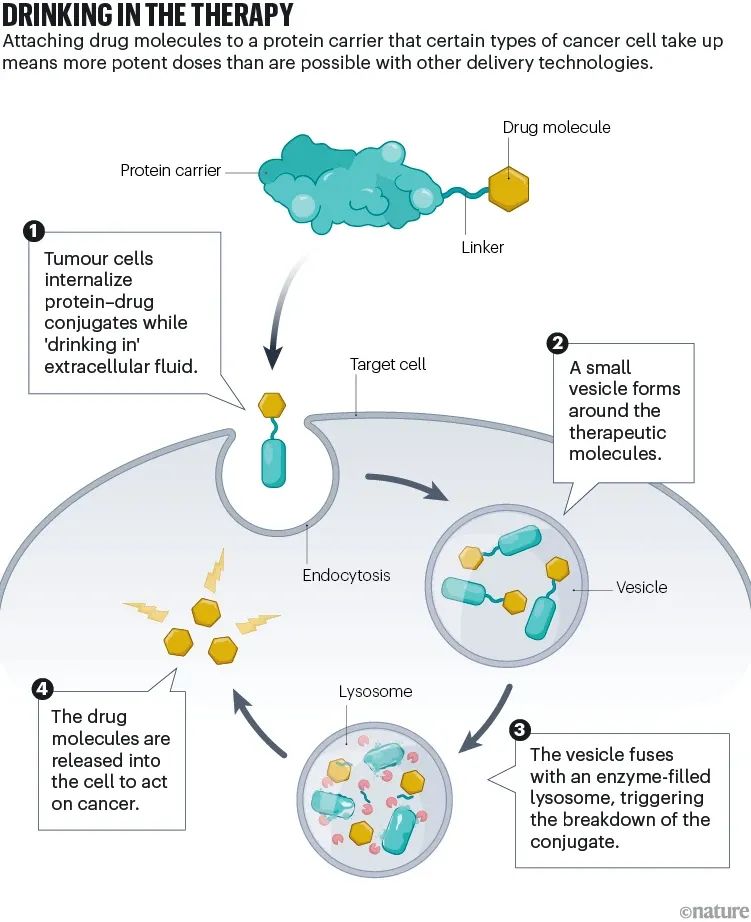
模式图(Credit: Nature)
TZT-102的开发与实验数据
在小出祥平的实验室中,研究人员找到了一种合适的载体单体(monobody),并与一种源自海洋软体动物的防御肽毒素结合,形成了蛋白质-药物结合物(protein–drug conjugate)。这种结合物被称为TZT-102。
自成立以来,Tezcat公司获得了数百万美元的研究资金,用于测试TZT-102在RAS突变的胰腺癌、肺癌和多发性骨髓瘤小鼠模型中的效果。实验结果显示,这种治疗方法在每种癌症类型中均表现出优异的效果,显著优于标准治疗选项。例如,在胰腺癌小鼠模型中,TZT-102治疗后肿瘤体积缩小了70%,而标准治疗仅能减少40%;在肺癌小鼠模型中,TZT-102的效果也明显优于现有的化疗药物。更重要的是,TZT-102表现出一系列有利的药理特性,表明它可能比其他药物递送平台更安全有效。
纽约大学Perlmutter癌症中心多发性骨髓瘤研究项目负责人加雷斯·摩根(Gareth Morgan)表示,TZT-102能够在肿瘤细胞中达到非常高的浓度,这使得治疗更加有效,同时减少了对健康组织的损害。他的同事费丝·戴维斯(Faith Davies)也认为,这种疗法在安全性和疗效上表现出了显著的优势。
学界的评价与前景
对于TZT-102的初步研究结果,学界给予了高度评价。清华大学的癌症治疗学研究者钱锋表示,TZT-102在小鼠中的肿瘤抑制效果非常令人印象深刻,而且副作用显著减少。麻省总医院系统生物学中心的癌症生物学家迈尔斯·米勒(Miles Miller)也认为,Tezcat公司的单体策略可能在促进肿瘤积累和减少非靶向效果方面特别有效。他表示:“他们的初步结果看起来很有希望。”
尽管有些药物递送方法试图利用巨胞饮作用,但结果往往不尽如人意。在某些情况下,药物被免疫细胞清除,或在脾脏和肝脏等器官中积聚,损害健康组织。Tezcat公司的方法通过部署靶向RAS相关的单体,同时确保其能迅速从体内清除,可能特别有效。
除了癌症治疗外,Tezcat公司的技术还有潜力应用于其他疾病。例如,神经退行性疾病、炎症状况和心血管疾病等也可能受益于这一技术平台。此外,该平台还可以用于诊断领域,帮助实时可视化肿瘤或在影像扫描中监测疾病进展。
为了避免资源过于分散,拉米雷斯和豪瑟决定为诊断应用成立一个独立的实体。新的公司IllumaRAS总部位于德克萨斯州休斯顿,旨在开发基于单体-结合物设计的成像工具,用于递送荧光染料或放射性同位素到RAS驱动的癌症中。
参考文献
Teng, K. W. et al. Nature Commun. 12, 2656 (2021).
Ramirez, C. et al. Nature 576, 477–481 (2019).
Beals, N. et al. Blood 142, 54 (2023).
https://www.nature.com/articles/d41586-024-02163-5


