骆卉妍教授:2024ASCO胃癌靶向研究新进展
时间:2024-07-07 06:00:45 热度:37.1℃ 作者:网络
编者按:2024年6月11日,第14届CGOG大会成功开幕,众多消化道肿瘤学专家、学者通过线上平台汇聚一堂,共同探讨胃癌治疗的最新进展。在本次大会的首场专题——胃癌ASCO速递中,中山大学肿瘤防治中心骆卉研教授为我们带来了胃癌靶向研究的最新进展,这些进度不仅为胃癌患者带来了新的治疗希望,也为临床医生提供了更多的治疗选择。本文将详细梳理各项研究的关键发现,为读者呈现胃癌治疗领域的最新动态。
CLDN 18.2的靶点
4036-SPOTLIGH研究的最终OS结果
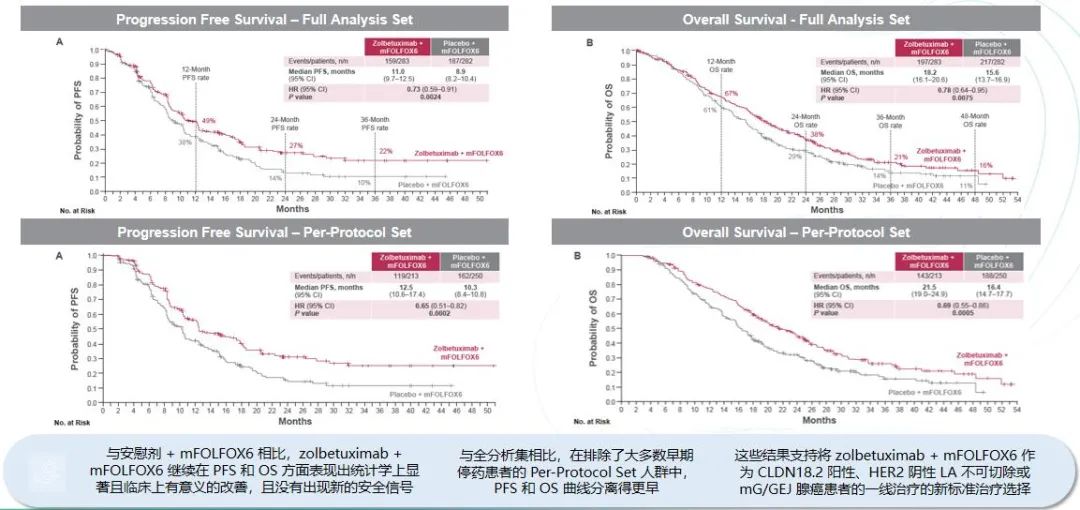
SPOTLIGHT研究评估了zolbetuximab联合mFOLFOX6化疗方案与单独使用mFOLFOX6方案在一线CLDN 18.2阳性胃癌患者中的疗效。
根据今年的数据更新,即使在更深层次的随访后,mFOLFOX6加上zolbetuximab的组合在无进展生存期(PFS)和总生存期(OS)上显示出持续的生存获益。特别是在排除了大多数早期停药患者的Per-Protocol Set(PPS)人群中,PFS和OS的获益曲线分离得更早,OS的分离更为显著。
最终分析结果进一步支持了以下观点:对于CLDN 18.2阳性的胃癌患者,在一线治疗中使用CLDN 18.2单克隆抗体联合化疗,可能成为这部分患者的新标准治疗选择。
2519-CLDN18.2/CD3双抗IBI389在实体瘤和GC/GEJC患者中的安全性和初步疗效研究
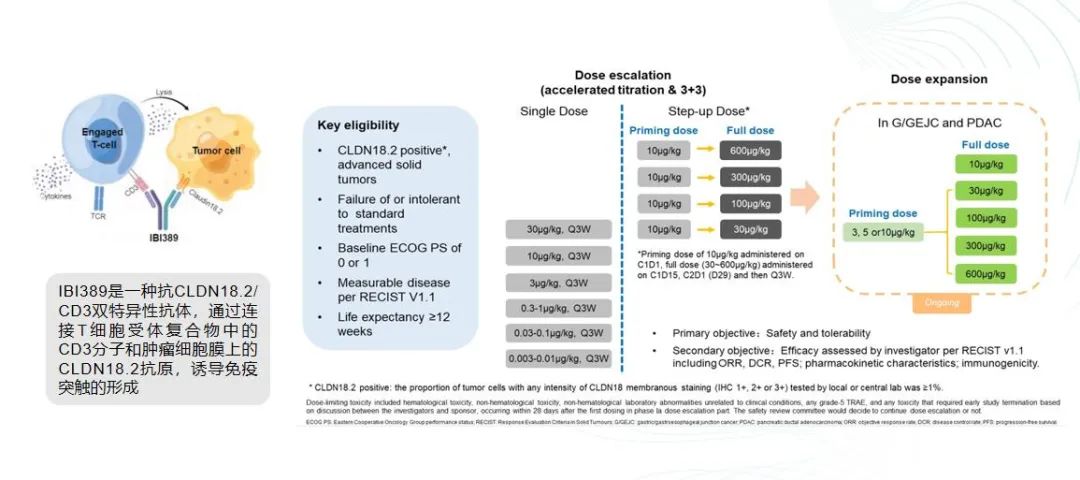
此项研究为针对CLDN 18.2与CD3的免疫双抗IBI389的Ⅰ期临床研究,主要在胃和胃食管结合部癌患者中展开。研究分为两个阶段:剂量递增和剂量扩展。
在剂量递增阶段,研究从最低剂量0.03μg/kg开始,逐步增加至660μg/kg。研究结果显示,这种免疫双抗在安全性方面表现出色,纳入的120名患者中,26名参与了剂量递增阶段。在剂量递增和剂量扩展阶段,未观察到剂量限制性毒性(DLT),也未达到最大耐受剂量。最常见的三级不良事件是肝功能中的谷氨酰转移酶升高和淋巴细胞减少。大约60%的患者出现了细胞因子释放综合征(CRS)相关不良事件,但三级CRS的发生率极低,仅有一例。
在疗效方面,所有患者的客观有效率(ORR)达到30.8%,疾病控制率(DCR)达到73.1%,中位无进展生存期(PFS)为3.5个月。研究对于CLDN 18.2阳性的患者,总体有效率更高。这些结果表明,这种免疫双抗在胃癌治疗中具有进一步探索的潜力。
Updates on Abstract 434420 - 针对晚期胃/胃食管结合部癌患者的Claudin 18.2 ADC CMG901的1期试验
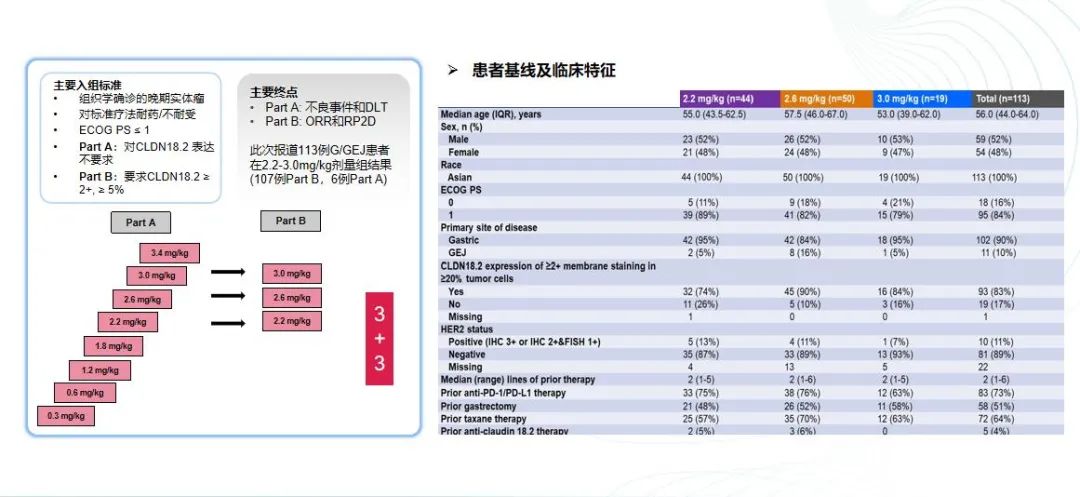
CMG901是一种针对CLDN18.2的首创抗体-药物偶联物,携带单甲基奥瑞司他汀E(MMAE),在2023年ASCO年会上已初步展示了其治疗潜力。今年,研究团队进一步更新了治疗结果。
中山大学肿瘤防治中心徐瑞华教授在ASCO会议上进行了口头汇报,详细介绍了CMG901的研究进展。该研究分为剂量递增的A部分(0.3-3.4 mg/kg)和剂量扩展的B部分(2.2、2.6和3.0 mg/kg)。报道主要集中在B部分,共有113例患者纳入研究,其中,G/GEJ癌症患者要求CLDN18.2表达为≥2+膜染色强度,在≥5%的肿瘤细胞中。大多数患者之前接受过PD-L1和紫杉类药物治疗,至少60%的患者之前接受过紫杉类治疗。
研究结果显示,无论患者之前是否接受过紫杉类或抗PD-1治疗,CMG901均显示出较好的有效率,整体有效率达到了35%,在2.2μg/kg剂量组中,有效率更是高达48%,而三个剂量组的中位OS均超过了11个月,显示出明确的生存和有效率提升。
在安全性方面,三个剂量组的耐受性均较好,未出现明显的不良反应事件。大于三级的不良事件主要集中在胃肠道反应,且发生率并不高,整体安全性可控。目前,CMG901已经转让给AstraZeneca,更名为AZD0901。AstraZeneca正在开展针对二线及二线以上治疗的Ⅲ期随机临床研究,以及更多针对一线治疗的Ⅱ期临床研究。
2501 - Claudin18.2 CAR-T 治疗胃肠肿瘤:CT041-CG4006 1期试验的最终结果

此项研究为北京大学肿瘤医院沈琳教授团队研究,由齐长松教授公布的CAR-T细胞疗法1期临床试验,是一项单臂、开放标签的研究,旨在评估靶向CLDN18.2的CAR-T细胞产品CT041在CLDN18.2阳性晚期胃肠道(GI)肿瘤患者中的安全性和有效性。试验采用“3+3”设计进行剂量递增,并在剂量扩展阶段设立了四个不同的队列(队列1:CT041用于标准治疗失败的晚期GI肿瘤患者,队列2:CT041联合PD-1单抗治疗用于接受过治疗的晚期GI肿瘤患者,队列3:胃癌一线治疗后序贯CT041,队列4:CT041用于先前对抗CLDN18.2抗体治疗失败的患者),以探索CT041在不同治疗背景下的应用。
研究共纳入98例患者,大多数为CLDN18.2中高表达的患者,且多数患者已接受过二线或以上治疗。CT041治疗的客观缓解率(ORR)达到了37.8%,特别是在队列3中,胃癌一线治疗后接受CT041治疗的患者,中位PFS达到了15.2个月。
对于胃癌患者,CT041治疗的ORR率为54.9%,中位持续缓解时间(DOR)为6.4个月,显示出显著的疗效提升。此外,CT041的安全性良好,未观察到治疗相关的严重不良事件,主要不良事件与前期化疗相关的血液毒性相符。
在亚组分析中,CLDN18.2高表达且无肝脏或骨转移的患者,从CAR-T治疗中获得了更好的生存获益。长期随访结果表明,CAR-T治疗前景广阔,安全性良好,且不同组合策略针对不同患者群体的探索,为未来的研究方向提供了明确的方向。
针对CLDN18.2这一靶点,目前在胃癌治疗领域已成为一个备受瞩目的焦点,预计不久的将来,CLDN18.2将成为改变胃癌治疗格局的重要靶点,为胃癌治疗带来新的突破。
VEGFR靶点
Updates on Abstract 438730 –FRUTIGA研究
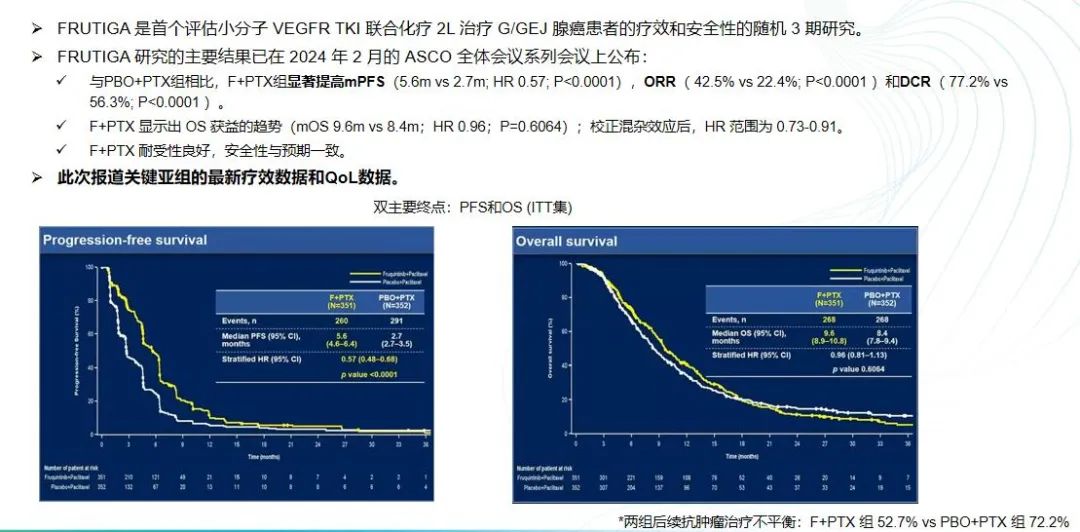
今年,针对VEGFR2靶点的临床研究取得了显著进展,其中包括徐瑞华教授团队在晚期胃癌二线治疗中进行的FRUTIGA研究。这项Ⅲ期随机对照临床研究比较了呋喹替尼联合紫杉醇与单药紫杉醇的疗效,其初步结果已于今年2月在ASCO线上会议上公布。
研究数据显示,呋喹替尼联合紫杉醇治疗显著延长了患者的PFS,从2.7个月延长至5.6个月,ORR也从单药紫杉醇的22.4%提高至42.5%。DCR显著提升,而OS虽未达到统计学差异,但显示出获益趋势。整体耐受性和安全性良好。
在ASCO会议上进一步报道了关键亚组的疗效情况。不同亚组分析显示,大多数亚组中观察到呋喹替尼联合紫杉醇治疗的生存获益,特别是在非弥漫性胃癌患者和淋巴结转移患者中,生存获益更为明显。对于这部分患者,PFS从2.7个月提高至6.1个月,OS从7.9个月提高至9.6个月,且OS显示出明显的统计学意义上的获益。有效率和DCR也得到进一步提升,提示这一亚组患者可能从呋喹替尼联合紫杉醇治疗中获得更好的生存获益。
此外,生活质量的报道显示,紫杉醇基础上加用呋喹替尼不会对患者生活质量产生不利影响。这一新的联合治疗模式可能成为晚期二线胃癌患者的新治疗选择。
总结
本次CGOG年会-胃癌ASCO速递所展现的胃癌靶向研究成果,凸显了靶向治疗在胃癌治疗中的重要性和潜力。CLDN 18.2靶点已成为今年肿瘤治疗领域备受关注的靶点,其中多项研究显示了,针对该靶点的单克隆抗体、免疫双特异性抗体、ADC以及CAR-T疗法的有效性和安全性。VEGFR2靶点的研究也取得了显著进展,这些研究不仅为胃癌患者带来了新的治疗希望,也为未来的研究方向提供了明确的方向。随着这些研究成果的进一步验证和应用,我们有理由相信胃癌治疗将迈入一个全新的时代。


