European Radiology:通过深度学习预测脑膜瘤分级和病理标记物表达
时间:2024-07-04 12:05:16 热度:37.1℃ 作者:网络
脑膜瘤起源于蛛网膜帽状细胞,是成人最常见的颅内轴外肿瘤,占中枢神经系统原发性肿瘤的39.0%,发病率为9.12/10万。约80%的病例为WHO1级脑膜瘤,组织学为良性,15-20%为2级(非典型) 脑膜瘤,1-3%为3级脑膜瘤(间变性) 脑膜瘤,特征为恶性程度更高,复发倾向更强,总体预后更差。一般而言,1级脑膜瘤采用全切除或放射治疗可获得良好预后,2级和3级脑膜瘤宜采用全切除联合辅助放疗。因此,对脑膜瘤患者术前进行准确的分级,可以改善预后并有利于临床决策。
Ki-67、组蛋白H3 (H3K27me3) 的赖氨酸27三甲基化 (K27) 和孕激素受体 (PR) 被认为是脑膜瘤预后的良好病理标志物。其中,Ki-67标记指数与细胞增殖高度相关,被认为是脑膜瘤的重要预后指标。在1级脑膜瘤中,复发风险增加与Ki-67表达增加有关。此外,H3K27me3 在肿瘤发生中起重要作用,它通过同源重组修复影响双链DNA损伤修复。
基于深度学习 (DL) 的放射组学是一种新开发的从各种放射图像中提取大量特征的方法。DL算法总是利用卷积神经网络 (CNN) 直接从成像数据中挖掘复杂的视觉信息特征,从医学图像中深度提取特征。由于它们的计算速度快、建模所需的时间更短,DL模型已应用于各种脑肿瘤的原发肿瘤识别、鉴别诊断、分级、突变和侵袭评估、治疗反应和复发预测。DL模型对脑膜瘤患者术前肿瘤分级、静脉窦侵犯和脑实质侵犯显示出良好的识别和预测潜力。

近日,发表在European Radiology杂志的一项研究建立了一项可预测脑膜瘤肿瘤分级及病理标志物表达的深度学习模型,为临床进行准确的术前诊断及分级评估提供了技术支持。
本项研究回顾性分析了2018年9月至2021年12月期间两个中心接受手术切除的1192例脑膜瘤患者。收集每位患者的病理资料及造影后的T1-weight图像。来自I研究所的患者被细分为培训组、验证组和测试组,而来自II研究所的患者作为外部测试队列。采用基于迁移学习的精细ResNet50模型对整个队列进行WHO分级,预测1级脑膜瘤的Ki-67指数、H3K27me3和孕激素受体(PR)状态。通过准确度和损失曲线、混淆矩阵、受试者工作特征曲线(ROC)和曲线下面积(AUC)评价预测效果。
每个标签的深度学习预测模型在两个队列中取得了较高的预测性能。对于WHO分级预测,内部测试组的曲线下面积(AUC)为0.966 (95%CI 0.957-0.975),外部验证组的曲线下面积(AUC)为0.669 (95%CI 0.643-0.695)。预测Ki-67指数、H3K27me3、PR状态的AUC在内测组分别为0.905 (95%CI 0.895 ~ 0.915)、0.773 (95%CI 0.760 ~ 0.786)、0.771 (95%CI 0.750 ~ 0.792),在外验证组分别为0.591 (95%CI 0.562 ~ 0.620)、0.658 (95%CI 0.648 ~ 0.668)、0.703 (95%CI 0.674 ~ 0.732)。
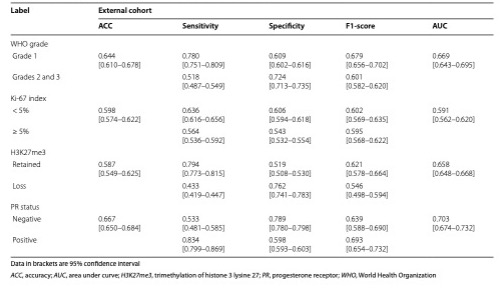
表 不同指标在队列中的预测表现
本项研究表明,DL模型能较好地预测脑膜瘤分级及病理标志物的表达。
原文出处:
Jiawei Chen,Yanping Xue,Leihao Ren,et al.Predicting meningioma grades and pathologic marker expression via deep learning.DOI:10.1007/s00330-023-10258-2


