AL型淀粉样变性的诊断和治疗:新加坡骨髓瘤工作组专家共识
时间:2024-07-01 13:01:24 热度:37.1℃ 作者:网络
AL型淀粉样变性
AL型淀粉样变性是最常见的系统性淀粉样变,但其症状具有非特异性,需要加强临床怀疑,以便在临床中发现无法解释的临床表现。早期发现和治疗至关重要,因为心脏受累程度是AL型淀粉样变性患者生存的主要预后预测因素。
在通过组织活检诊断为AL型淀粉样变性后,应立即开始以硼替佐米、环磷酰胺和地塞米松为基础的一线诱导治疗,联合或不联合达雷妥尤单抗。治疗目标是尽可能达到最佳的血液学反应,理想情况下游离轻链<20mg/L,因其可提供器官功能改善的最佳机会。
如果患者在治疗2个周期内没有达到部分缓解,或在4个周期后或自体干细胞移植后没有达到非常好的部分缓解,则应改变治疗,因为获得深度和持久缓解可转化为更好的器官缓解和长期结局。肾脏、心脏病、神经科和胃肠科等多学科专科医生早期参与可给予受累器官的最佳维护和支持。
近日《Annals Academy of Medicine Singapore》发表了新加坡骨髓瘤工作组起草的AL型淀粉样变性共识指南,现整理主要内容供参考。该共识与中国指南和美国发表的综述有所差异,亦有一定参考价值。

诊断、分期和风险分层
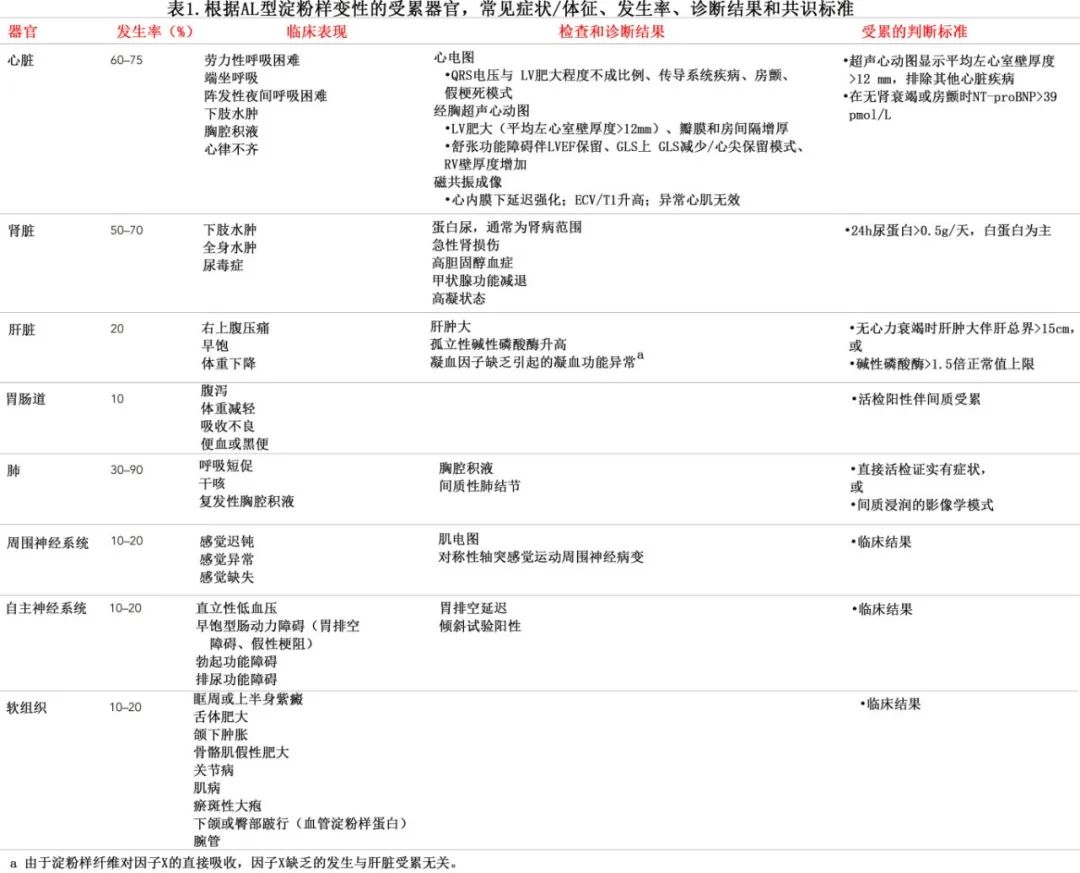
开始治疗之前必须先确诊,确定疾病累及的范围、部位和严重程度及其临床结局,以及详细评估可能影响治疗选择的合并症。表1为AL型淀粉样变性的发生率、器官受累症状、诊断结果和确定器官受累的共识标准。由于其症状多与终末器官功能障碍有关,并且晚期淀粉样变性死亡率较高(即使治疗),因此在适当的临床环境中应对不明原因的表现进行高度怀疑,从而早期诊断AL型淀粉样变性,最终提高患者总生存率。
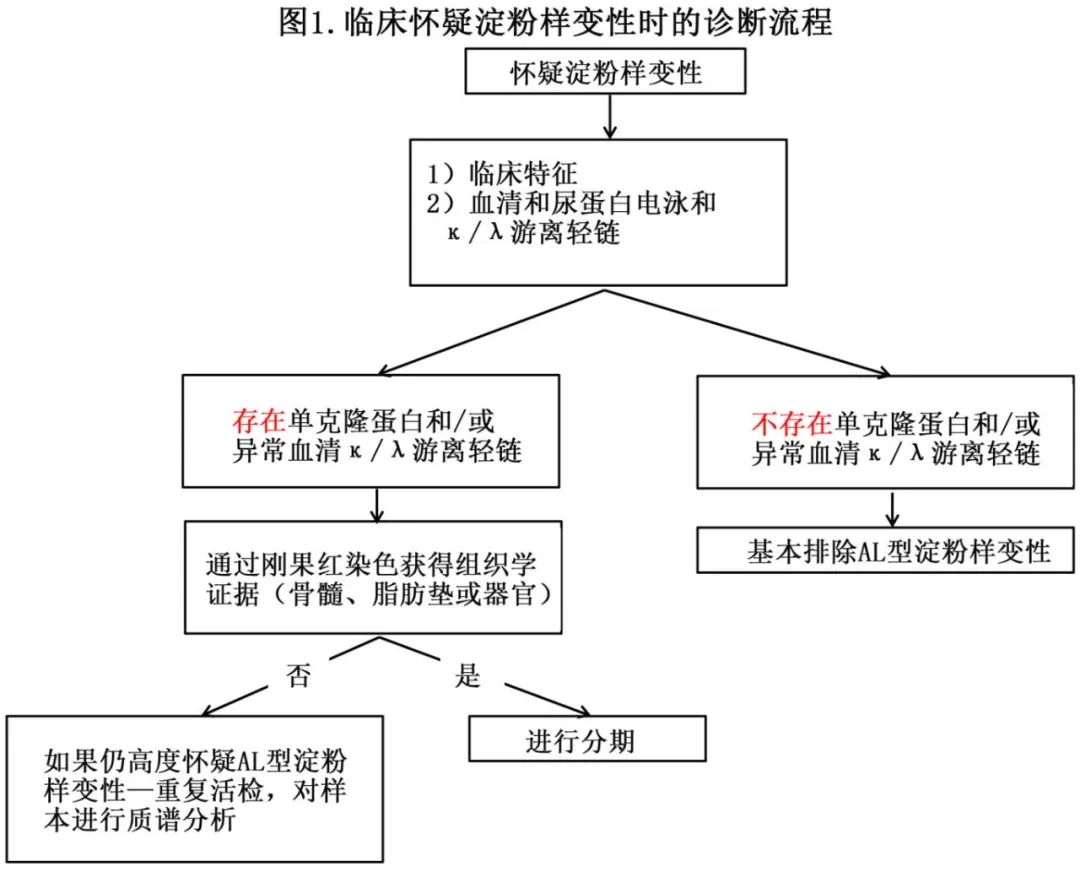
在临床怀疑淀粉样变性的情况下,患者检查的流程如图1所示。
一旦确诊为 AL型淀粉样变性,则需要进一步检查以评估器官受累,如表2所示。

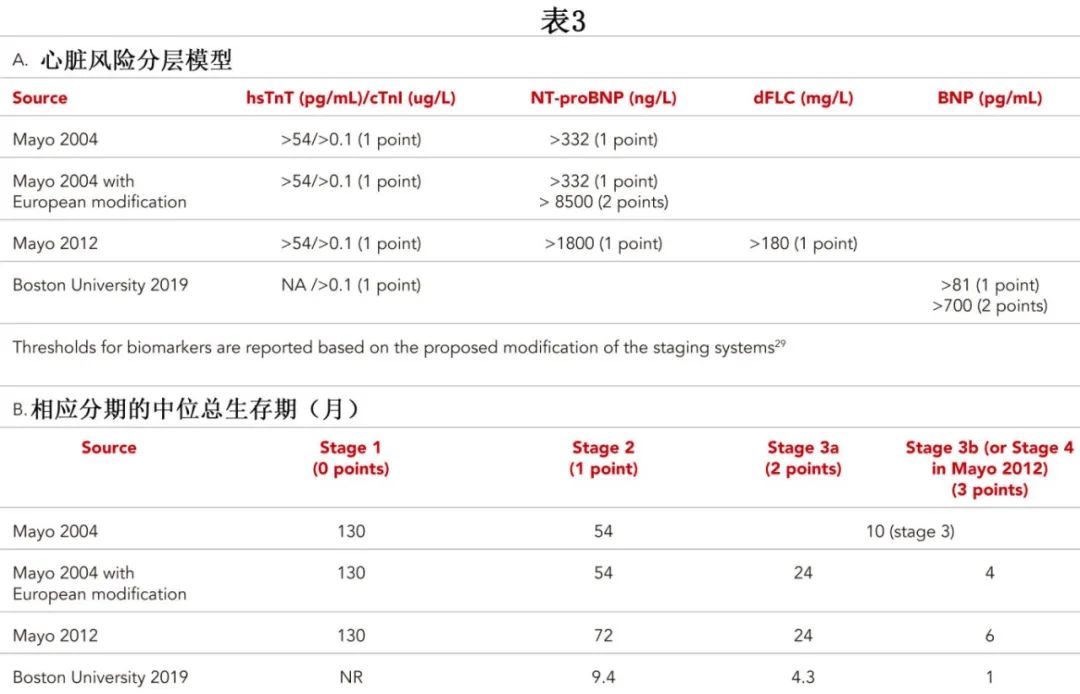
心脏受累程度是短期和长期生存的唯一最重要预测因素。主要的心脏风险分层模型见表3。
此外,肾脏分期模型有助于预测患者透析依赖的风险(表4)。

治疗
治疗目标
治疗目标应为患者尽可能达到最佳血液学缓解(如可行,受累游离轻链[iFLC] <20mg/L),因为这是器官功能改善的最佳机会。但须与治疗相关毒性和评估的局限性进行权衡。
治疗开始后2个周期内未达到至少部分缓解 (PR) 或4个周期后或自体干细胞移植 (ASCT) 后达到 VGPR 的患者应考虑接受其他治疗。
实现深度和长期的克隆缓解可转化为更好的器官反应,应该是治疗的长期目标。
建议多学科亚专科医生(如肾病医生、心脏病专家、神经科医生和胃肠病学家)早期参与,以对受累器官进行最佳维持和支持。
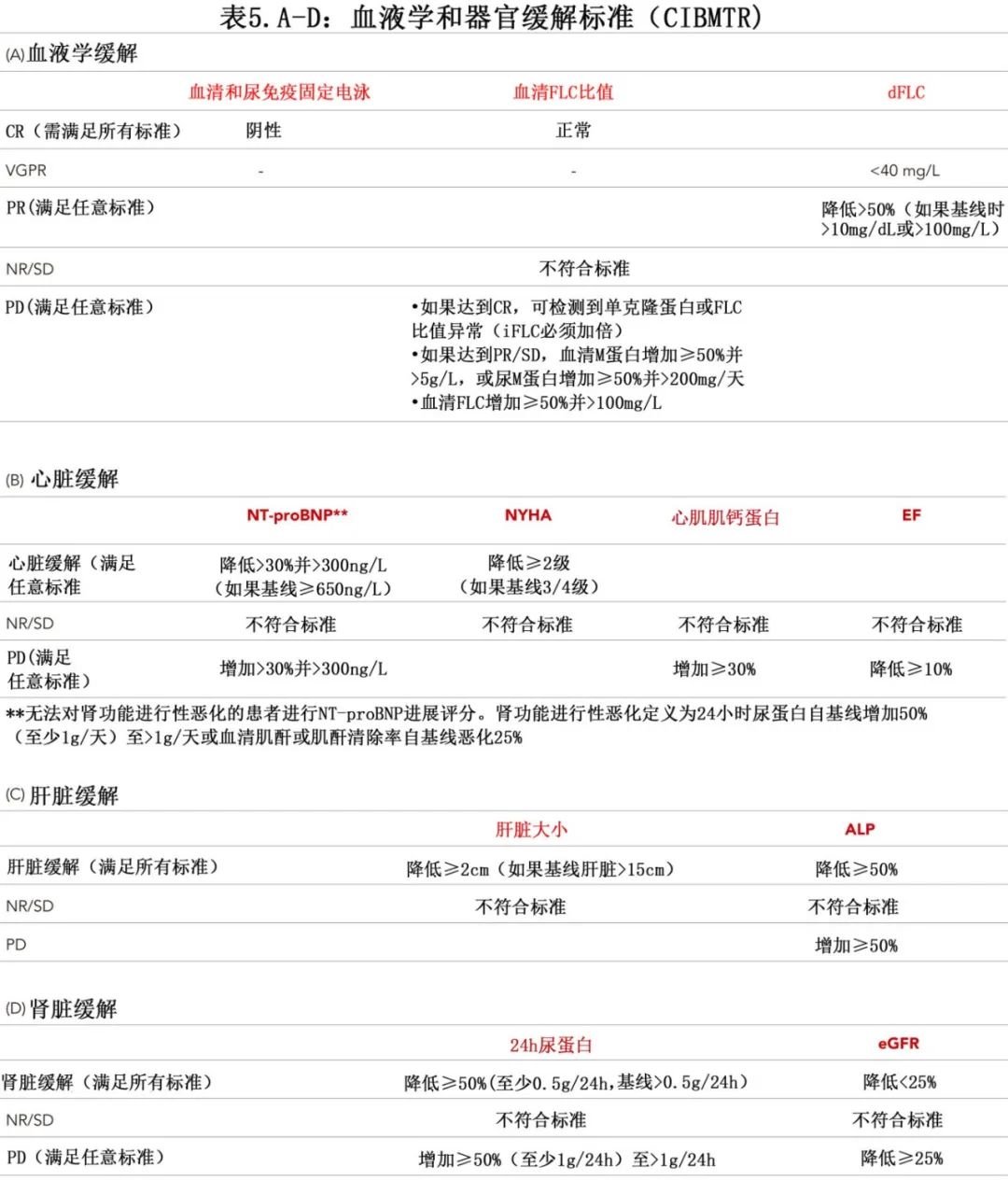
FLC浓度的早期和深度降低与器官恢复的最大机会(表5)及无进展生存期(PFS)和总生存期(OS)的延长相关。
治疗选择
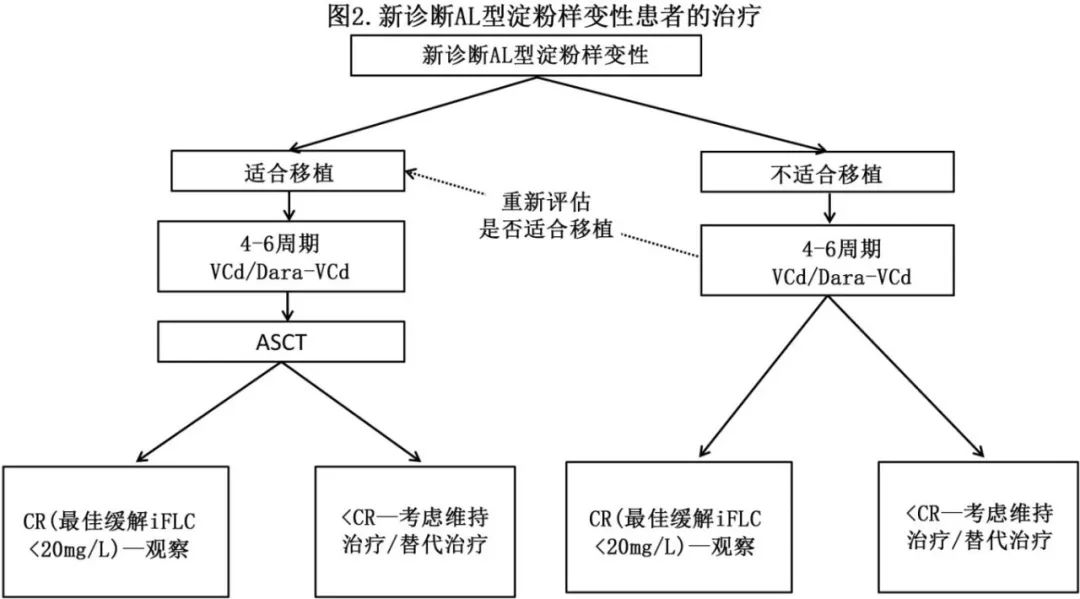
一线治疗:
推荐的一线诱导为联合化疗;硼替佐米环磷酰胺和地塞米松联合或不联合达雷妥尤单抗
如果初始治疗为VCD,2个周期后缓解不佳 (<VGPR) 的患者可考虑加用达雷妥尤单抗以加深缓解。
对于无共存 MM或高危 FISH 异常的患者,诱导治疗持续时间4-6个周期;共存 MM或高危 FISH 异常的患者应考虑6-12个月的诱导治疗以及后续维持治疗。
必须在每个化疗周期后评价治疗反应参数(即风险比 [HR] 和比值比 [OR])。
造血干细胞移植:
适合移植患者均应考虑高剂量化疗序贯自体干细胞移植 (ASCT) 。
ASCT的时间将根据具体情况决定。
在有淀粉样变性 ASCT 经验的中心进行患者选择和评估至关重要。对于适合移植但不可能耐受全剂量美法仑的患者,可酌情考虑风险调整方案(risk-adapted approach)。
维持治疗
对于高危 FISH 异常或骨髓瘤表型(诊断时浆细胞>10%)的患者,可考虑在 ASCT 后进行维持治疗。
ASCT后未达到 CR 的患者可考虑进一步继续治疗,同时平衡治疗相关毒性的风险。
目前不建议根据 MRD 结果决定治疗方案,应仅在临床试验背景下考虑。
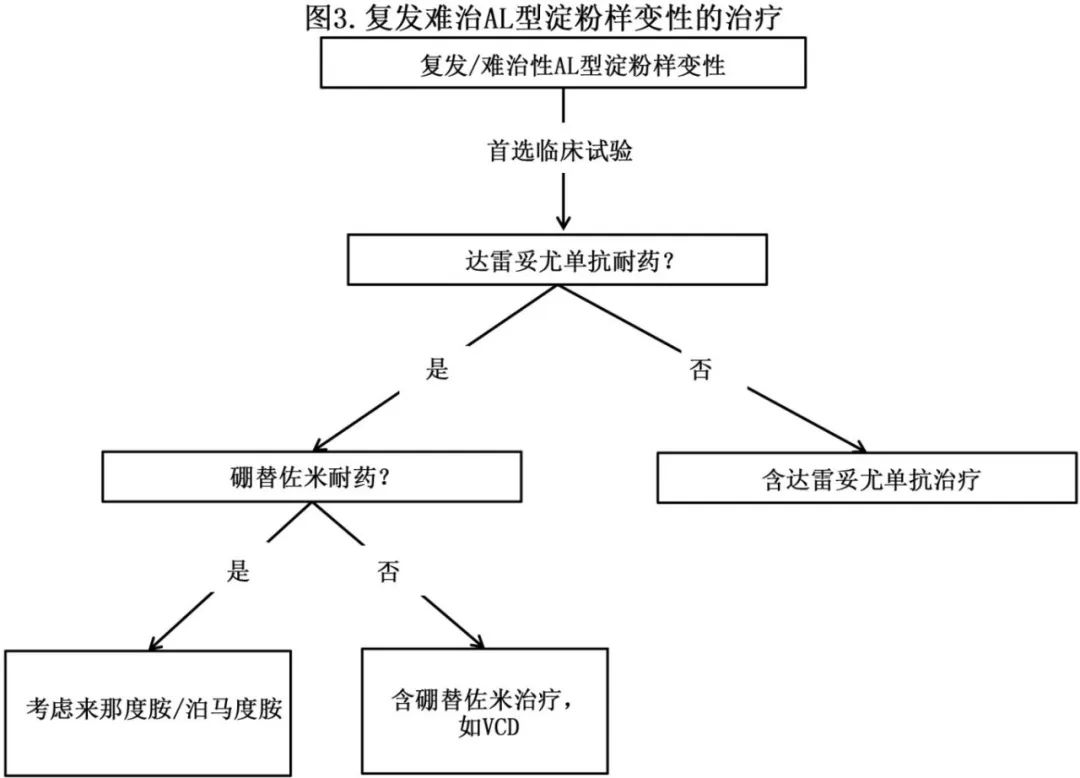
复发难治性AL型淀粉样变性的治疗
一线治疗后未达到最佳缓解血液学 VGPR的患者应考虑接受二线治疗。对于复发时何时重新开始治疗尚未达成共识。大多数人同意器官功能恶化表明需要早期开始治疗,因为心脏进展预示着生存期缩短,肾脏进展预示着需要早期透析。然而,在器官进展发生前,是否由于 iFLC 升高(不符合血液学进展)而重新开始或改变治疗仍有争议。
对于达雷妥尤单抗耐药的患者,达雷妥尤单抗联合地塞米松是首选挽救治疗方案。
硼替佐米-地塞米松是达雷妥尤单抗耐药和硼替佐米敏感患者的首选挽救治疗方案。伊沙佐米+地塞米松是替代方案。
来那度胺-地塞米松或泊马度胺-地塞米松是达雷妥尤单抗和蛋白酶体抑制剂耐药患者的首选挽救治疗。
支持治疗
多西环素的临床前研究证实具有抗纤维化作用,很多研究建议用于心脏淀粉样变性患者。但北京协和医院李剑教授发现多西环素加入VCD未改善PFS或心脏PFS。因此其地位有争议。
心力衰竭或并发症的管理
应联合使用袢类利尿剂和盐皮质激素受体拮抗剂治疗液体超负荷。
由于存在严重低血压风险,应避免使用或慎用β受体阻滞剂和ACEi/ARB。
地高辛可慎重用于 AF 的心率控制,但需频繁监测地高辛水平/毒性。胺碘酮和消融也是合理选择。建议与心脏病专家进一步讨论。
肾衰或并发症的管理
AL型淀粉样变性和肾病综合征患者从诊断至透析的中位时间为14个月,1/3的患者需要透析。水肿的主要治疗为利尿剂。ACEI 可减少蛋白尿患者的蛋白尿,但考虑到高钾血症的风险,必须仔细监测电解质。这些患者的透析可能具有挑战性,因为许多患者可能伴随心脏淀粉样蛋白或体位性低血压伴复发性透析中低血压发作。动静脉瘘的建立也可能增加出血风险,尤其是在凝血病或血管和皮肤淀粉样蛋白患者中。
胃肠道并发症的管理
AL型淀粉样变性累及胃肠道的常见症状包括腹泻和便秘交替、体重减轻、胃灼热和恶心,高达50%的患者可能出现胃肠道出血。对于有动力障碍症状的患者,建议进行营养补充和饮食调整,包括经常食用低可溶性纤维和脂肪的小容量液体或匀浆食物,以及促动力药,如甲氧氯普胺、红霉素或多潘立酮。对于腹泻患者,可开始使用抗腹泻药物,如洛哌丁胺。
器官移植
在特殊情况下,可考虑器官移植(心、肾)。

药物毒性和剂量调整
硼替佐米每周一次皮下给药。
密切监测毒性作用,包括心脏毒性、低血压、神经病变。
如果耐受,在剂量递增前可以考虑硼替佐米和地塞米松的初始较低剂量,以避免晚期心脏病患者(Mayo 3b期)的过度毒性。
肾功能不全或长期透析的患者需要调整治疗(表9)。

参考文献
Tan M,et al. AL amyloidosis: Singapore Myeloma Study Group consensus guidelines on diagnosis, treatment and management.Ann Acad Med Singap . 2023 Nov 29;52(11):601-624. doi: 10.47102/annals-acadmedsg.2023101.

