【EASL2024速递】乙肝新药JNJ-3989研究进展汇总
时间:2024-06-29 06:04:25 热度:37.1℃ 作者:网络
编者按
2024年欧洲肝脏研究协会(EASL)年会-国际肝脏大会(ILC 2024)于2024年6月5 - 8日在意大利米兰举行。会议期间披露了多项乙肝新药研究进展,肝霖君精选其中的重要进展与大家分享。
JNJ-3989是Arrowhead Pharma和Janssen共同开发的一款siRNA药物,目前该药物的全球权益已转让给GSK。前期II期研究显示JNJ-3989 + NA ± JNJ-6379可使HBsAg平均下降1.9-2.6 log,70% - 75%的患者HBsAg降至< 100 IU/mL,但几乎无患者实现HBsAg清除,联合JNJ-6379的三联疗法与二联疗法效果相似;而JNJ-3989 + NA ± JNJ-6379序贯联合聚乙二醇干扰素α(PegIFNα)在免疫耐受期患者中有19%的患者出现至少一次的HBsAg清除,其中70%(7/10)在最后检测时间点维持HBsAg清除。
ARC-520是Arrowhead Pharma开发的另一款siRNA药物,因安全性问题现已终止开发。
本次EASL2024大会摘要披露了有关JNJ-3989的最新研究数据,JNJ-3989(负荷剂量)+ NA + nivolumab可使HBsAg平均下降2 log10 IU/mL,约90%的患者HBsAg降至< 100 IU/mL,至停药随访24周70%-85%维持HBsAg < 100 IU/mL,无患者获HBsAg清除;siRNA药物JNJ-3989或ARC-520治疗结束后平均随访52个月有31.2%的患者HBsAg < 100 IU/mL,基线HBsAg水平和治疗后最大HBsAg降幅与随访结束时HBsAg < 100 IU/mL的患者比例独立相关。
研究一
JNJ-3989(负荷剂量)联合nivolumab未能提高抗病毒疗效

研究方法
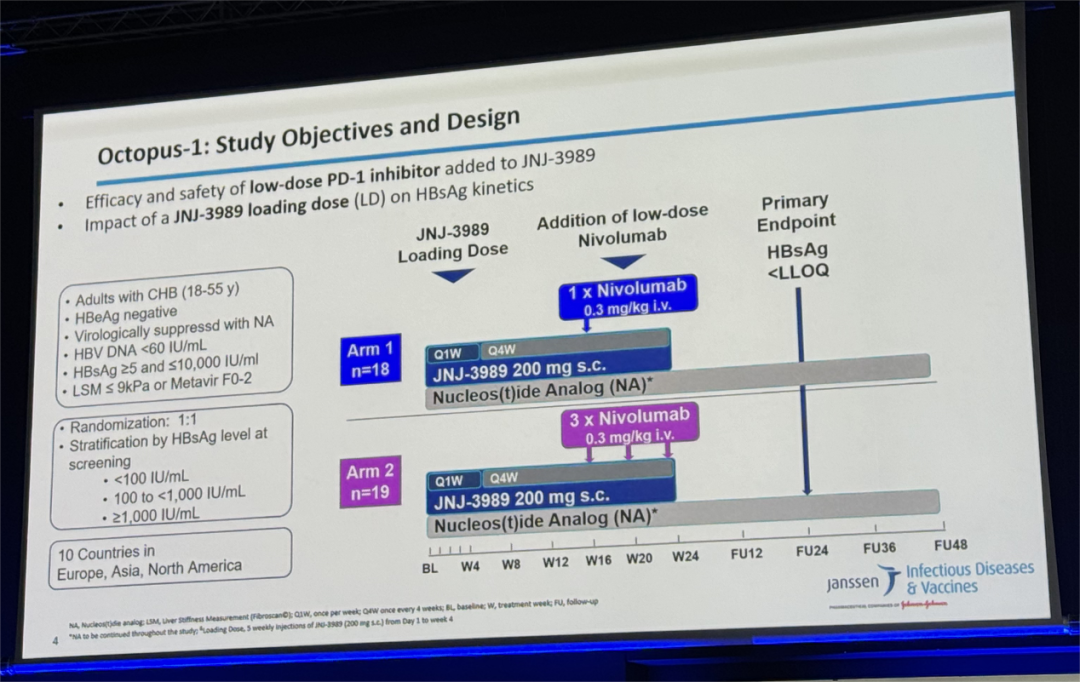
OCTOPUS-1是一项随机、多中心、开放标签、平行组对照的II期研究,纳入HBeAg阴性、病毒学抑制的慢乙肝患者接受JNJ-3989 + nivolumab + NA治疗,根据nivolumab的给药次数分为Arm 1和2,具体给药方式如下:
JNJ-3989 200 mg,QW(负荷剂量),治疗4周,随后Q4W治疗至24周;
nivolumab(0.3 mg/kg,IV),Arm 1:第16周给药1次;Arm 2:第16、20、24周共给药3次;
NA,QD,在停药随访期间维持治疗。
主要终点为停药随访24周时的HBsAg清除率,同时评估病毒标志物(HBsAg、HBcrAg和HBV DNA)水平变化和安全性。
研究结果
研究共入组37例患者(Arm 1 : 18 例,Arm 2 : 19例),所有患者均完成JNJ-3989给药。最后2例患者在第3剂nivolumab给药前进行了方案修订,停止nivolumab给药。患者平均年龄(SD)为 44.38(7.38)岁,18.9%为女性,37.8%为亚洲人。Arm 1和Arm 2基线平均HBsAg水平分别为3.25(0.47)、3.13(0.54)log10 IU/mL;Arm 1中基线HBsAg水平< 100 IU/mL、100至< 1000 IU/mL、≥ 1000 IU/mL的患者比例分别为0%、38.9%和61.1%,Arm 2分别为0%、42.1%和57.9%。
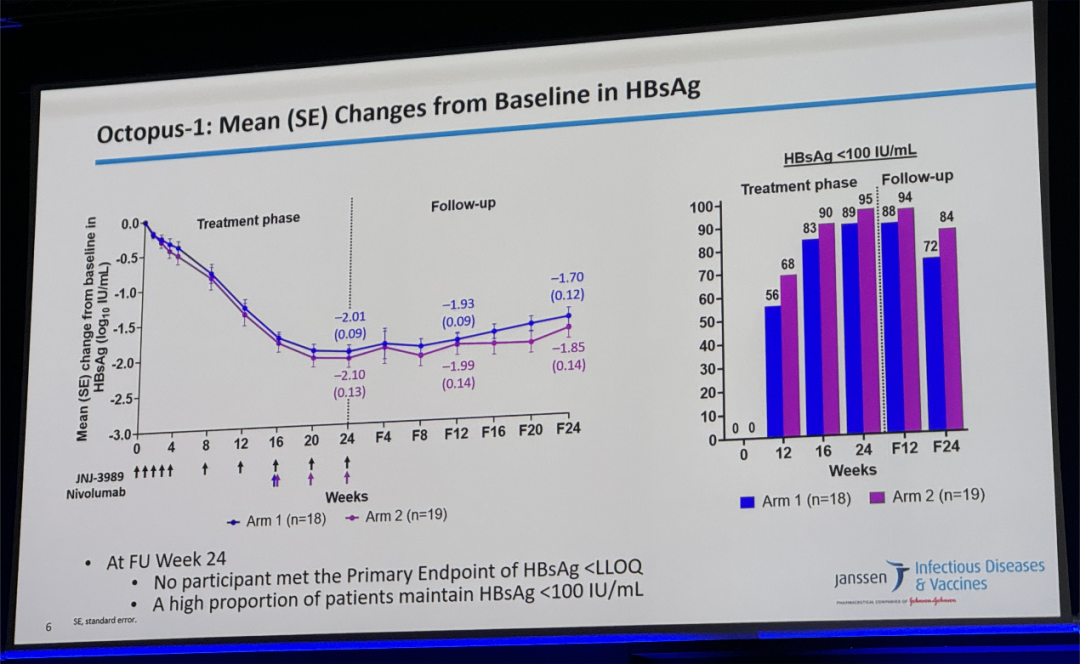
Arm 1和Arm 2在第24周HBsAg相比基线平均下降2.01(0.09)和2.10(0.13)log10 IU/mL,其中58.8%和55.6%的患者HBsAg降幅≥ 2 log10 IU/mL,89%和95%的患者实现HBsAg < 100 IU/mL。到随访24周,Arm 1和Arm 2 HBsAg相比基线平均下降1.70(0.12)和1.85(0.14)log10 IU/mL,72%和84%的患者维持HBsAg < 100 IU/mL,两组均无患者获HBsAg清除。Arm 2有1例患者在随访40周(研究结束之后)获HBsAg清除。
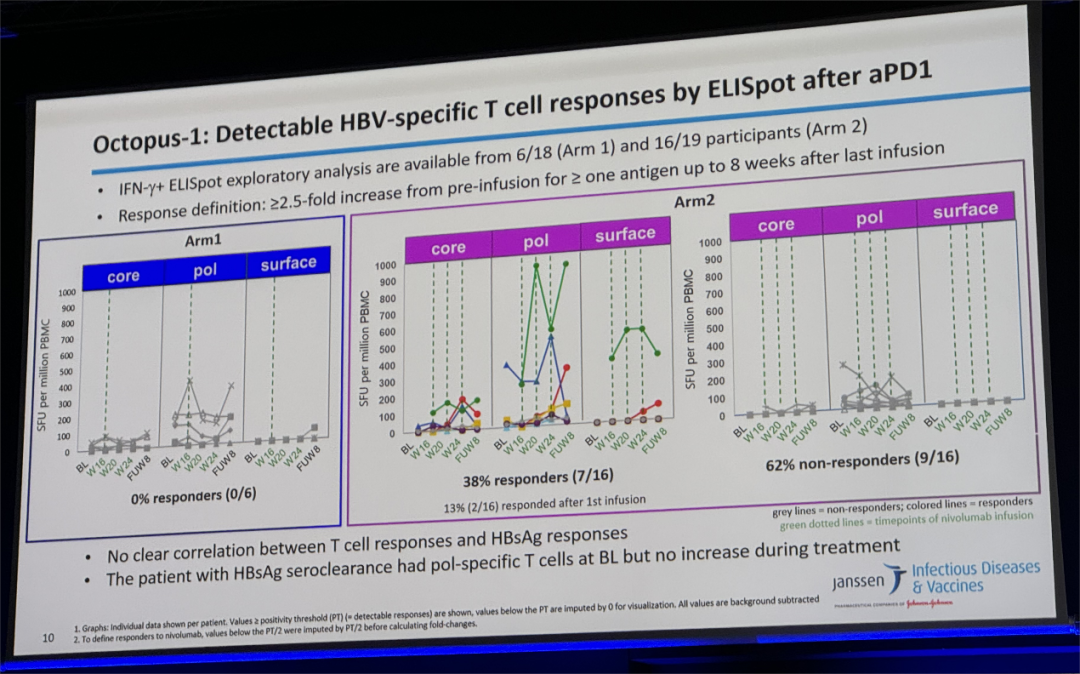
29/35(83%)的患者在第16周nivolumab给药后2小时受体占用率大于90%。Arm 1和Arm 2分别有6例、16例患者进行了HBV特异性T细胞应答分析,应答定义为直到末次输注nivolumab后8周,≥ 1种抗原特异性T细胞相比输注前增加> 2.5倍。Arm 1无患者实现应答,Arm 2有38%的患者实现应答。T细胞应答者和HBsAg应答者之间无明确相关性,1例随访40周实现HBsAg清除的患者在基线检测到pol-特异性T细胞但治疗后水平未增加。
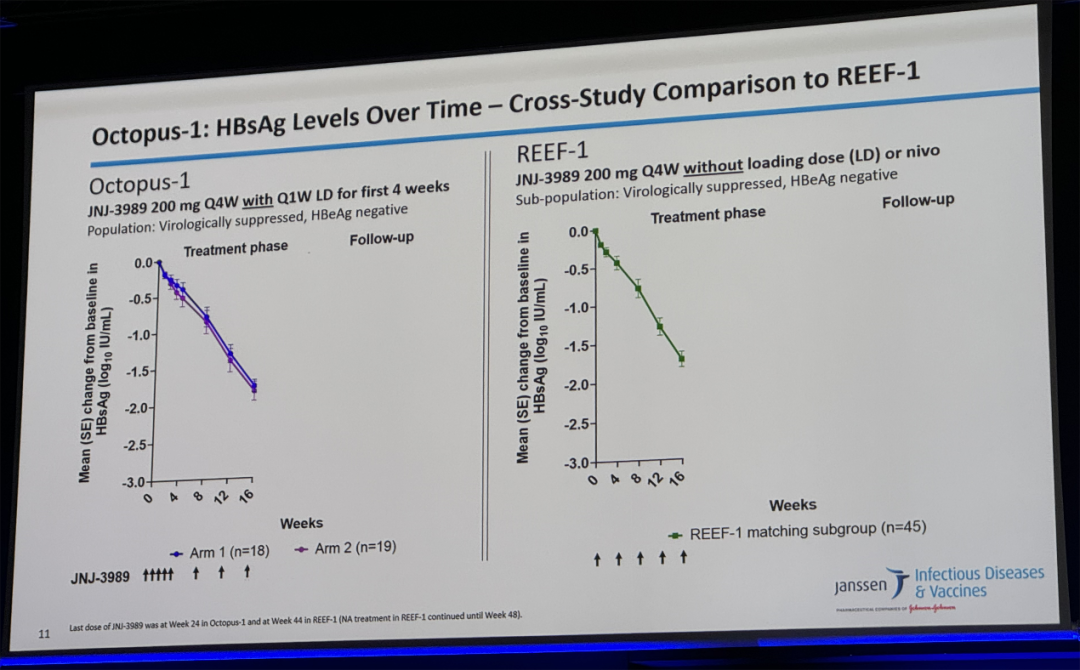
与同样针对病毒学抑制、HBeAg阴性患者的REEF-1研究(JNJ-3989未给予负荷剂量)相比,本研究前4周JNJ-3989给予负荷剂量并未提高患者的HBsAg下降水平。
没有观察到SAE或 3/4 级AE,无患者提前结束研究。48.6%的患者出现TEAE,其中13.3%与JNJ-3989相关,5.4%与nivolumab相关。JNJ-3989负荷剂量导致平均ALT水平轻度升高,从基线的23 U/L升高至第8周的35 U/L,直至治疗结束没有进一步升高,无患者达急性升高标准。Arm 1有2例患者在接受nivolumab治疗8周后出现促甲状腺激素(TSH)抑制,这导致了后续nivolumab给药终止,2例患者均迅速缓解。未观察到其他免疫相关事件或病毒学突破。
研究结论
JNJ-3989 + NA + nivolumab治疗24周,两组患者HBsAg相比基线的降幅均达2 log10 IU/mL。JNJ-3989与REEF-1中病毒学抑制、HBeAg阴性患者的交叉研究分析显示,JNJ-3989负荷剂量或nivolumab均未明显提高疗效。治疗总体上安全耐受,但由于观察到TSH抑制,研究中低剂量nivolumab的使用被终止。
研究二
JNJ-3989或ARC-520治疗后的长期疗效与基线HBsAg水平、最大HBsAg降幅独立相关

研究方法
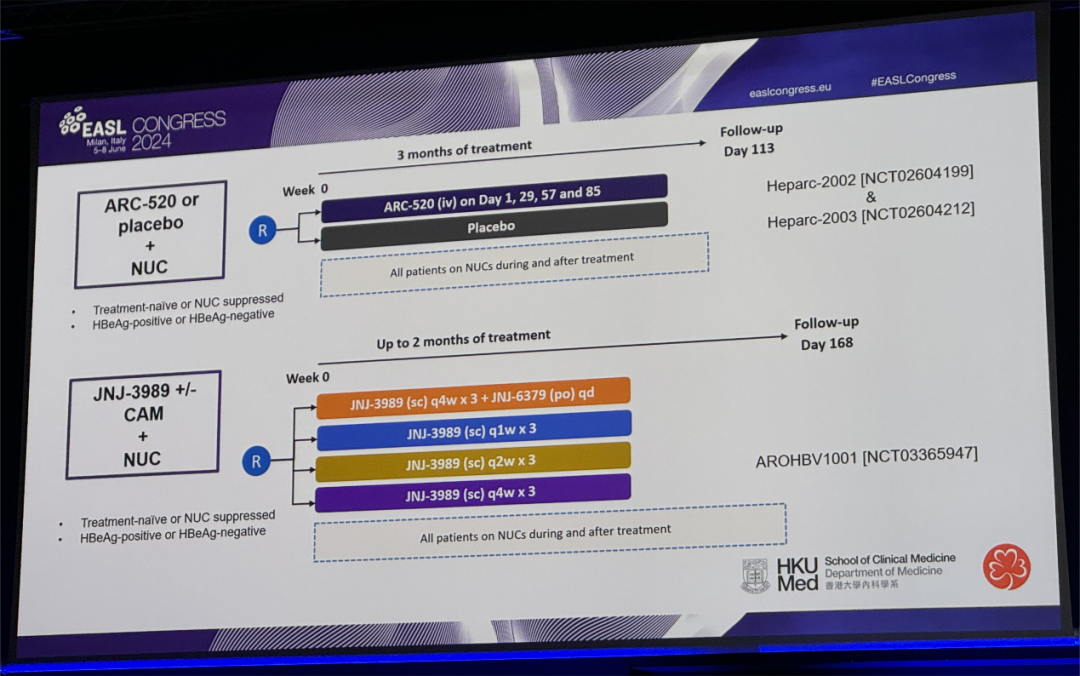
该研究前瞻性随访了接受短期siRNA治疗的慢乙肝患者,siRNA包括ARC-520(4剂,Heparc-2002和Heparc-2003研究)或JNJ-3989(3剂,AROHBV1001研究),均联合NUC治疗。纳入受试者中前期接受ARC-520 + NUC治疗15例,JNJ-3989 + NUC治疗38例,安慰剂 + NUC治疗5例。根据原始方案连续采血,每24周一次,直到最后一次随访(LFU,平均持续时间52.5 ± 14.4个月)。根据多元回归分析结果,采用整数计分系统构建LFU时实现qHBsAg < 100 IU/mL的模型评分。
研究结果
53例接受siRNA + NUC治疗患者的平均年龄为46.8岁,基线HBsAg水平为3.08 log10 IU/mL,其中5.7%的患者基线HBsAg < 100 IU/mL,83%为NUC经治,34%为HBeAg阳性。
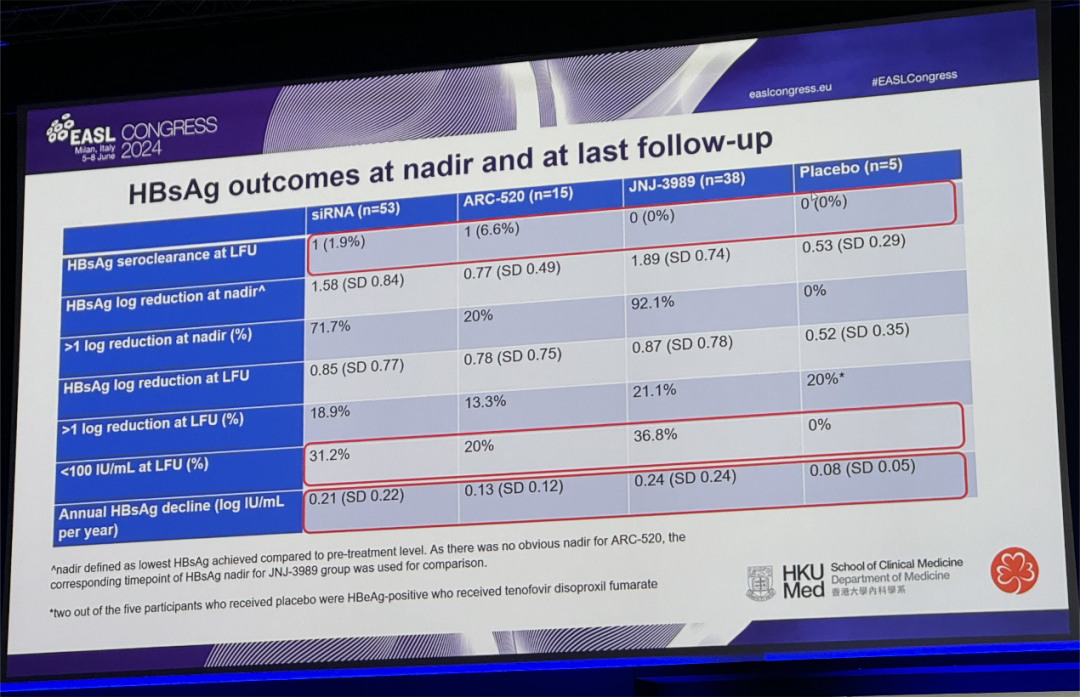
siRNA治疗受试者在LFU时达到HBsAg清除或< 100 IU/mL的患者比例分别为1.9%和31.2%,而安慰剂组均为0%。siRNA治疗和未治疗受试者在LFU时的平均HBsAg降幅分别为0.85、0.52 log(p = 0.123)。在LFU时两种siRNA药物的qHBsAg水平均比安慰剂低,但无统计学意义(第72个月,ARC-520 vs 安慰剂:2.15 vs 2.52 log10 IU/mL,p = 0.503;第60个月,JNJ-3989 vs 安慰剂:1.86 vs 2.63 log10 IU/mL, p = 0.368)。与安慰剂相比,siRNA治疗后的HBsAg年下降幅度更大(0.21 vs 0.08 log,p = 0.003)。
年龄与HBsAg最大降幅(r = -0.406,p = 0.003)及LFU时降幅(r = -0.427,p = 0.001)呈负相关。基线qHBsAg水平(OR 0.016,95%CI 0.001 - 0.171)和最低点HBsAg下降log数(OR 16.979,95%CI 3.131 - 92.083)与LFU时HBsAg < 100 IU/mL的患者比例独立相关。
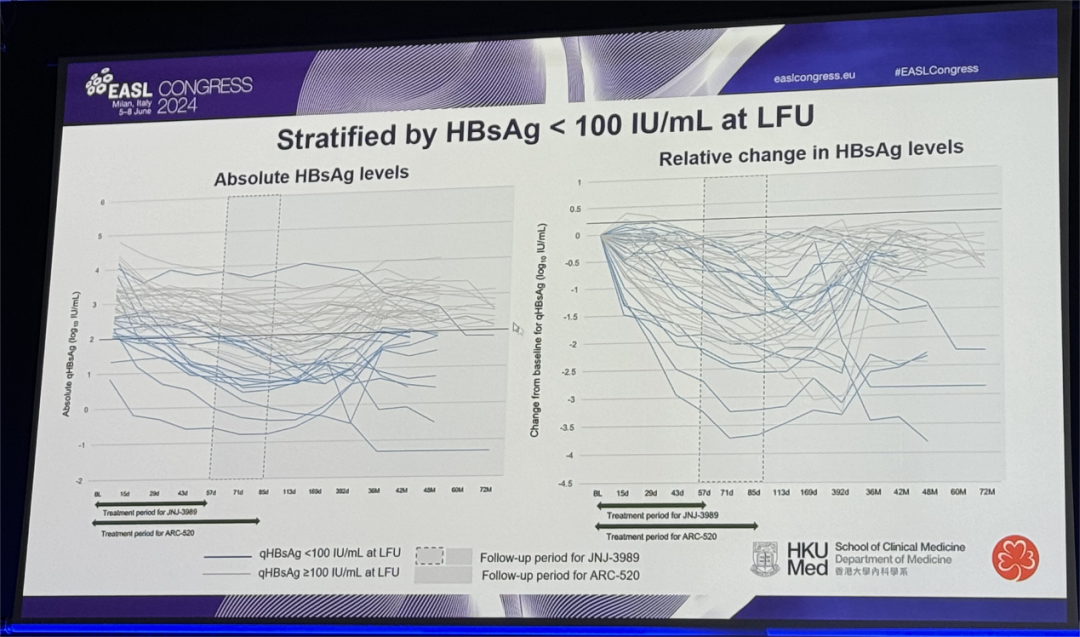
siRNA-100 评分(由基线qHBsAg和最低点HBsAg下降log数得出)为 0、1、2、3 和≥4 的受试者在LFU时实现HBsAg<100 IU/mL的概率分别为100%、80%、66.7%、38.5% 和 0%。
研究结论
由基线qHBsAg和最低点HBsAg下降log数计算得到的siRNA-100评分或可评估末次随访时实现HBsAg < 100 IU/mL的概率。
肝霖君有话说
siRNA药物降低HBsAg效果显著,但单药治疗较少能实现HBsAg清除,目前大部分siRNA都在积极探索联合治疗策略。根据先前研究数据,JNJ-3989联合衣壳抑制剂JNJ-6379并未导致疗效的提高,目前已停止JNJ-6379的开发;本研究中JNJ-3989联合PD-1抑制剂nivolumab也未能明显提高疗效;从现有数据来看,JNJ-3989仅在联合PegIFNα后促进了患者的HBsAg清除。多种新药在联合PegIFNα后也都实现了更高的HBsAg清除率。探索最佳联合疗法将是我们持续面临的挑战。
最大HBsAg降幅与停药后的持久疗效相关,因此,筛选优化能最大程度上抑制HBsAg的新产品对探索最佳联合疗法以及有限疗程后的安全停药也非常重要。
参考文献:
Asselah T, Fung SK, Akhan S, et al. A phase 2 open-label study to evaluate safety, tolerability, efficacy, and pharmacodynamics of JNJ-73763989, nucleos(t)ide analogs, and a low-dose PD-1 inhibitor in patients with chronic hepatitis B-Interim results of the OCTOPUS-1 study. EASL2024, Abstract (OS-033).
Mak LYL, Wooddell C, Lenz O, et al. Long-term hepatitis B surface antigen response after finite treatment with siRNAs ARC-520 or JNJ-3989. EASL2024, Abstract (OS-032).



