【柳叶刀•肿瘤学】IMWG关于多发性骨髓瘤CAR-T治疗和反应评估的共识指南
时间:2024-06-02 18:01:30 热度:37.1℃ 作者:网络
MM的CAR-T治疗指南
BCMA CAR-T细胞疗法是晚期难治性多发性骨髓瘤患者的希望,缓解率可达73%到98%。目前全球已经上市三种BCMA CAR-T产品:Idecabtagene vicleucel (ide-cel)、ciltacabtagene autoleucel (cilta-cel)和伊基奥仑赛注射液(equecabtagene autoleucel,eque-cel)。
CAR-T细胞疗法不同于以往的抗骨髓瘤疗法,具有独特的毒性作用,需要不同的缓解策略。因此,国际骨髓瘤工作组(IMWG)免疫治疗专委会召集涵盖造血细胞移植、细胞治疗和多发性骨髓瘤治疗领域的专家小组撰写共识性指南,旨在协调CAR-T的管理,为患者选择、桥接治疗、清淋、反应评估和一般毒性管理提供广泛建议。
该指南近日发表于《The Lancet Oncology》,第一作者和通讯作者为梅奥诊所Yi Lin教授,中国医学科学院血液病医院(血液学研究所)邱录贵教授作为第二作者参与指南撰写,上海长征医院杜鹃教授是重要撰稿人。

指南建议
患者选择
美国食品和药物管理局(FDA)批准的cilta-cel和ide-cel适用于既往至少接受过4线治疗的患者,而欧洲药品管理局批准的cilta-cel适用于既往至少接受过3线治疗的患者。既往接受3线或≥4线治疗的患者的缓解率和无进展生存期相当,可能是由于药物难治的类别比治疗线数更能预测预后。在考虑CAR-T细胞治疗和使用其他免疫疗法时,使用IMWG标准计算既往治疗线数极为重要(包括针对难治性疾病、复发疾病或因不耐受而开始的新疗法)。
部分疾病和治疗相关特征可阻碍患者接受CAR-T细胞治疗:大包块或进展迅速的疾病可增加单采洗脱期或CAR-T细胞制备期间临床恶化的风险;持续的重度血细胞减少可能影响安全单采和成功制备CAR-T细胞;暴露于大剂量烷基化剂会对外周血淋巴细胞计数和T细胞健康度产生负面影响,从而影响CAR-T细胞制备。尽管具有高危特征的患者(包括存在高危细胞遗传学、髓外病变和晚期患者)对所有常规治疗的临床反应往往较差,但这些患者仍可获益于CAR-T,因此不应予以排除。活动性浆细胞白血病、继发性中枢神经系统受累、肾功能差(肌酐清除率<30ml/min)和继发性淀粉样变性患者被KarMMa-1和CARTITUDE-1研究所排除,因此BCMA CAR-T在这些情况下的安全性仍有待确定。病例报告有成功经验,但进行中的试验将有助于指导这些患者未来的使用。Panel 1总结了患者选择的建议,包括考虑既往治疗、疾病特征和器官功能。

关于CAR-T资格的其他考虑因素,进行了一项专家意见调查,参见下表。
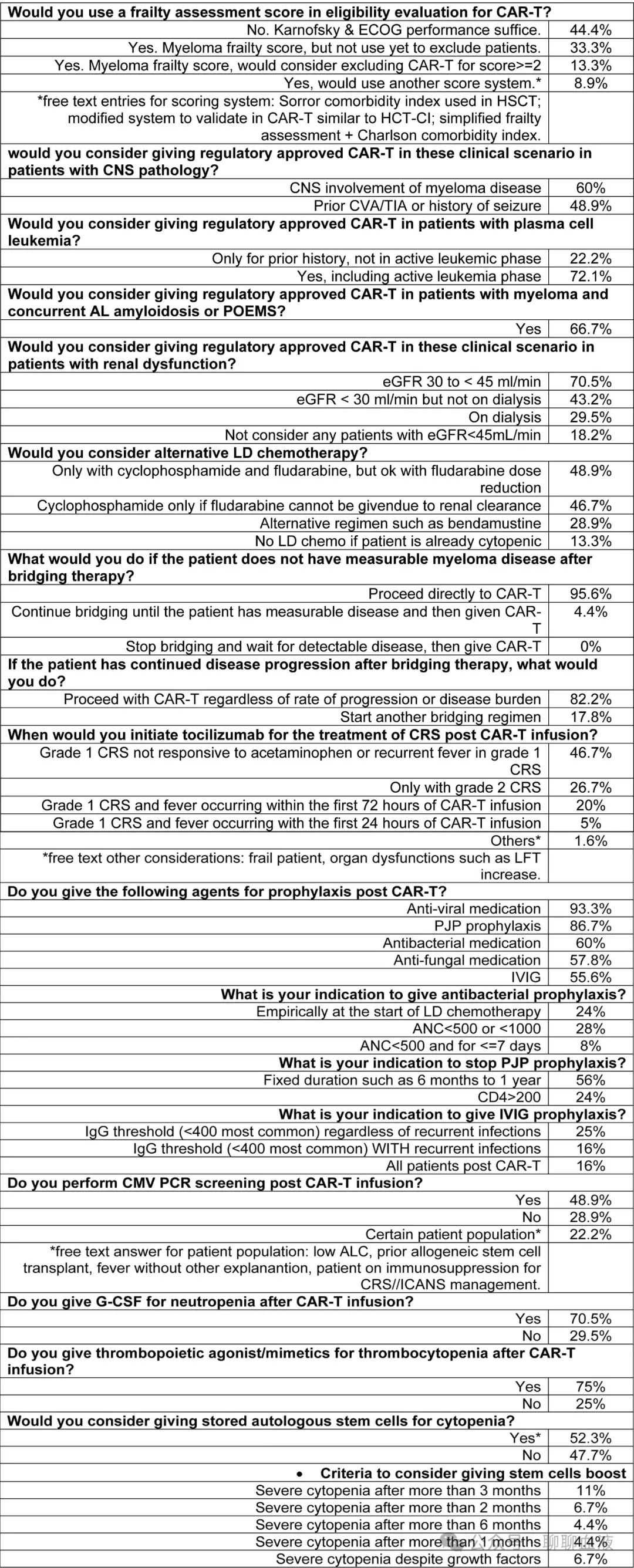
既往治疗
应讨论单采前挽救治疗的选择和时机,因为单采和CAR-T细胞制备前的许多药物会对外周血淋巴细胞计数和T细胞健康度产生负面影响。特别是淋巴细胞抑制剂,如苯达莫司汀、环磷酰胺、美法仑、氟达拉滨和大剂量类固醇,可能在数月的范围内具有长期作用,应在单采前1-2个月甚至更长时间内避免使用。对于常见的抗骨髓瘤药物,2周的洗脱期是标准策略,以允许血细胞计数恢复。对于半衰期短的药物,如低剂量糖皮质激素、免疫调节剂和维奈克拉,停药5个半衰期可能是合理的(即使少于14天)。放疗范围小于骨髓体积的5%时,对有症状的浆细胞瘤进行无洗脱期的限制性放疗是合理的。尽管许多CAR-T的研究排除了先前异基因干细胞移植的患者,但CARTITUDE-1研究成功招募了7例先前进行过异基因干细胞移植的患者,未发生意外毒性或移植物抗宿主病。
尽管CAR-T细胞的制备成功率在所有三个注册研究中都很高,但FDA批准的产品放行规范比临床试验中使用的要更窄,并且在真实世界中制备失败一直存在问题。如果第一次制造失败,可能需要重复单采,如果存在合适的替代方案,应避免使用淋巴细胞抑制剂进行桥接治疗。Panel 1总结了单采前考虑骨髓瘤治疗的建议。
既往BCMA 靶向治疗
在KarMMA-1和CARTITUDE-1研究以及其他早期治疗线(KarMMa-3和CARTITUDE-4)中,入组时不需要评估浆细胞BCMA表达。基于骨髓中BCMA的免疫组化表达情况,临床反应并无差异。而其他BCMA靶向疗法现已上市,它们的使用可能会影响复发时骨髓瘤细胞中BCMA的表达,以及后续BCMA靶向治疗的反应。正在进行的临床试验正在招募既往接受过BCMA靶向治疗的患者,将有助于了解既往BCMA靶向治疗对CAR-T细胞治疗临床结局的影响。
CAR-T治疗后BCMA会出现基因组缺失和功能识别和结合的丧失,应开发临床可用的手段来检测BCMA的基因组和功能损失,以指导后续治疗选择。在缺乏临床可用的检测BCMA缺失的手段的情况下,考虑到BCMA表达通常可以在进展时观察到且随着时间的推移而增加,患者可能会从获益于非BCMA靶向治疗,而非另一种BCMA靶向治疗。
对BCMA T细胞衔接剂(TCE)难治或复发的患者中存在T细胞耗竭,而双特异性抗体后接受一段无治疗期可能有助于改善T细胞的健康度。TCE治疗后使用免疫调节剂、小脑E3连接酶调节药物或抗CD38单克隆抗体是否能改善T细胞功能,还有待探讨。新出现的临床试验数据和实际经验将有助于提供信息,此时是否以及如何考虑BCMA CAR-T细胞治疗。建议同时符合TCE和CAR-T细胞治疗条件的患者首先考虑CAR-T。
重复CAR-T给药
在ide-cel或cilta-cel的研究中,相同的CAR-T细胞重复给药未产生持久的临床缓解。持续缓解患者给予相同CAR-T细胞的额外剂量,其潜在获益尚未确定,有初步结果表明缓解可能有所改善。不建议在复发时使用相同的CAR-T细胞重复治疗,但靶向不同抗原或结合域的CAR-T细胞治疗仍可考虑。
器官功能及合并症
年龄不应限制CAR-T细胞治疗的资格。作为资格标准,心肺健康和虚弱可能更相关,因为患者需要能够耐受CAR-T细胞治疗相关的副作用。推荐的器官功能检查列于Panel 2。

肾功能不全是骨髓瘤的常见并发症。鉴于研究证实氟达拉滨清淋对CAR-T细胞活性的重要性,临床试验中肾脏清除率>45mL/分钟才能减少氟达拉滨的剂量,但不能省略;这些试验排除需要血液透析的患者。美国骨髓瘤免疫治疗联盟(US Myeloma Immunotherapy Consortium)显示,在196例在标准护理实践中接受单采以制备ide-cell的患者中,75%的患者不符合KarMMA研究的条件,最常见的原因为器官功能障碍(28%),其次为肾功能障碍(13%);与之类似,在143例在标准护理实践中接受单采以制备cilta-cell的患者中,57%不符合CARTITUDE-1研究的条件,其中12%的患者由于器官功能障碍。真实世界分析的早期随访显示,尽管真实世界的患者不太fit,但与KarMMa相比的安全性和临床反应相当。然而,国际血液和骨髓移植研究中心(CIBMTR)对821例接受标准治疗的ide-cell患者的分析显示,接受苯达莫司汀的患者的无进展生存期和总生存期明显降低。其他病例报告表明,终末期肾病患者环磷酰胺单药或联合剂量调整的氟达拉滨是安全的。
感染筛查
CAR-T细胞治疗不应用于可能有活动性感染的患者,包括:慢性病毒感染;肝炎和艾滋病毒;巨细胞病毒、EB病毒和细小病毒B19等再激活。开始CAR-T细胞治疗之前应对患者进行以下评估:HIV抗体;乙型肝炎病毒表面抗原、表面抗体、核心抗体;丙型肝炎病毒抗体伴核酸检测(如果有任何检测提示活动性或慢性肝炎)。对于流行地区或既往暴露或感染的患者,筛查巨细胞病毒、细小病毒B19或其他既往感染(包括侵袭性真菌感染、分枝杆菌感染或非典型分枝杆菌感染)可能是合理的。值得注意的是,描述CAR-T细胞在活动性HIV感染患者中成功治疗的病例也有报道。上呼吸道病毒(如SARS-CoV-2)的无症状病毒性心电图不应排除启动CAR-T细胞治疗。无临床感染证据的巨细胞病毒血症应该在单采或CAR-T细胞治疗之前进行治疗。无临床感染证据的EB病毒血症可以进行治疗,但并非单采或CAR-T细胞治疗的禁忌。
转诊问题
获得批准的CAR-T细胞疗法的生产准入受到限制。在美国,许多经过认证的治疗中心每个月只收到很少的制备插槽(manufacturing slots),但有很长的等待名单,而早期转诊(特别是对于患有侵袭性疾病的患者)可以帮助减少等待时间。提供最新的临床信息,特别是进展时间和改变的治疗,可以帮助CAR-T细胞治疗团队维持等待名单和选择患者,并为单采的挽救治疗提供指导。此外,鉴于患者获得护理的机会存在差异,治疗中心应有意识地加强其区域内的社区参与,以改善少数民族和社会经济上处于不利地位的患者的机会。
CAR-T制备期间的治疗
桥接治疗定义为在单采后和清淋化疗前给予的抗骨髓瘤治疗,在KarMMa-1和CARTITUDE-1研究中,超过2/3患者接受了桥接治疗。在等待制备细胞的过程中,疾病控制和避免器官功能障碍是重中之重。尽管在注册研究中,患者在CAR-T细胞制备期间要接受先前的暴露方案,但随后正在进行的CARTITUDE研究允许在桥接期间使用新方案,以减少肿瘤负荷,作为缓解策略的一部分以降低迟发性神经性自身脑炎的风险(包括帕金森)。
对于桥接治疗后无可测量疾病的患者,缺乏表达抗原的骨髓瘤细胞对于CAR-T细胞持久性和有效性的影响仍无结论。一线治疗中开展诱导后给予CAR-T细胞治疗的试验,将产生关于微小到无可测量的疾病情况下CAR-T细胞持久性和有效性的信息。尽管桥接方案可能诱导临床缓解,但CAR-T细胞治疗应尽早给予,并且在患者临床安全时接受治疗,没有必要延迟CAR-T细胞治疗直到桥接治疗达到最深缓解。Panel 1总结了CAR-T细胞制备期间骨髓瘤治疗(桥接治疗)的考虑。
不符合规格的CAR-T产品
不符合规格的CAR-T细胞指产品放行标准规格(多为存活力和CAR+ T细胞数量)超出FDA批准的范围,但符合注册研究中使用的范围。这些产品可以作为扩展使用方案(expanded access protocol)或可控使用方案(managed access protocol)的一部分提供。在从这些方案中获得临床结局之前,有理由认为,不符合规格的CAR-T细胞产品产生类似临床反应的几率很高。但值得注意的是,CAR+ T细胞剂量与ide-cell无进展生存期的增加呈正相关。鼓励提供者与制造商沟通不符合规格的参数、重复制备以满足放行标准的可能性,以及患者进行重复单采(如果需要)或等待重复制备的可能性。在重复单采或制备延迟不可行的情况下,在扩展使用方案或可控使用方案中使用超出规格的CAR-T细胞产品也是合理选择。
清淋化疗
中国最早的cilta-cel临床试验仅使用环磷酰胺作为清淋,但所有三个注册研究都使用环磷酰胺和氟达拉滨。2022年美国出现氟达拉滨短缺,从而提出在CAR-T细胞治疗中省略氟达拉滨或替代清淋方案的问题。部分机构使用苯达莫司汀,但其长期影响尚不清楚。虽然需要进一步研究替代清淋化疗对CAR-T细胞治疗结局的影响,但只要可行,建议使用各自CAR-T说明书中指定的清淋化疗类型,并根据肾功能进行适当调整。
细胞因子释放综合征的管理
细胞因子释放综合征是CAR-T细胞治疗后的常见毒性,美国移植和细胞治疗学会(ASTCT)共识分级系统是评估细胞因子释放综合征分级的标准,但细胞因子释放综合征的管理应考虑到所有可能受影响的器官(Panel 1)。
疾病特征、患者合并症和CAR-T细胞产品设计都会影响细胞因子释放综合征。在骨髓瘤CAR-T细胞治疗的注册研究中,细胞因子释放综合征大多为低级别且可控。虽然有单独的风险评估和缓解系统(Risk Evaluation and Mitigation System,REMS;FDA可以要求某些具有严重安全问题的药物确保药物的获益大于风险,旨在加强药物使用行为和行动,以支持药物的安全使用),但每种CAR-T细胞产品都可能成为行政负担。细胞因子释放综合征干预的研究经验,特别是考虑到三线药物(如anakinra),将提供信息以确保在实践中使用CAR-T细胞治疗时具有类似的安全性。目前的数据支持使用托珠单抗治疗2级细胞因子释放综合征,或1级细胞因子释放综合征伴早发或快速进展或持续时间超过72小时。托珠单抗和类固醇的使用不影响治疗反应,因此应考虑在细胞因子释放综合征早期进行干预,以优化疾病负荷较高的患者和因合并症而虚弱的患者的安全性。早期开始细胞因子释放综合征治疗可以帮助减少免疫效应细胞相关神经综合征(ICANS)的可能性。目前没有数据支持使用预防性细胞因子阻断来管理骨髓瘤CAR-T细胞治疗后的细胞因子释放综合征。
免疫效应细胞相关噬血细胞性淋巴组织细胞增生症样综合征
噬血细胞淋巴组织细胞增多症和巨噬细胞活化综合征是CAR-T治疗后罕见但高度致命的并发症,可在细胞因子释放综合征期间或消退后升级为不受控制的过度炎症。噬血细胞淋巴组织细胞增多症和巨噬细胞激活综合征的发生率约小于8%,但考虑到体征和症状与细胞因子释放综合征重叠,CAR-T细胞相关噬血细胞淋巴组织细胞增多症和巨噬细胞激活综合征的诊断具有挑战性。2023年ASTCT提出了定义免疫效应细胞相关噬血细胞性淋巴组织细胞增生症样综合征(IEC-HS)的统一标准,以更好地描述其在不同CAR-T细胞疗法中的发病率(见于Hines MR, Knight TE, McNerney KO, et al. Immune effector cellassociated hemophagocytic lymphohistiocytosis-like syndrome.Transplant Cell Ther 2023; 29: 438.e1–16.)。尚无相关管理指南,但专家意见建议IL-6抑制剂序贯糖皮质激素后再给予额外的细胞因子抑制剂(如anakinra)和靶向治疗(如芦可替尼)。Emapalumab是一种干扰素抗体,已获FDA批准用于原发性噬血细胞淋巴组织细胞增多症,最近有报道用B细胞急性淋巴细胞白血病的儿童IEC-HS。考虑到混杂的并发症(如感染和血细胞减少),IEC-HS的管理极具挑战性;因此,在高度怀疑的情况下,建议在完全符合噬血细胞淋巴组织细胞增多症诊断标准之前进行早期干预。如果患者已经接受IL-6抑制剂和类固醇作为细胞因子释放综合征管理的一部分,或者这些干预措施没有改善,建议使用影响髓系通路的药物,包括anakinra和芦可替尼。此外,如果有CAR-T细胞扩增或持续存在的证据,应考虑使用环磷酰胺或抗胸腺细胞球蛋白等淋巴细胞抑制剂。
ICANS的管理
神经毒性是另一种常见的CAR-T细胞治疗相关副作用,但对其作用机制的认识劣于细胞因子释放综合征。血脑屏障破坏与内皮细胞的激活之间存在关联。有报告发现1例患者中枢神经系统中表达BCMA。最常见的神经毒性发生于细胞因子释放综合征期间。早期体征和症状包括注意力下降和找字困难,进而发展为语言障碍、失语、思维混乱和失写症;癫痫发作和脑水肿也罕见发生。ICANS的ASTCT共识分级指南是目前的标准,相关管理建议总结于Panel 1。
尽管骨髓瘤各CAR-T研究报告的神经系统症状类型有所不同(包括使用不同的分级系统),但ICANS的具体表现通常为低级别和可逆,脑水肿的总体报告率很低。但需要注意的是,在CARTITUDE-1研究中,cilta-cell报告了细胞因子释放综合征消退后的迟发非典型神经功能缺陷。此外脑神经麻痹、帕金森氏症和Guillain–Barré综合征也有报道。中国另一项使用相同CAR结构的研究(LCAR-B38M)未报告类似的神经学结果。为了解延迟性神经毒性的发生率和临床过程,需要对正在进行的CARTITUDE研究中更大的人群进行随访,但危险因素似乎包括高级别细胞因子释放综合征、既往ICANS、高肿瘤负荷和CAR-T细胞的快速扩增。随后的CARTITUDE研究使用了缓解策略,包括早期和积极治疗细胞因子释放综合征和改善血细胞减少,以减少肿瘤负荷,目前似乎已将帕金森病的发病率从6%显著降低到1%,但在CARTITUDE-2中仍有1例患者出现面神经麻痹,而CARTITUDE-4中有16例(9.1%)。
虽然IL-6抑制剂可用于缓解ICANS期间的细胞因子释放综合征,但地塞米松最常用作初始治疗,因其渗透中枢神经系统且副作用低。使用托珠单抗阻断IL-6受体可能会增加ICANS风险,可能是由于增加循环血清IL-6。ICANS也可能在不使用地塞米松的情况下自行消退。谨慎监测和检测癫痫发作和脑水肿极为重要,识别癫痫发作后需要增加类固醇和抗癫痫药物的使用。同样,考虑到快速恶化和高死亡率的风险,脑水肿应在ICU密切监测颅内压并升级治疗。通常使用大剂量甲泼尼龙。IL-1通路抑制剂anakinra也广泛使用,而淋巴细胞抑制剂(如环磷酰胺和抗胸腺细胞球蛋白)可用于难治性患者。
血液学毒性的管理
尽管细胞因子释放综合征和神经毒性最受关注,但血液毒性普遍发生于CAR-T细胞治疗中,需要积极的支持治疗。血液学毒性的病因包含多种因素,包括先前的骨髓瘤治疗、先前存在的克隆造血、清淋化疗、细胞因子释放综合征及其管理药物,以及感染。重度中性粒细胞减少症、贫血、血小板减少症和白细胞减少症的发生率通常>50%,现在称为免疫效应细胞相关血液毒性。血细胞计数延迟恢复很常见,恢复正常通常需要6-12个月。因此,在CAR-T细胞治疗后的前6-12个月,需要密切监测血液学恢复并持续支持治疗,包括生长因子和输血治疗。CAR-HEMATOTOX评分可以在清淋化疗前识别免疫效应细胞相关血液毒性的危险因素,目前正在评估该评分以指导未来基于风险的管理。
血细胞减少和支持治疗的建议
由于接受CAR-T细胞治疗的患者普遍存在血细胞减少,因此在重度贫血和血小板减少症发病时,应根据机构指南提供密切的血细胞计数监测和血液制品支持。在大多数试验中,在细胞因子释放综合征危险期或活动性细胞因子释放综合征或ICANS期避免使用生长因子支持治疗,其使用可能会加重急性毒性或炎症,或可能促进巨噬细胞激活综合征样症状。有数据表明,在治疗过程中早期使用粒细胞集落刺激因子可能是安全的,不会产生不良反应。在细胞因子释放综合征危险期后(通常在第14天之后),以及出现延迟或迟发性血细胞减少的患者,应考虑使用生长因子。同样,根据机构指南,对于长期和重度贫血或血小板减少症,可以考虑使用促红细胞生成剂和促血小板生成剂。
自体干细胞支持治疗(Autologous stem-cell boost)(无预处理化疗)似乎对长期重度血细胞减少患者的血细胞计数恢复有效。19例患者在CAR-T细胞输注后中位53天给予中位剂量2.75×106 CD34+干细胞/kg(无预处理化疗),植入成功率为95%。作为预防措施,对于早期接受CAR-T细胞治疗的患者和尚未储存干细胞的患者,应考虑在单采后收集和储存自体干细胞。
感染
感染在接受CAR-T治疗的患者中很常见。感染和病原体的类型根据CAR-T细胞治疗的四个不同阶段而变化(图)。肺孢子虫肺炎已有报道,主要发生于CAR-T细胞治疗后早期(90天)停止预防的患者。临床显著的病毒再激活也有报道,包括巨细胞病毒、EB病毒和细小病毒B-19,但发病率也很低,很少有巨细胞病毒血症合并终末器官疾病的报道。
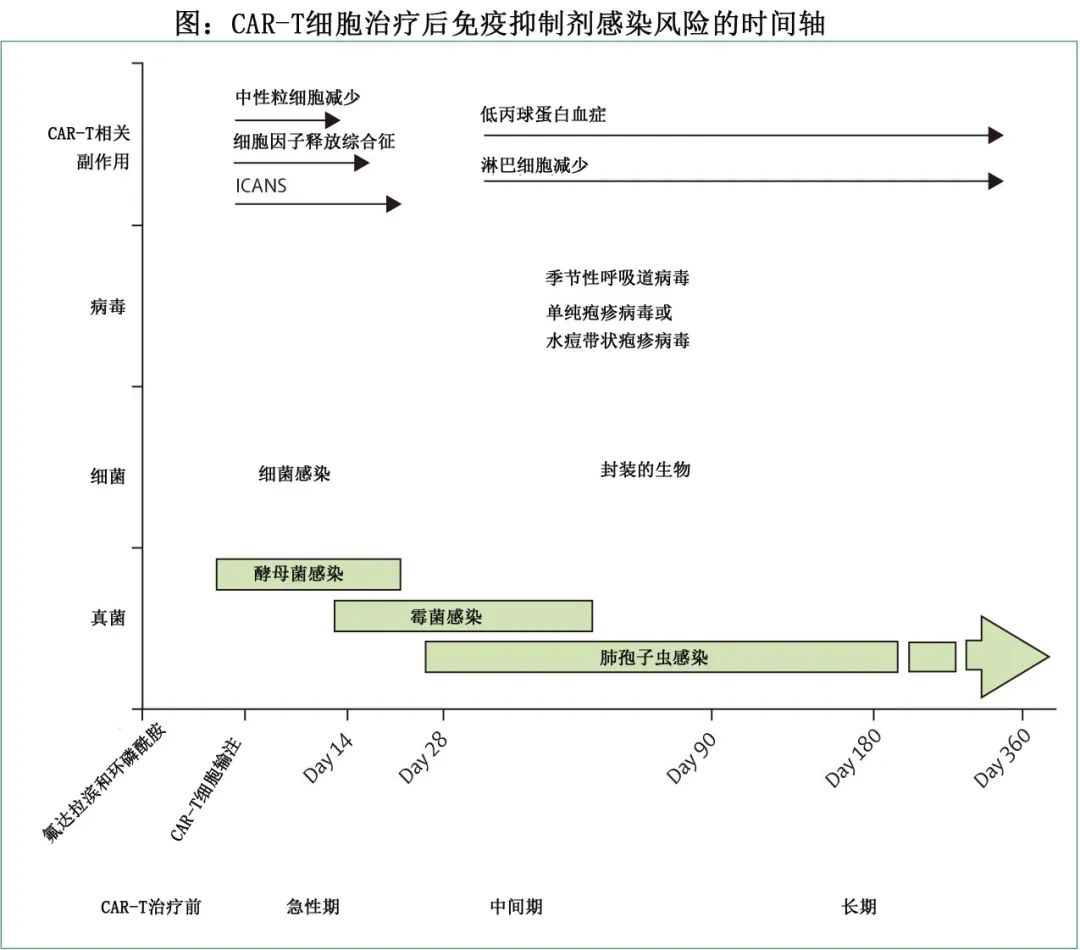
Panel 3总结了导致感染风险较高的特征。晚期感染罕见,但可发生于显著和长期的淋巴细胞减少和低丙球蛋白血症的患者。

急性感染
发热伴细胞因子释放综合征常与中性粒细胞减少症一起发生,患者需要密切监测并积极治疗可能的感染,应继续按照机构指南管理中性粒细胞减少性发热。控制细胞因子释放综合征和ICANS的药物可以掩盖发热,应持续进行谨慎的感染监测。应考虑经验性使用抗病毒药物或霉菌活性的抗真菌治疗。机会性感染风险最高的患者可考虑筛查病毒再激活(巨细胞病毒、细小病毒和EB病毒)和机会性感染(肺孢子菌肺炎和水痘带状疱疹病毒),病毒再激活的治疗应以机构方案为指导。还应考虑使用生长因子和丙种球蛋白替代治疗。
抗菌预防
对于免疫功能低下的宿主,抗菌预防是预防感染的主要手段。表1总结了接受BCMA CAR-T细胞治疗的复发或难治性多发性骨髓瘤患者中预防最常见感染的建议。由于感染的发生率和类型可能因地区和使用的CAR-T细胞产品而异,因此应酌情使用机构实践来补充这些指南。
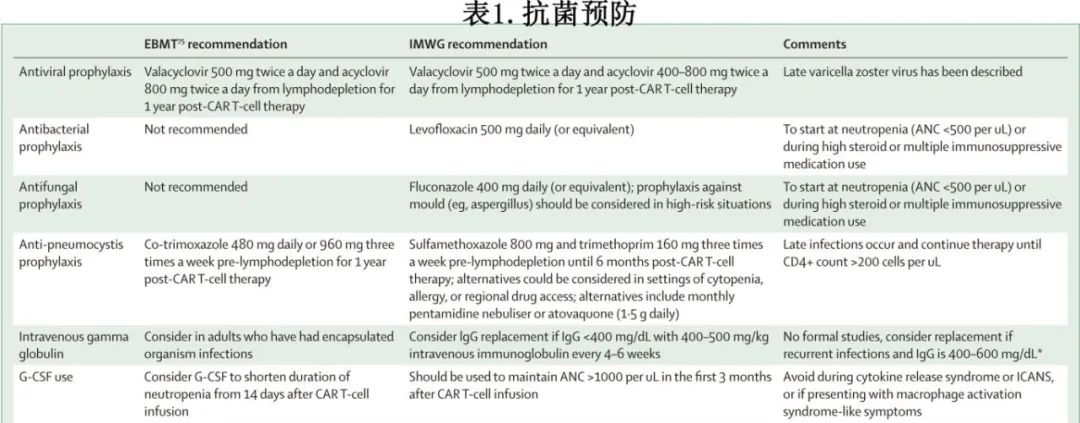
免疫球蛋白替代治疗
由于缺乏临床试验数据,使用免疫球蛋白治疗(静脉注射或皮下免疫球蛋白)尚争议,但对于重度低丙球蛋白血症 (IgG<400 mg/dL)或中度低丙球蛋白血症(IgG 400-600 mg/dL)伴复发性或重度感染的患者,可以考虑使用免疫球蛋白替代治疗。对于IgG骨髓瘤患者,Hevylite检查或总IgG水平减去单克隆蛋白(M蛋白)可用于估计非骨髓瘤IgG水平,以考虑静脉注射免疫球蛋白替代治疗。治疗可以在CAR-T细胞治疗前开始,并至少在CAR-T治疗后的前3-6个月持续治疗,目标为IgG水平维持在400mg/dL以上。复发性感染患者应遵循静脉注射免疫球蛋白替代治疗的机构指南。
疫苗注射
指导接受CAR-T治疗的多发性骨髓瘤患者的疫苗接种策略尚缺乏数据,BCMA CAR-T细胞治疗对体液免疫的长期影响也尚未得到很好研究。然而,低丙球蛋白血症常见于BCMA CAR-T治疗后,并可持续6-12个月或更长时间。也有患者在CAR-T细胞治疗后1年的骨髓样本中检测到很少或没有浆细胞。因此,在为接受CAR-T细胞治疗的患者制定正式疫苗接种指南之前,还需要进一步研究。部分中心已经开始按照干细胞移植的指南为CAR-T治疗患者接种疫苗。在获得进一步的数据之前,应避免使用活疫苗。可按照机构指南在CAR-T细胞治疗前后接种疫苗,特别是流感和呼吸道合胞病毒等高危呼吸道感染的疫苗。
关于COVID-19疫苗,部分接受CAR-T细胞治疗的患者接受RNA疫苗接种,但疫苗的疗效尚未得到严格研究。许多中心目前正在监测抗COVID-19刺突蛋白抗体和细胞介导反应的存在。需要注意的是,没有关于COVID-19疫苗接种后疑似危害的报告,各中心建议在CAR-T细胞治疗后最早1个月接种COVID-19疫苗。不同的COVID-19疫苗在接受CAR-T细胞治疗的患者中的最佳时机和临床效果尚不清楚。
反应评估
IMWG提出了一种统一的方法来评估多发性骨髓瘤患者接受CAR-T细胞治疗的反应。由于CAR-T的独特后勤状态,以及为了对所有接受CAR-T细胞治疗的多发性骨髓瘤患者的反应评估进行协调,更新和明确的标准很有必要。
建议的评估
CAR-T细胞治疗在后勤方面与自体干细胞移植治疗相似,因此,干细胞移植反应评估的一些原则也可用于CAR-T。
治疗标准应当是,医生并不拘泥于只使用以前使用过的桥接方案,也可以使用新的、可能具有更高抗肿瘤活性的桥接治疗方案,以使患者在开始清淋化疗前即达到完全缓解;随着CAR-T细胞疗法用作一线巩固治疗的一部分,未来这一现象可能会更常见。目前在临床试验中,在CAR-T细胞输注之前获得完全缓解的患者认为无法评估反应,作者建议将这些患者纳入疗效评估。基线评估应在疾病可测量时进行,即在诊断时(CAR-T作为一线治疗的一部分)、复发时(单采前)和开始计划的桥接治疗时。
基线评估见表2。反应评估应在整个治疗过程中进行,并使用基线值来量化反应。
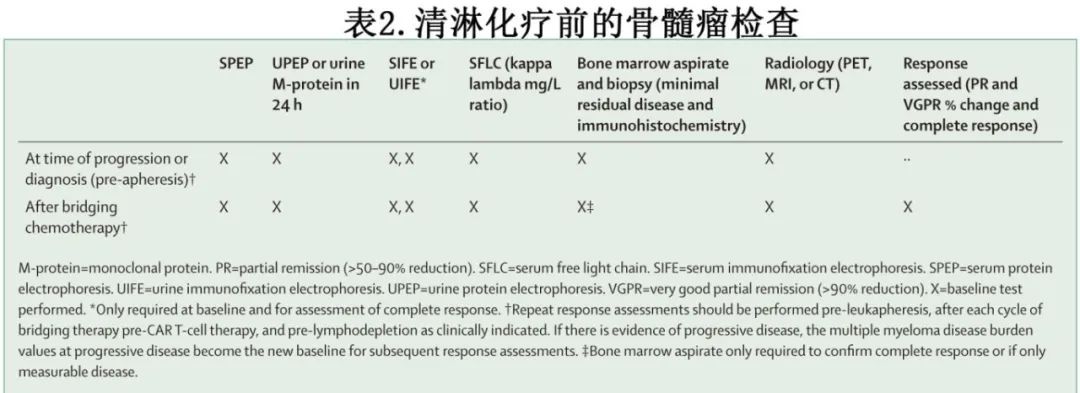
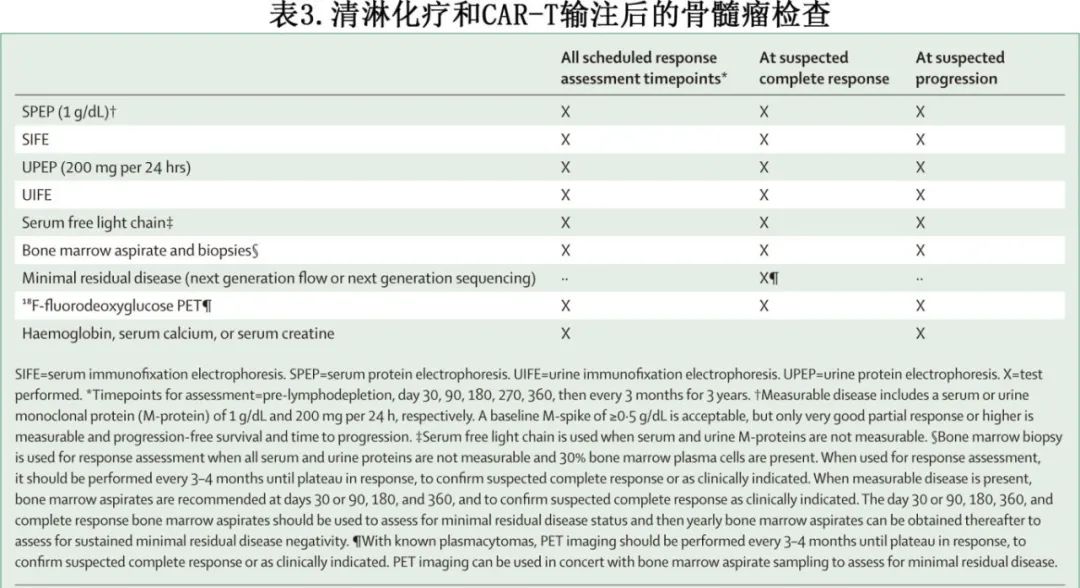
推荐的CAR-T细胞治疗后评估如表3所示,其中包括可接受的最低检测频率,且治疗机构可能会更频繁地进行评估。一般来说,血液和尿液M蛋白的评估,包括血清蛋白电泳、血清免疫固定电泳、血清游离轻链、尿蛋白电泳和尿免疫固定电泳应在第30、90、180、270和360天进行,此后至少每3个月进行一次。在CAR-T细胞治疗后,建议在第30天或第90天、第180天、第360天以及任何时间点进行骨髓活检和穿刺,以确认临床指示的完全缓解,此后每年进行连续微小残留疾病(MRD)监测。在骨髓取样时,MRD检测可用于评估获得≥非常好的部分缓解的患者。放射学评估(包括PET-CT、MRI或负重CT扫描)可能需要评估有软组织髓外病变证据的患者的反应。软组织髓外病变的患者应在基线和至少在大约90、180、270和360天进行放射学评估,以确认完全缓解或临床指征的疾病进展。对于完全缓解的髓外病变,PET-CT、MRI或负重-CT计划应配合骨髓穿刺和活检进行MRD监测。每个反应级别的标准遵循应统一的IMWG反应标准。
生存(Time-to-event)的定义
为CAR-T细胞治疗提供统一的生存定义很重要,这些终点已在先前的临床试验指南中进行定义,但对于接受CAR-T细胞治疗的患者需要修改这些定义。这些定义应该是一致的,无论CAR-T细胞治疗的临床情况如何(即,一线治疗、早期复发和大于四线治疗)。建议的定义见Panel 4。

实践的考虑
关于CAR-T细胞治疗的反应评估,必须强调几个实际要点。首先,接受CAR-T细胞疗法治疗复发或难治性多发性骨髓瘤的患者可能具有很强的侵袭性,因此有必要在CAR-T细胞输注前进行一系列疾病评估,以确保有代表性的基线疾病评估并辅助桥接管理。CAR-T细胞输注后,游离轻链(FLC)清除可以迅速发生,并且通常先于M蛋白清除,因此无法计算FLC比率。它是长期无进展生存期的预后因素,因此可能与严格意义的完全缓解伴正常血清FLC比率相似。复发或难治性多发性骨髓瘤患者更有可能在CAR-T细胞治疗前发生髓外病变,或在CAR-T细胞治疗后发生髓外疾病复发,因此建议按系列计划持续进行影像学监测(表3)。
第二肿瘤
在KarMMa-3研究中, ide-cell治疗组13例(6%)患者和对照组6例(5%)患者在短随访期内发生第二肿瘤;13例患者中9例(69%)为侵袭性癌症(实体瘤比血液肿瘤略常见),而4例(31%)为非侵袭性皮肤癌。在CARTITUDE-4研究中,cilta-cell治疗组的9例(4%)患者和对照组的14例(7%)患者发生第二肿瘤;在9例患者中,3例(33%)为血液系统恶性肿瘤,包括急性髓系白血病、骨髓增生异常综合征和外周T细胞淋巴瘤各1例。CAR-T细胞治疗后应遵循适合年龄的所有肿瘤筛查指南。
2023年11月28日,FDA宣布对其已批准的所有六种CAR-T细胞疗法(包括B细胞急性淋巴细胞白血病、淋巴瘤和骨髓瘤)相关的T细胞淋巴瘤风险进行评估。初步分析表明,17700例(0.068%)B细胞恶性肿瘤和多发性骨髓瘤输注后发生12例T细胞淋巴瘤。CAR+的T细胞淋巴瘤病例数尚未报道,但已知有一例为cilta-cell。在评估CAR-T细胞治疗的风险与获益时,应与患者讨论该风险,并使用最新数据。
未来方向
许多正在进行的临床试验正在研究将ide-cel和cilta-cel用于一线治疗,此外多个异基因CAR-T细胞临床试验作为潜在的现成选择也在测试中。目前来说,尽管CAR-T细胞的持久性和缓解的持久性仍有挑战,但安全性表面没有严重的移植物抗宿主病。快速制备的CAR-T细胞(FasT CAR-T、GC012F和PHE885)是改善患者获得治疗的更有希望的策略,值得注意的是,这些细胞在功能上似乎比目前的传统CAR-T细胞更fit和有效。在西班牙的一项研究中,使用ARI0002H CAR-T的细胞疗法也证明了床旁(point-of-care)制备的可行性。靶向其他表面抗原(如GPRC5D、双BCMA和CD19)的CAR-T细胞疗法也在临床试验中。
参考文献
Lin Y, Qiu LG, Usmani S,et al.Consensus guidelines and recommendations for the management and response assessment of chimeric antigen receptor T-cell therapy in clinical practice for relapsed and refractory multiple myeloma: a report from the International Myeloma Working Group Immunotherapy Committee.Lancet Oncol. May 28, 2024DOI:https://doi.org/10.1016/S1470-2045(24)00094-9


