乐普生物ADC药物MRG003治疗复发/转移性鼻咽癌获美FDA授予快速通道资格,86.2%疾病控制率!
时间:2023-12-07 14:37:44 热度:37.1℃ 作者:网络
2023年12月4日,乐普生物自主研发的靶向EGFR的抗体偶联药物(ADC)注射用MRG003获得美国食品和药物监督管理局(FDA)授予快速通道资格(FTD),用于治疗复发/转移性鼻咽癌(NPC)。
此前,2022年9月21日,国家药监局药品审评中心(CDE)官网公示,注射用MRG003拟纳入突破性治疗品种,拟定适应症为:既往经至少二线系统化疗(包括含铂化疗)和PD-1(L1)抑制剂治疗失败的复发/转移性鼻咽癌。
MRG003是一种由EGFR靶向单抗与强效的微管抑制有效载荷MMAE分子通过vc链接体偶联而成的ADC,其以高亲和力特异性地结合肿瘤细胞表面的EGFR,通过内吞进入肿瘤细胞后释放强效的有效载荷,从而导致肿瘤细胞死亡。
EGFR高表达于结直肠癌、肺癌、头颈癌等多种恶性实体瘤中,89%晚期鼻咽癌存在EGFR表达。因此,EGFR是癌症治疗的重要靶点之一。乐普生物表示,MRG003是我国进度领先的靶向EGFR的ADC,处于临床研究阶段,有望抢占市场机遇。
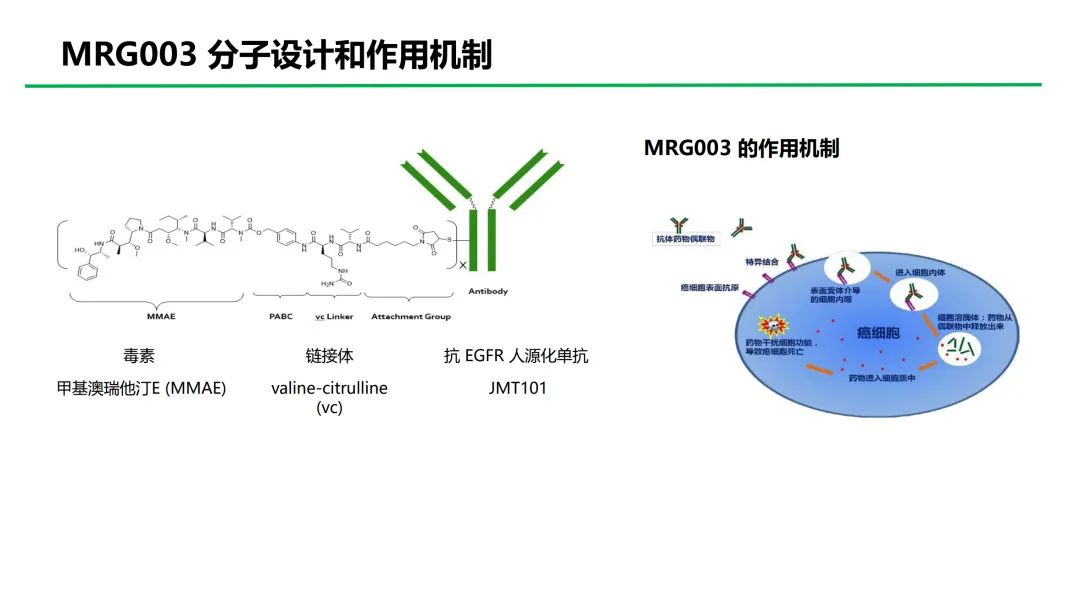
图注:靶向EGFR的ADC药物MRG003分子设计和作用机制
代号:MRG003
靶点:EGFR
厂家:乐普生物
临床数据
在2022年11月5-12日期间召开的第二十五届全国临床肿瘤学大会暨2022年CSCO学术年会上,中山大学肿瘤防治中心韩非教授发布了由徐瑞华教授领衔的MRG003治疗复发/转移鼻咽癌的多中心Ⅱ期临床研究(MRG003-005)结果。
在这项开放、非随机、多中心Ⅱ期临床研究中,主要评估了MRG003治疗既往至少经一线含铂方案和PD-1抑制剂系统治疗期间、治疗后或不耐受的复发/转移性鼻咽癌患者的疗效与安全性。研究的主要评价指标是客观缓解率(ORR);次要评价指标包括疾病控制率(DCR)、疾病缓解持续时间(DOR)、无进展生存期(PFS)、总生存期(OS)、安全性、药代动力学参数和免疫原性。
截止2022年6月8日,共入组了61例中国患者,其中2.0mg/kg剂量组30例,2.3mg/kg剂量组31例。入组患者的既往系统中位治疗线数为2线,均接受过含铂+PD-1方案,约90%的患者接受过放疗。
研究结果显示,在有效性分析集的患者(n=57)中,总体ORR为47.4%,DCR为79.0%,3个月DOR率为90%;在2.0mg/kg剂量组(n=28)中,ORR为39.3%,DCR为71.4%;在2.3g/kg剂量组(n=29)中,ORR为55.2%,DCR为86.2%。
亚组分析显示, 96.5%的患者EGFR表达量为1+及以上,无论肿瘤组织EGFR表达量高低,MRG003均取得了良好的疗效。
在安全性方面,MRG003表现出良好的安全性和耐受性,不良事件多为1~2级,未见治疗相关死亡,整体安全可控。
小结
综上所述,在复发/转移性鼻咽癌患者中,MRG003表现出良好的临床疗效和安全性。MRG003此次获得美FDA授予快速通道资格,意味着有机会通过各种形式加快评审进程,期待早日上市造福更多晚期癌症患者。
参考来源:
https://www.lepubiopharma.com


