【佳作推荐】日本药企Chugai Pharmaceutical JACS论文:有望成为类药五原则升级版的类药环肽开发新标准
时间:2023-11-28 12:29:46 热度:37.1℃ 作者:网络
细胞内很多信号通路通过蛋白-蛋白相互作用(Protein-Protein Interactions, PPIs)发挥作用,通常涉及大而平坦且疏水的结合表面,相比于主流的小分子和抗体,中等尺寸环肽能够更好地适用于细胞内以及缺乏小分子结合深腔的靶点。它们通常比传统的小分子更大,分子量在1000-2000g/mol,并且可以在其分子的一小部分表现出抗体样的结合亲和力和特异性。这也是大环多肽抑制剂能表现出高选择性、较少脱靶副作用的理论根据。环肽也能保持许多理想的小分子特性,如低免疫原性和抵抗蛋白水解降解等。
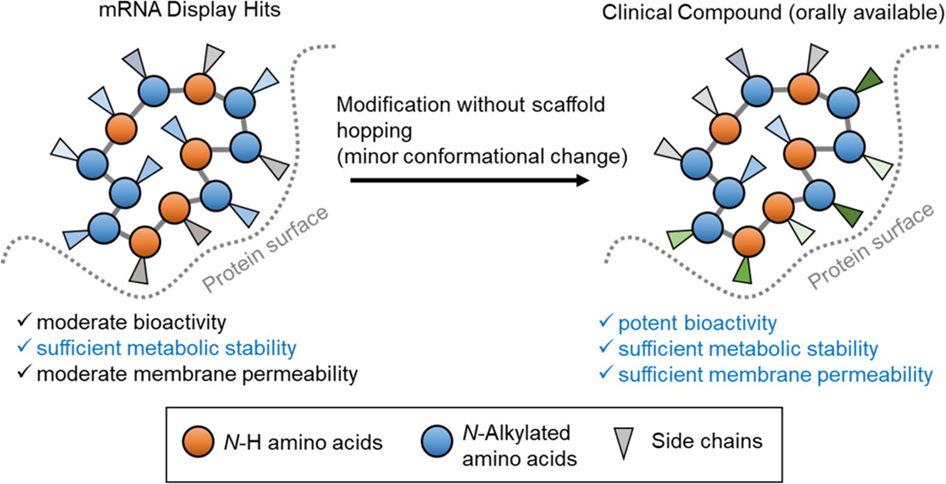
然而,当前除了Lipinski类药五原则(Rule of Five)之外,人们对于分子量大于500g/mol中等尺寸环肽的类药性缺乏系统性的认知。因此,目前筛选得到的多肽类先导化合物往往在类药性方面表现不佳,在后续经历漫长类药性优化的过程中,存在活性丧失的风险。中外制药株式会社(以下写作中外制药)针对这一问题,通过详细阐述类药环肽的结构特征和理化性质,系统性总结环肽类药性的潜在参考标准,对多肽药物研发者有一定借鉴意义。中外制药通过其构建的环肽文库成功地针对细胞内一度被称为不可靶向靶点KRAS设计获得了具有强效口服可行性的环肽。近日,该项研究工作发表在美国化学会出版的Journal of the American Chemical Society期刊(J. Am. Chem. Soc. 2023, 145 (44), 23891-24436)。
首先,为了避免对骨架进行大幅修改,就能获得足够的生物活性和药物相似性,作者参考已上市药物环孢素(Cyclosporine)的结构特征,设计并合成了环肽文库(见图1)。作者的研究旨在探讨环孢素是否在类药性方面为特例,以及如果不是特例,是否存在一些肽特有的结构特征,使其具备类药性。文库中的环肽由天冬氨酸侧链的N端胺和羧酸或其C端衍生物连接而成。总体上该文库具有如下多样性分布:氨基酸残基8−12个、N-烷基化0−8个、Clog P为4.4-15.2、羟基0或1个、分子量为845-1499 g/mol。
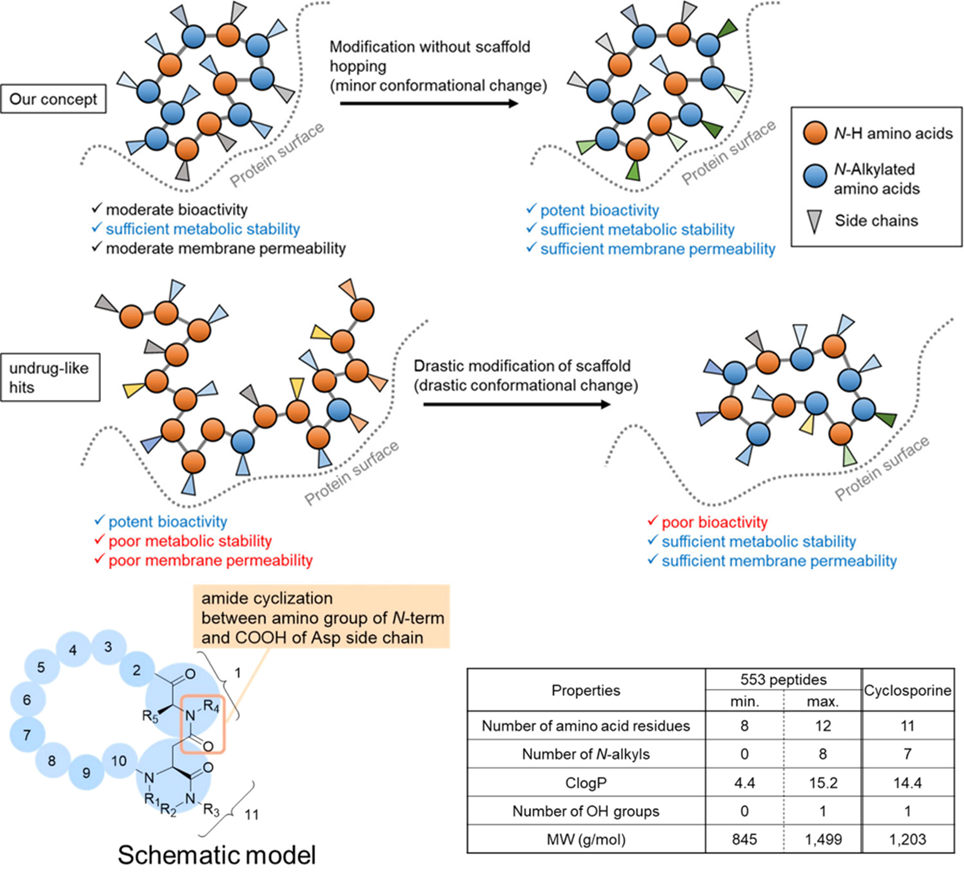
图1、环肽先导化合物的设计思路及文库构建
本文将“类药性”定义为可接受的代谢稳定性和膜渗透性,并分别用体外肝微粒体实验和Caco-2渗透性实验对文库中的肽进行评估。初步评估表明,含有11个残基的环肽符合类药性标准的比例最高。此外,作者进一步发现,Clog P大于12.9和N-烷基化多于6个对类药性具有显著贡献(见图2)。在极性和带电基团方面,研究结果表明,存在3个羟基或一个带电基团会显著降低环肽的膜渗透性。最终,作者证实了上述筛选得到的类药环肽确实具有较好的口服生物可及性和体内分布,从而强化了前述结论的可靠性。
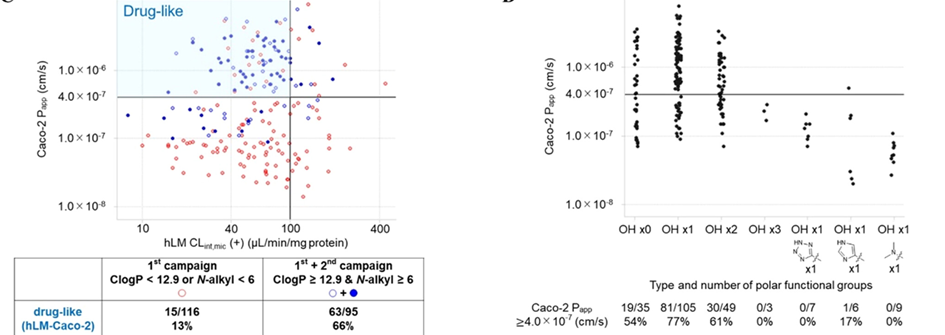
图2、不同结构特征环肽类药性评估
对上述类药肽的研究表明,这些类药肽需要具备不同于已报道的环肽库中肽的特征,例如高度烷基化、酰胺环化、强烈的疏水性、适当的肽长度以及受限的侧链极性等。换言之,优异类药性的环肽文库与已有的环肽建库方法存在显著差异。基于这一认识,作者设计构建体外翻译体系(In Vitro Translation, IVT)以期望获得具有良好类药性的环肽。这需要解决两个问题,其一是N-烷基化氨基酸的连续插入。通过对比,作者最终采用了pCpA方法而非pdCpA法(原因见图3ABC),并通过对每个氨酰tRNA合成酶进行突变,将N-烷基化氨基酸的连续插入效率提高至80%以上。其二是实现代谢稳定的成环策略。作者通过采用还原脱除正交保护基以及类似于天然化学偶联(Native Chemical Ligation,NCL)的成环反应(见图3D),成功解决了上述问题。
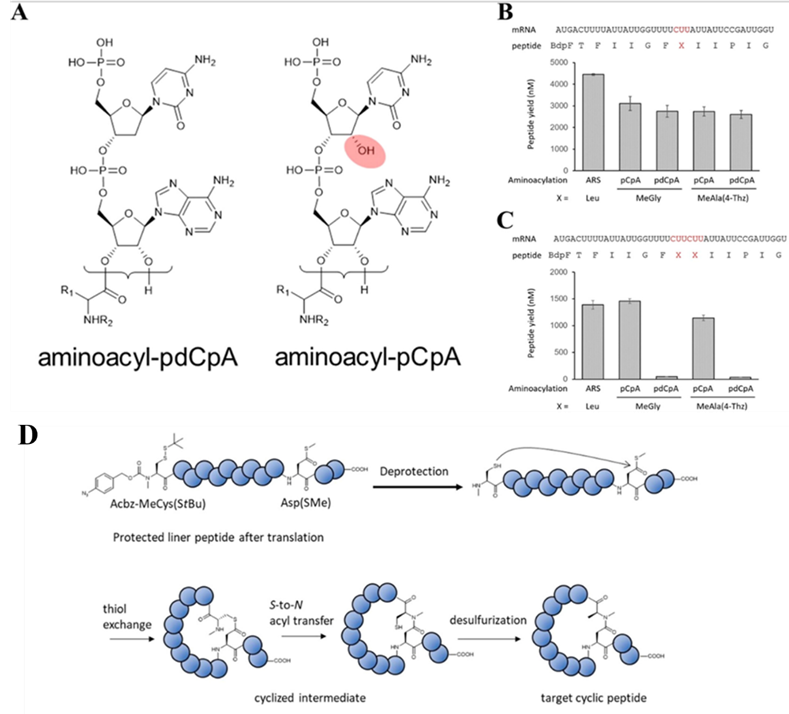
图3、特征环肽库构建策略
利用上述IVT体系,作者建立了具有良好类药性的mRNA展示文库,并以KRAS为模型蛋白进行筛选。所得环肽与KRAS的亲合力为0.3-2.9 μM,其中,先导化合物AP8784对KRAS与SOS1之间的PPI表现出良好的抑制效果,IC50值为180 nM(见图4)。
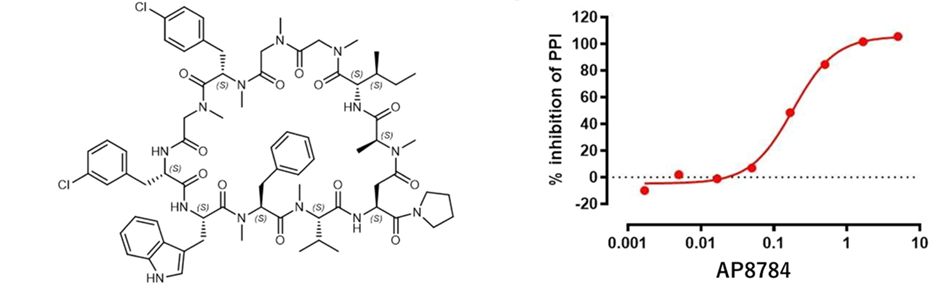
图4、先导化合物AP8784结构及抑制活性数据
最后,作者对AP8784进行了一些结构优化,得到了活性更优的化合物LUNA18(见图5)。LUNA18对各种KRAS突变体均具有超强的亲和力,KD最低可达31 pM。对于多种KRAS-G12X突变的癌细胞系,LUNA18亦表现出nM的抑制效果。
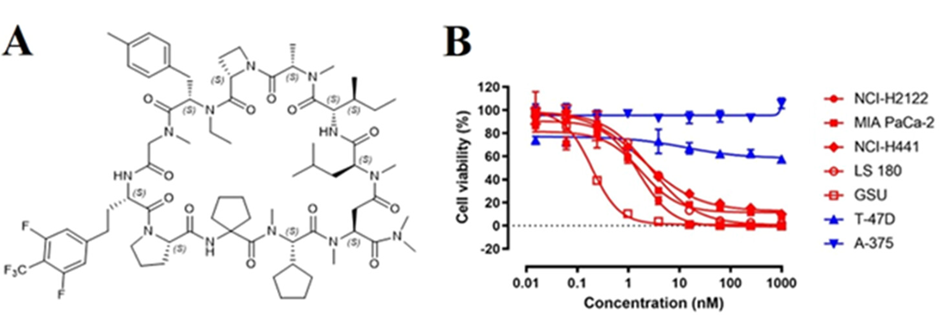
图5、化合物LUNA18结构及细胞活性数据
小结:综上所述,通过文库分析,作者详尽阐明了类药环肽的结构特征和理化性质,为类药环肽的开发提供了新的参考数据。在此基础上,作者成功建立了一种具有较高类药性环肽的mRNA展示技术。最终在针对细胞内靶点KRAS的研究中,发现了活性优异的先导环肽AP8784,并通过改良获得了具有强效可口服的环肽LUNA18。根据文中的药代动力学数据,小鼠、大鼠、犬、猴均表现出低清除率,进一步改善吸收可能有望提高生物利用度。这些结果表明,LUNA18这种环肽具有成为口服药物的治疗潜力。目前,LUNA18正在日本和美国开展一期临床试验。
参考文献
【1】Atsushi Ohta*, Mikimasa Tanada, Shojiro Shinohara, Yuya Morita, Kazuhiko Nakano, Yusuke Yamagishi, Ryusuke Takano, Shiori Kariyuki, Takeo Iida, Atsushi Matsuo, Kazuhisa Ozeki, Takashi Emura, Yuuji Sakurai, Koji Takano, Atsuko Higashida, Miki Kojima, Terushige Muraoka, Ryuuichi Takeyama, Tatsuya Kato, Kaori Kimura, Kotaro Ogawa, Kazuhiro Ohara, Shota Tanaka, Yasufumi Kikuchi, Nozomi Hisada, Ryuji Hayashi, Yoshikazu Nishimura, Kenichi Nomura, Tatsuhiko Tachibana, Machiko Irie, Hatsuo Kawada, Takuya Torizawa, Naoaki Murao, Tomoya Kotake, Masahiko Tanaka, Shiho Ishikawa, Taiji Miyake, Minoru Tamiya, Masako Arai, Aya Chiyoda, Sho Akai, Hitoshi Sase, Shino Kuramoto, Toshiya Ito, Takuya Shiraishi, Tetsuo Kojima and Hitoshi Iikura*. Validation of a New Methodology to Create Oral Drugs beyond the Rule of 5 for Intracellular Tough Targets. J. Am. Chem. Soc. 2023,145(44),24035-24051.https://doi.org/10.1021/jacs.3c07145


