【前沿】95.5%疾病控制率!实体瘤CAR-T细胞疗法BNT211新疗效数据出炉!
时间:2023-11-08 20:42:52 热度:37.1℃ 作者:网络
2023年11月5日,《OncLive》医学在线期刊公布了CAR-T细胞疗法BNT211治疗CLDN6阳性复发或难治性实体瘤患者的疗效和安全性。
CLDN6(Claudin6,重组靶向紧密蛋白连接蛋白6)是一种在正常成人健康组织中不表达,但是在卵巢癌、睾丸癌、肺腺癌、子宫癌等多种癌症类型中表达的蛋白。因此,CLDN6很有可能是继Claudin18.2之后,Claudin家族中另一个癌症治疗的潜力靶点。
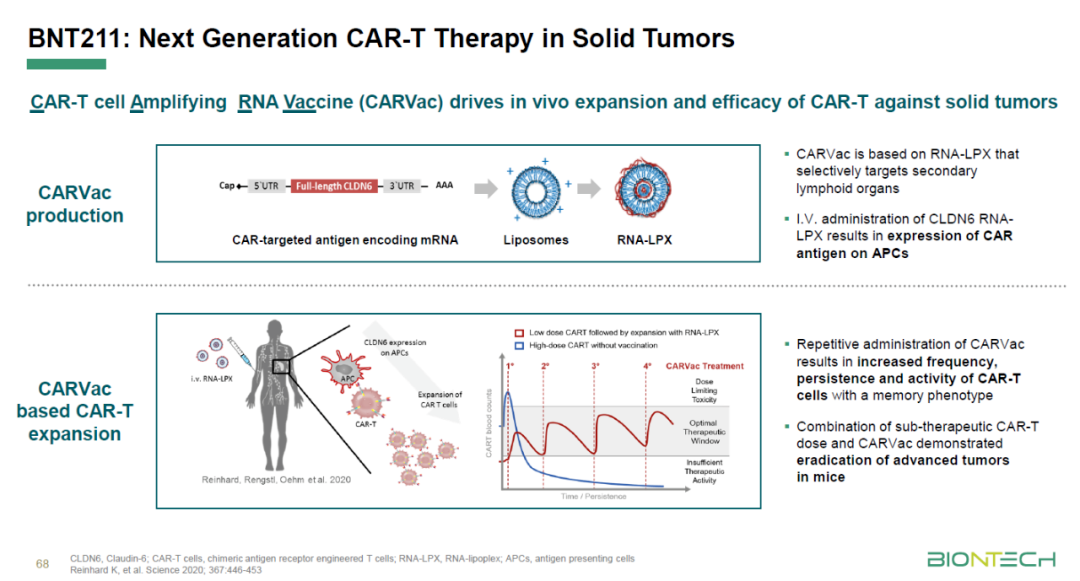
BNT211是一款潜在first-in-class疗法,由两种药物构成,一种是针对癌胚抗原CLDN6的自体CAR-T细胞疗法,另一种是编码CLDN6的协助CAR-T细胞扩增的RNA疫苗(CARVac),该疫苗基于BioNTech的mRNA脂质体技术开发,旨在改善过继移植细胞的持续性和功能。
BNT211设计的亮点包括:
1)开发的CAR-T细胞是靶向在多种实体瘤中高表达的新型肿瘤特异性抗原CLDN6;
2)BioNTech还开发了一种编码CLDN6的RNA的疫苗CARVac,从而维持CLDN6 CAR-T细胞在体内扩增、持久性和有效性。
图注:BNT211的作用机制
代号:BNT211
靶点:CLDN6
厂家:BioNTech公司
美国首次获批:尚未获批
中国首次获批:尚未获批
临床数据
在I/IIa期BNT211-01试验(NCT04503278)中,招募了患有复发或难治性晚期CLDN6阳性实体瘤的患者。
入组患者的人群特征包括:年龄为48岁;大多数患者是男性(n=25)并且具有CLDN6 2+/3+细胞(95%);上皮性卵巢癌(n=17)、生殖细胞肿瘤(GCT,n=16)或者其他癌症(n=11);先前接受治疗的线数为4。
试验的主要终点是安全性和耐受性以及评估剂量限制毒性(DLTs);次要终点包括免疫原性、客观缓解率(ORR)、疾病控制率(DCR)、反应持续时间(DOR)和无进展生存期(PFS)。
试验结果显示,在38例可评估疗效的患者中,总体客观缓解率(ORR)为44.7%,其中包括17例部分缓解(PR)或完全缓解(CR)的患者和11例疾病稳定(SD)的患者,10例患者出现了疾病进展(PD)。此外,疾病控制率(DCR)为73.7%。
值得注意的是,在接受剂量水平2【1×10^8个CAR-T细胞,无论是否接受过CAR-T的RNA疫苗(CARVac)】的BNT211治疗的22例可评估疗效的患者中,ORR为59.1%,其中13例患者获得PR或CR,8例患者出现SD,1例患者出现PD。而该队列的DCR为95.5%。
其他数据显示,在接受低于剂量水平2的BNT211治疗的9例疗效可评估患者中,ORR为11.1%,其中包括1例PR/CR患者和1例SD患者,7例患者出现PD;DCR为22.2%。
在接受大于剂量水平2的7例可评估疗效的患者中,ORR为42.9%,包括3例PR/CRs和2例达到SD的患者,2例患者出现PD;DCR为71.4%。
安全性
中位随访时间为94.5天(范围为9-401天),30例患者出现了与研究药物相关的3级或更高级别的治疗中出现的不良反应(TEAEs);14例患者出现了与研究药物相关的治疗中出现的严重不良事件。4例患者出现了剂量限制性毒性(DLTs)。
此外,23例患者患有细胞因子释放综合征,2例患者患有免疫效应细胞相关综合征。
小结
研究结果表明,CAR T细胞疗法BNT211在CLDN6阳性复发或难治性实体瘤患者中显示出临床活性的迹象,并且安全性在可控范围内。
参考来源:
https://www.onclive.com



