JCI Insight:肥胖会导致脂肪组织内复杂的炎症反应
时间:2023-10-15 11:27:02 热度:37.1℃ 作者:网络
最新数据显示,到2035年,全球超重或肥胖人口将超过40亿,约占全球人口的51%!值得关注的是,儿童青少年(5~19岁)肥胖率在所有年龄段中上升最快。肥胖已被认为是一种慢性低度炎症,脂肪组织参与了人体代谢、激素和免疫过程,从而导致慢性炎症。
尽管脂肪组织参与机体的免疫过程已被充分记录,但其调节免疫和代谢功能障碍的分子机制及其在脂肪细胞内的空间组织仍鲜为人知。近期,发表在JCI Insight杂志的一项最新研究,揭示脂肪组织结构的基本原理,特别是与肥胖相关的炎症,希望能解开脂肪堆积与不良健康后果之间的联系。

研究人员通过基因表达的单细胞分析与空间转录组学技术,揭示了以前未曾认识到的免疫细胞类型和脂肪组织内的相互作用。空间转录组学是一种较新的技术,它能捕捉整个组织薄片上所有基因表达。
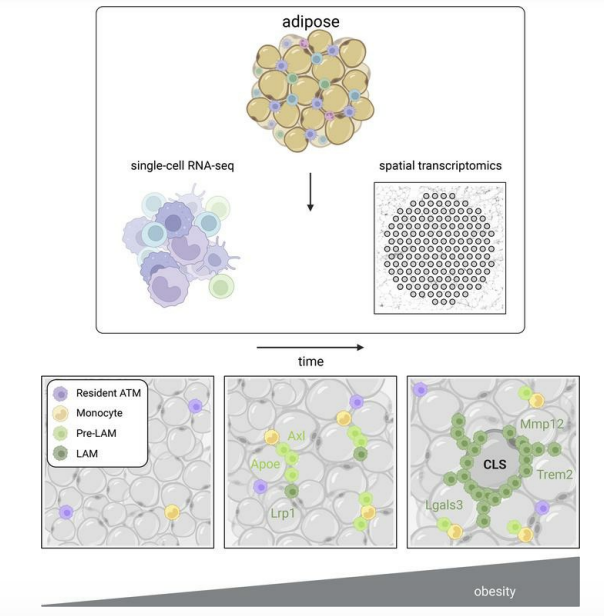
研究小组通过高脂肪饮食喂养小鼠14周,收集脂肪组织,然后利用单细胞和空间转录组学技术分析出样本中存在的所有mRNA。结果发现,给小鼠喂食“发胖饮食”的过程,脂肪组织内部的细胞,尤其是“脂质相关巨噬细胞”(LAM),会发生有趣的巨大变化。
具体而言,这些巨噬细胞分为五种类型,Mac1、2、3、4 和 5,其中Mac1在正常饮食的瘦小鼠和肥胖小鼠的组织中都有驻留。Mac2和Mac3有促炎症作用,小鼠在发胖饮食8周后达到高峰。随着身体进一步发胖,发胖饮食喂养到14周的时候,抑炎症作用的Mac4和Mac5就占了主导地位,而之前的促炎症的Mac2和Mac3细胞则减少了。
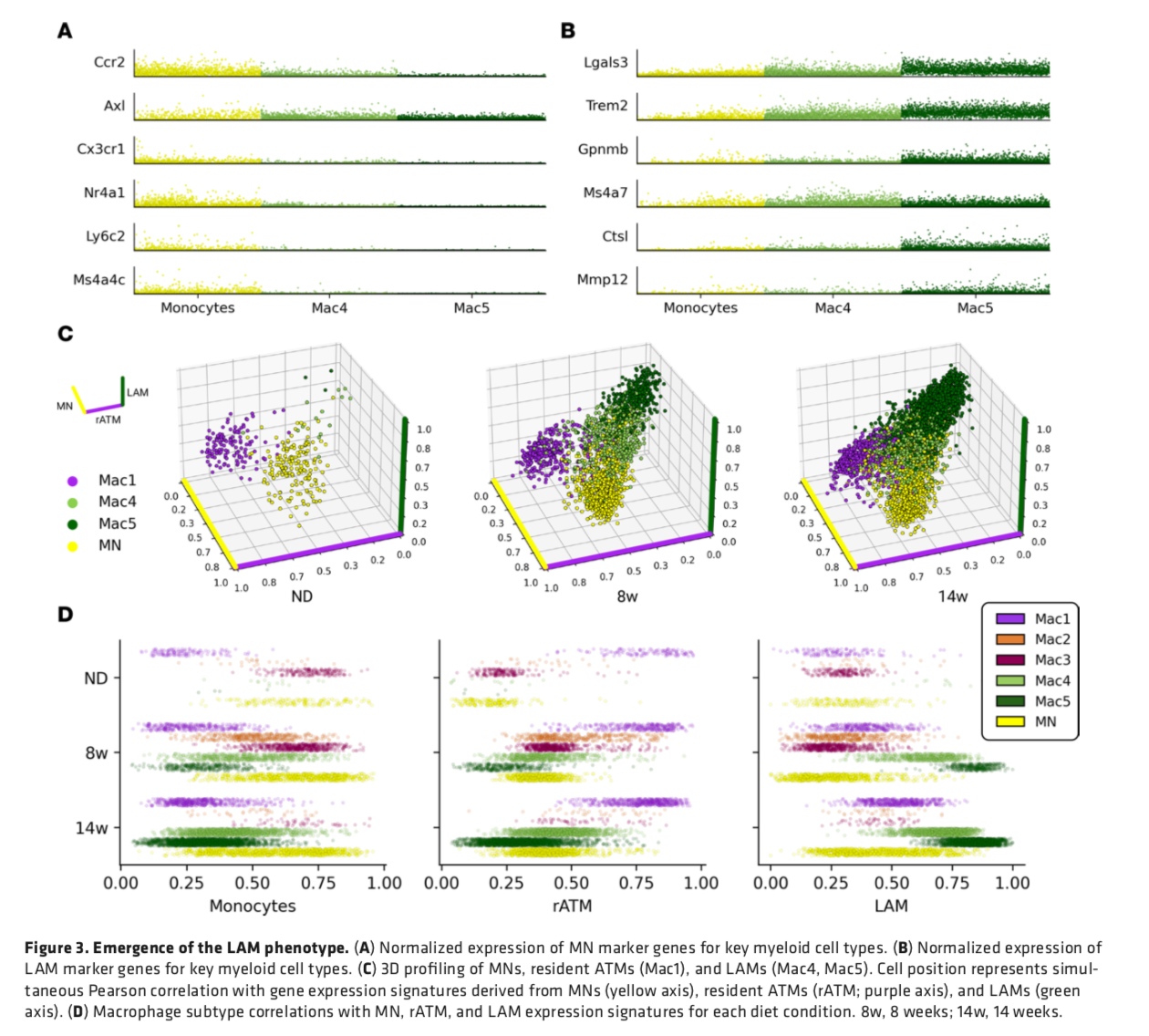
接下来,研究小组对新鲜冷冻脂肪组织进行了细致的切片分析,发现被称为类冠状结构的蛛丝马迹,这种结构与胰岛素抵抗有关。
“类冠状结构一旦出现,需要很长时间才能消失,它们的出现预示着组织功能障碍。”研究者表示,“通过图像处理,根据这些区域的密度确定了可能是冠状结构的区域,然后进入这些区域进行验证,我们可以直观地看到它们。这些结构的基因表达表明存在 Mac4 和 Mac5 LAMs。”
尽管脂肪组织受到人人喊打的地步,但其实它是一种重要的能量储备以及内分泌器官。健康状态下,脂肪组织其实是一种调节我们内在环境的一种“缓冲系统”。随着社会经济的发展,不良的生活方式增加了超重和肥胖的可能,导致脂肪组织不再那么“可爱”。
原始出处
Cooper M. Stansbury et al, A lipid-associated macrophage lineage rewires the spatial landscape of adipose tissue in early obesity, JCI Insight (2023). DOI: 10.1172/jci.insight.171701


