自体干细胞移植后pembrolizumab治疗T细胞非霍奇金淋巴瘤的2期研究(NCT02362997)
时间:2023-08-28 16:45:43 热度:37.1℃ 作者:网络
研究背景
自体干细胞移植(ASCT)常用于首次缓解的几种亚型外周T细胞淋巴瘤(PTCL)的巩固治疗。然而,许多患者在ASCT后复发,预后很差。对于移植后PTCL的维持或巩固,目前尚无批准的治疗方案。PD-1阻断已证明对PTCL患者有一定疗效。因此,我们对首次缓解的PTCL患者进行ASCT后抗pd -1单克隆抗体的2期多中心研究。
纳入人群
年龄≥18岁的首次缓解(部分或完全)PTCL患者被纳入研究。符合条件的PTCL亚型包括PTCL、NOS、AITL;ALK-negative ALCL;肠病相关T细胞淋巴瘤(EATL); 单形性嗜上皮性肠道T细胞淋巴瘤( (MEITL);和ENKTL。其他PTCL亚型包括ALK阳性PTCL和皮肤 T细胞淋巴瘤的患者不符合条件。
主要入选标准为 ECOG评分≤1,血液学和器官功能良好,无抗PD-1治疗禁忌。淋巴瘤累及中枢神经系统的患者排除在外。此外,先前接受过抗PD-1、抗PD-L1或抗CTLA-4治疗的患者不符合本研究的条件。
研究方案
治疗和评估建议在ASCT术后出院后21天内开始治疗,不迟于移植第60天。在开始治疗之前,患者需要有适当的血液学恢复(根据不良事件通用术语标准(CTCAE) 4.0版本2级或更低)。治疗包括Pembrolizumab 200mg,每3周静脉给药,最多8个周期。
该给药方案是基于pembrolizumab在HL和DLBCL的同伴研究中的剂量。不允许修改剂量。然而,随后的给药可延迟至12周毒性。ASCT后,参与者不能接受任何额外的治疗(包括放疗、化疗或免疫治疗)。由于4级治疗相关不良事件(AE)和选定的3级免疫相关不良事件(irAEs),该药被永久停药。
研究终点
主要终点是接受Pembrolizumab治疗的ASCT住院患者的18个月无进展生存期(PFS)率。
次要终点包括18个月总生存期(OS)、PFS、ASCT后可测量疾病患者对Pembrolizumab的反应率和安全性。
研究结果
在2017年1月至2020年7月期间,共有21名患者参加了这项研究。
中位年龄为58岁(33-73岁)。最常见的亚型是PTCL NOS(52%)。其他亚型为AITL(19%)、ENKTL(14%)、ALK- ALCL(10%)和MEITL(5%)。所有患者既往均接受1次治疗。大多数患者在ASCT前为4期(43%)。在所有患者中,14%为低风险IPI, 43%为中等风险,5%为高风险IPI, 38% IPI评分未知。
在ASCT之前,90%的患者处于完全代谢反应(CMR)。在研究开始时,95%的患者处于CMR状态。在21例患者中,14例患者完成了计划的8个疗程的治疗。其余患者完成1 (n=4例)、2 (n=1)、4 (n=1)和5 (n=1)个周期。周期的中位数为8。
3例患者出现给药延迟,1例患者漏给药。
停止治疗的原因有毒性(n=4)、疾病进展(PD) (n=1)、撤回同意(n=1)和COVID-19感染(n=1)。在4例因毒性停止治疗的患者中,2例患者为2级和3级转氨酶升高,1例患者为3级腹泻,1例患者为2级关节痛。
在所有受试者中,13/21在ASCTt后18个月存活且无进展,从而达到主要终点。其余8例患者在前18个月的随访中,3例分别在4、12和12个月时复发,5例在18个月时没有随访资料。
中位随访时间为24个月。放射学进展发生在第10周。在4例因毒性而停止治疗的患者中,2/4的患者持续CR达14和16个月;1例患者仅进行了一次评估,因此被审查;最后一名患者的CR持续了23个月,直到PD。
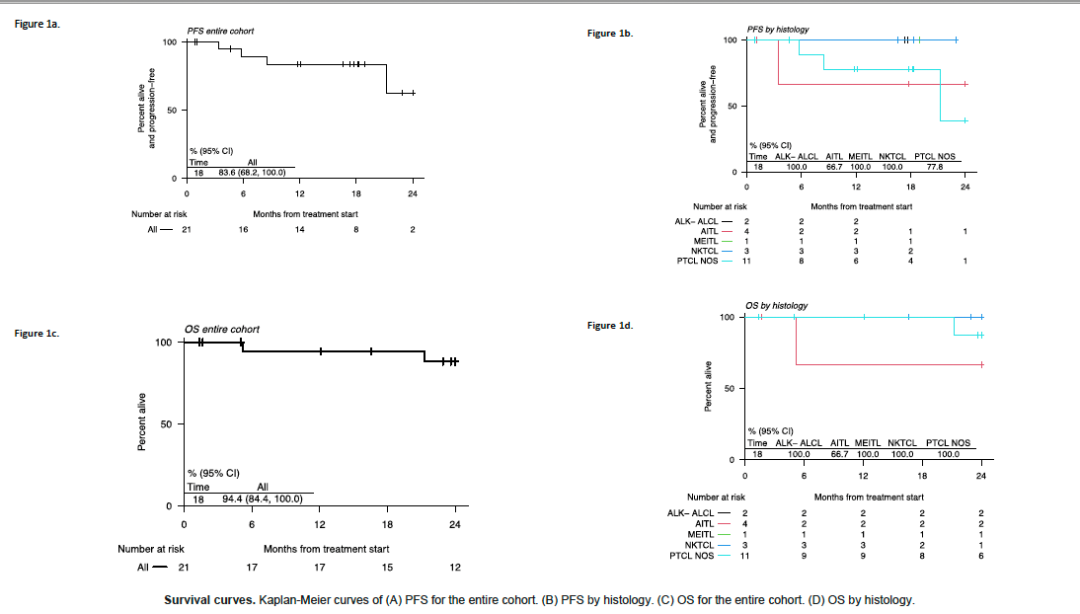
PFS和OS的Kaplan-Meier估计如图1所示。18个月PFS估计为83.6% (95% CI: 68 - 100), OS为94.4% (95% CI: 84 - 100)。在研究期间死亡的2名患者患有帕金森病。对不同亚型的PFS和OS进行评估,无显著差异(图1b和1d)。值得注意的是,3例ENKTL患者在研究期间没有进展(图1b)。21例患者中有13例存在EBV状态。EBV阳性组与阴性组PFS (p=0.55)和os (p=0.49)差异无统计学意义。如前所述,我们没有系统地收集18个月后的数据。因此,我们没有对这些患者进行更长期的随访。
毒副作用与已知的Pembrolizumab毒性作用一致,无5级毒性。
研究结论
Pembrolizumab作为PTCL首次缓解期患者的巩固治疗有效。ASCT后给予Pembrolizumab具有可接受的安全性。


