Nat Mater:新型纳米颗粒递药平台,突破血脑屏障,显著增强脑肿瘤治疗效果
时间:2023-03-11 11:01:25 热度:37.1℃ 作者:网络
髓母细胞瘤(Medulloblastoma,MB)是最常见的儿童恶性脑肿瘤,约占儿童所有脑肿瘤的20%,其具有高度侵袭性,难以治疗,近30%的患者被认为是无药可治的。即使是治疗成功的儿童也可能经历严重的长期残疾和健康问题,这主要是由于放疗和化疗的不良副作用导致的。
由于血脑屏障(Blood-Brain Barrier,BBB)的存在,将药物靶向递送到受影响的脑组织是目前临床面临的一大挑战。血脑屏障是指脑毛细血管壁与神经胶质细胞形成的血浆与脑细胞之间的屏障,和由脉络丛形成的血浆和脑脊液之间的屏障,仅允许特定类型的分子从血流进入大脑神经元和其他周围细胞。
血脑屏障的存在,对于阻止有害物质由血液进入大脑具有重要意义,但这也同时阻止了绝大部分小分子和大分子药物(例如多肽,蛋白质和核酸)的转移,严重限制了中枢神经系统疾病(例如神经退行性疾病、脑肿瘤,脑部感染和中风等)的治疗。
近日,纪念斯隆·凯特琳癌症中心的研究人员在 Nature 子刊 Nature Materials 上发表了题为:P-selectin-targeted nanocarriers induce active crossing of the blood–brain barrier via caveolin-1-dependent transcytosis 的研究论文。
该研究表明,脑肿瘤中的血管内皮细胞表达P-选择素(P-selectin),并通过微囊蛋白1(Caveolin-1)介导的胞吞转运(Transcytosis)促进物质在完整血脑屏障中的跨内皮转运。
利用这一机制,研究团队开发了靶向P-选择素的岩藻多糖-纳米颗粒,这一纳米载体携带的抗癌药物维莫德吉Vismodegib,能够更高效突破血脑屏障(BBB),主动转运到脑肿瘤组织,而不影响正常大脑组织,在小鼠模型中展示了更强的癌症治疗效果和更低的副作用。同时,辅助低剂量放疗,能够促进内皮细胞的P-选择素表达水平,进一步增强治疗效果。

由于血脑屏障对大脑的保护作用,将药物靶向递送到受影响的脑组织一直是一大难题,血脑屏障的完整性会极大地影响治疗效果。这在髓母细胞瘤(Medulloblastoma,MB)的治疗中已经得到了很好的验证。大约三分之一的髓母细胞瘤是由Sonic hedgehog(SHH)信号通路介导的,这部分患者(SHH-MB)的临床结果更差,部分原因是血脑屏障限制了药物的进入,导致药物达不到治疗所需浓度。
鉴于相关小分子药物难以通过血脑屏障,研究人员已经转向研究纳米颗粒,将其作为改善药物向脑组织递送效率的潜在方法。然而,现有的将装载药物的纳米颗粒被动运输以突破完整血脑屏障,抑或是受损的血脑屏障,效率都不尽如人意。
在这项最新研究中,研究团队尝试使用主动运输方式来解决这一难题。在人体面临病原体感染时,免疫系统能够将免疫细胞主动运输到受感染、出现炎症或组织损伤的部位。免疫系统并非随机将免疫细胞运输到全身各处,而是在激活的血管上有一种归巢机制,这一机制由血管内皮细胞表达的P-选择素(P-selectin)所介导,而这种独特的归巢机制在脑肿瘤血管中也存在。
该研究团队此前已经证明了岩藻多糖-纳米颗粒可以靶向P-选择素,还发现了极低剂量的放疗可以增强内皮细胞上P-选择素的表达水平,从而使纳米颗粒在肿瘤部位积聚得更多。而该研究进一步发现,P-选择素促进物质在完整血脑屏障中的跨内皮转运是通过微囊蛋白1(Caveolin-1)介导的胞吞转运(Transcytosis)实现的。
利用这一机制,可以将载药的岩藻多糖-纳米颗粒靶向脑肿瘤,而不影响正常大脑组织。
Vismodegib(维莫德吉)是由Genentech开发的一款小分子药物,通过选择性靶向SHH通路的效应物SMO蛋白发挥作用,已被FDA批准用于治疗基底细胞癌。临床试验显示,其对SHH通路相关髓母细胞瘤(SHH-MB)有效,但血脑屏障会导致其进入大脑的药物浓度,从而降低治疗效果,如果增加使用剂量,则会导致患儿出现骨毒性。
研究团队使用具有完整血脑屏障的SHH-MB小鼠模型上验证了这一岩藻多糖-纳米颗粒药物递送平台的效果。实验结果显示,装载Vismodegib的岩藻多糖-纳米颗粒(简称FiVi),能够在低剂量下展示出强大抗肿瘤效果,并且显着减弱了骨毒性。此外,辅助极低剂量的放疗(XRT),还能够进一步增强治疗效果。
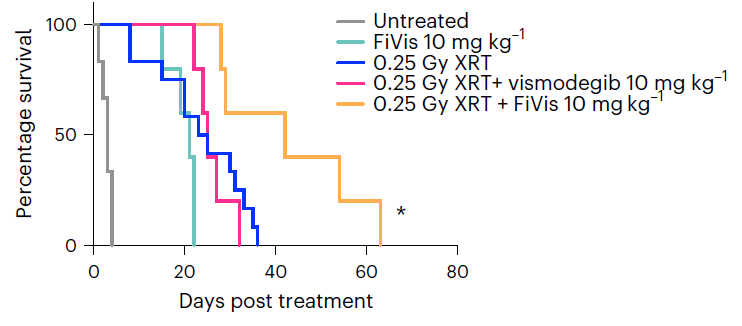
总的来说,该研究证明了一种高效突破血脑屏障的纳米载体药物递送策略,能够更高效、更特异性地将治疗药物递送到脑肿瘤组织,实现更好的癌症治疗效果和更低的副作用。更重要的是,这一纳米载体药物递送平台,还有望改善儿童和成人的其他脑肿瘤,以及脑部疾病的治疗,包括癫痫、多发性硬化症、中风、神经退行性疾病等等。
原始出处:
Tylawsky, D.E., Kiguchi, H., Vaynshteyn, J. et al. P-selectin-targeted nanocarriers induce active crossing of the blood–brain barrier via caveolin-1-dependent transcytosis. Nat. Mater. 22, 391–399 (2023). https://doi.org/10.1038/s41563-023-01481-9.


