2022年终盘点 | NSCLC靶向治疗之KRAS篇
时间:2023-01-03 15:01:03 热度:37.1℃ 作者:网络
每年有近 180 万人死亡,肺癌仍然是全世界癌症相关死亡的主要原因。非小细胞肺癌 (NSCLC) 占所有确诊病例的 85%,腺癌是最常见的组织学亚型。近年来,分子表征的进展和新靶向疗法的开发改变了 NSCLC 的治疗方案。到目前为止,多年来被认为无法通过药物治疗的分子改变,例如 KRAS 突变,现在可能会受益于靶向药物。
NSCLC中的KRAS:不同的改变和患者的特征
在 NSCLC 中,高达 30% 的病例发现 KRAS 突变,最常见的是密码子 12(90% 的病例),而不太常见的突变见于密码子 13 (2–6%) 和 61 (1%)。在密码子 12 突变中,KRAS G12C突变代表了 NSCLC 中最普遍的 KRAS 改变(占所有 KRAS 突变病例的 40%),其次是KRAS G12V (21%), 以及KRAS G12D (17%)。
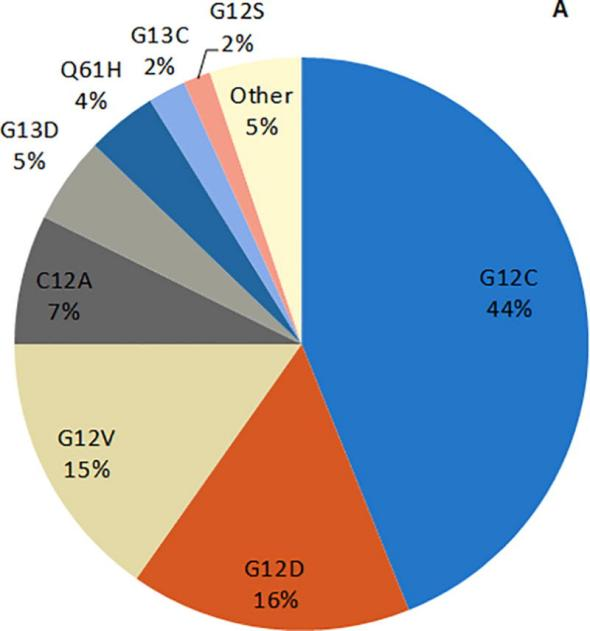
KRAS 突变 NSCLC 的靶向治疗
KRAS 突变多年来一直被认为是不可治愈的。靶向这种蛋白质的困难主要与其光滑的表面及其对 GTP 的高亲和力有关,这使得靶向 GDP/GTP 结合位点非常具有挑战性 。随后发现的 KRAS 蛋白开关口袋 II 代表了 KRAS 突变治疗的突破,并且进一步开发了特异性结合 KRAS 突变蛋白半胱氨酸残基的分子。尽管迄今为止已开发出不同的分子,但索托雷塞 (AMG 510)和 adagrasib 是迄今为止获得监管批准的两种药物。

新型 KRAS 抑制剂的作用机制
索托雷塞 (AMG 510)
索托雷塞 (AMG 510) 是最早进入临床试验的分子之一。在单组 I-II 期 CodeBreaK100 试验中,评估了索托雷塞 (AMG 510)在不同类型的 KRAS G12C 突变癌症中的疗效和安全性。
FDA加速批准是基于CodeBreak 100研究Ⅱ期研究结果。在126例既往治疗后发生疾病进展的局部晚期或转移性KRAS G12C突变NSCLC患者中对索托雷塞进行评价。在评估反应的 124 名患者中,4 名 (3.2%) 有完全反应,42 名 (33.9%) 有部分反应;在 102 名患者 (82.3%) 中观察到任何程度的肿瘤缩小;在 46 名出现客观缓解的患者中,中位缓解时间为 1.4 个月(范围,1.2 至 10.1 个月),中位缓解持续时间为 11.1 个月(95% CI,6.9 至无法评估)。
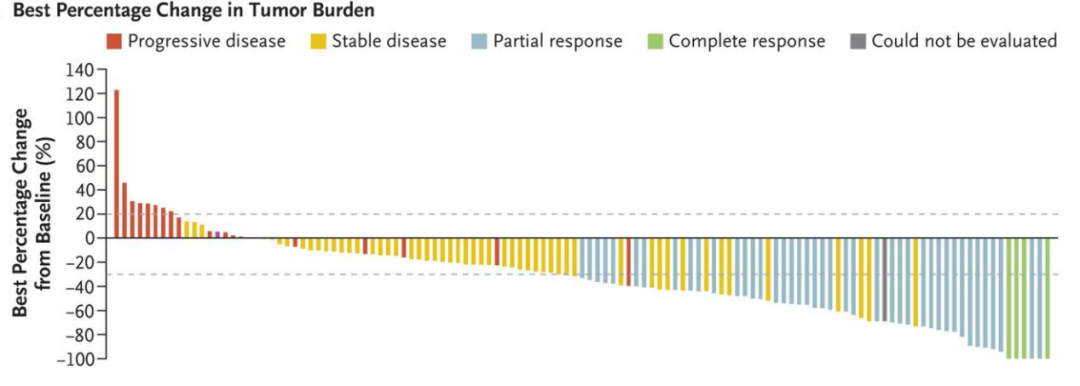
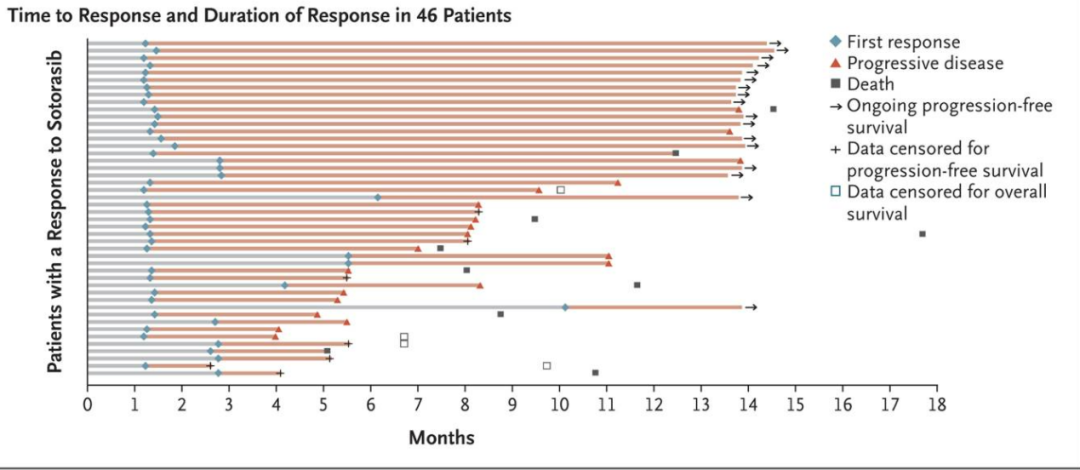
可评估的 124 名患者的中位无进展生存期为 6.8 个月(95% CI,5.1 至 8.2)。Kaplan-Meier 估计的无进展生存期在 6 个月时为 52.2%(95% CI,42.6 至 60.9),在 9 个月时为 37.5%(95% CI,28.4 至 46.5)。所有 126 名登记患者的中位总生存期为 12.5 个月(95% CI,10.0 至无法评估)。
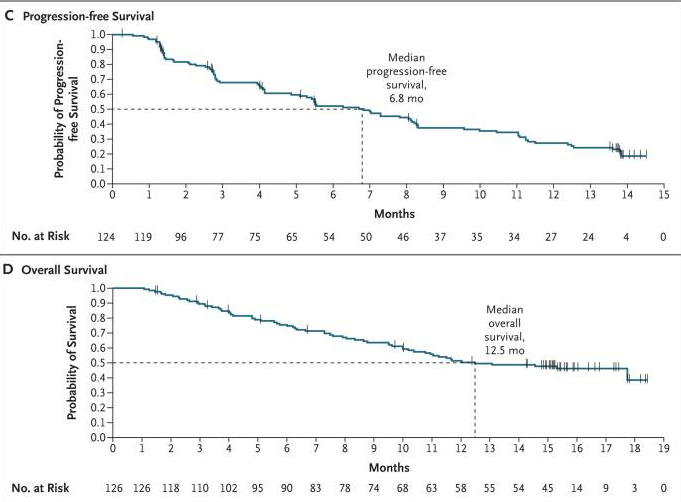
有趣的是,一项事后分析证明了 sotorasib 的颅内疗效。值得注意的是,在基线时有可评估脑转移的 40 名患者中,ORR 为 25%,DCR 为 87.5%。
CodeBreak 200 试验的初步结果已在 2022 年 ESMO 会议上公布。这是一项全球性、开放标签、随机的 III 期试验,旨在评估 索托雷塞 与多西紫杉醇对 KRAS 突变 NSCLC 患者的疗效。
在中位随访 17.7 个月时,与多西紫杉醇相比,索托雷塞显示出更长的 PFS(HR= 0.66 [95% CI: 0.51, 0.86],p= 0.002),索托雷塞和多西他赛组报告的 1 年 PFS 分别为 24.8% 和 10.1%。在次要终点中,ORR 和 DCR 有利于 索托雷塞。在安全性方面,索托雷塞 的耐受性优于多西紫杉醇,并且与上述结果一致,索托雷塞 组最常报告的 ≥ 3 级副作用是腹泻 (33.7%)、恶心 (14.2%)、疲劳 (6.5%)、肝酶改变(ALT/AST 各增加 10.1%)。
Adagrasib (MRTX849)
Adagrasib (MRTX849) 是第二种进入临床试验的 KRAS G12C 抑制剂。2022 年 12 月 12 日,Mirati Therapeutics 宣布美国 FDA 加速批准 adagrasib 作为具有 KRAS G12C 突变的局部晚期或转移性非小细胞肺癌( NSCLC )患者的靶向治疗选择。该监管决定是基于 2 期 KRYSTAL-1 试验 (NCT03785249) 的结果。
基于 KRYSTAL-1 研究的第 2 期注册启用队列,KRAZATI 已显示出积极的获益-风险概况,并在 116 名 KRAS G12C突变晚期 NSCLC患者中评估了 KRAZATI 600 mg 胶囊每天两次口服给药,这些患者先前接受过用铂类方案和免疫检查点抑制剂治疗。该试验表明 ORR 为 43%(95% CI:34-53),80%(95% CI:71-87)的患者实现了疾病控制。中位 DOR 为 8.5 个月(95% CI:6.2-13.8)。
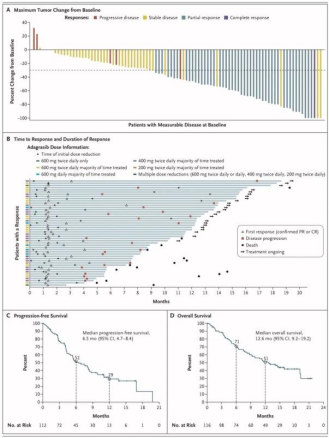
在一项汇总疗效分析 (n=132) 中,包括来自 KRYSTAL-1 研究的 1/ 1b期 NSCLC 和注册的 2 期 NSCLC 队列,评估adagrasib 作为单药口服 600 毫克胶囊,每天两次, adagrasib 显示出 44% 的 ORR 和基于 BICR 的疾病控制率为 81%,中位 DOR 为 12.5 个月(95% CI,7.3-NE),中位总生存期为 14.1 个月(94% CI,9.2-19.2)。
在参加 KRYSTAL-1患者中,最常见 (≥ 20%) 的不良事件 (AE) 包括腹泻、恶心、疲劳、呕吐、肌肉骨骼疼痛、肝毒性、肾功能损害、呼吸困难、水肿、食欲下降、咳嗽、肺炎、头晕、便秘、腹痛和 QTc 间期延长。
不用出境就可以和国外同步使用最新抗癌新药
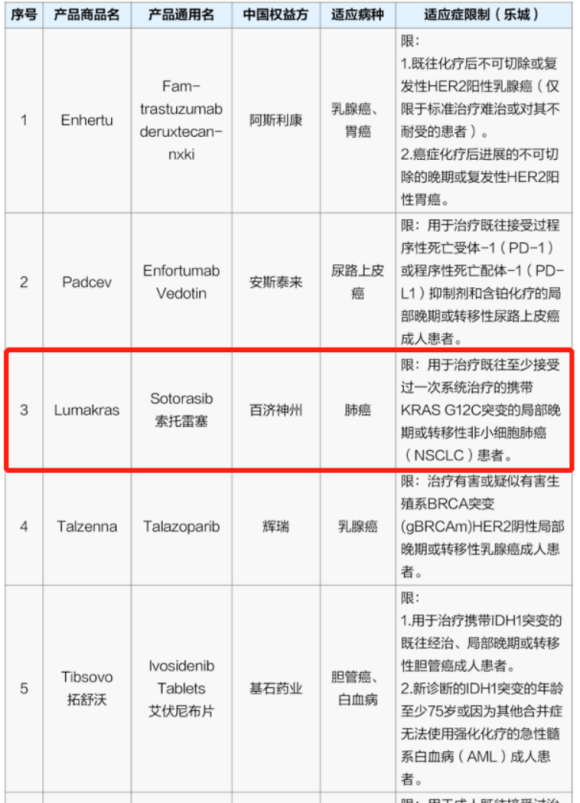
海南博鳌乐城国际医疗旅游先行区是我国首个以国际医疗旅游服务为主要内容的国家级试验区,并且在肿瘤治疗领域形成产业集聚,特别是肿瘤新药发展加速推进,积极探路打造医疗健康开放新高地。目前多款肿瘤新药可惠及中国患者,文中提到的索托雷塞(索托雷塞(AMG510))已完美落地海南博鳌,并且根据进口药品带离管理暂行办法,患者经过审批,可将仅供自用的口服进口药品带离先行区,这也大大增加了患者用药的便捷性,降低了患者及家属用药衣食住行等辅助成本。
另,从目前国家政策来看,各渠道都在大力推广海南新特药的内地肿瘤患者用药,并且纳入多款城市惠民保免费用药政策,例如上海,北京,海南,内蒙和西宁,现在针对索托雷塞(索托雷塞(AMG510))海南用药均可以报销。

参考文献:
Cascetta P, Marinello A, Lazzari C, Gregorc V, Planchard D, Bianco R, Normanno N, Morabito A. KRAS in NSCLC: State of the Art and Future Perspectives. Cancers (Basel). 2022 Nov 4;14(21):5430. doi: 10.3390/cancers14215430. PMID: 36358848; PMCID: PMC9656434.
: , 。 视频 小程序 赞 ,轻点两下取消赞 在看 ,轻点两下取消在看


