ASCO 2021:非小细胞肺癌专场--口头报告(01)
时间:2021-06-05 21:01:50 热度:37.1℃ 作者:网络
主席:Raymond U. Osarogiagbon,FACP,MBBS ,浸信会癌症中心,多学科胸肿瘤科| Christine L. Hann,医学博士,博士,约翰霍普金斯大学医学院,悉尼金梅尔综合癌症中心日
主题:非小细胞肺癌
摘要介绍1
晚期非小细胞肺癌 (NSCLC) 患者的一线纳武单抗 (NIVO) 加伊匹单抗 (IPI) 加两个周期的化疗(化疗)与单独化疗(4 个周期):来自 CheckMate 9LA 的两年更新
DOI:10.1200/JCO.2021.39.15_suppl.9000
在随机 3 期 CheckMate 9LA 试验 (NCT03215706) 中,一线 NIVO + IPI 联合 2 个周期的化疗与单独化疗相比显着提高了总生存期 (OS)、无进展生存期 (PFS) 和客观缓解率 (ORR) (4 个周期)。无论程序性死亡配体 1 (PD-L1) 表达水平和组织学如何,都观察到了临床益处。在这里,我们报告了这项研究最少随访 2 年的数据。
根据 PD-L1(< 1% vs. ≥ 1%)、性别和组织学(鳞状或非鳞状)对IV 期/复发性 NSCLC、ECOG 体能状态 ≤ 1且无已知敏感EGFR/ALK改变的成年患者(pts)进行分层-squamous) 并按 1:1 随机分配至NIVO 360 mg Q3W + IPI 1 mg/kg Q6W + 化疗(2个周期;n = 361)或单独化疗(4 个周期;n = 358)。单独化疗组中的非鳞状 NSCLC 患者可以接受培美曲塞维持治疗。主要终点是OS。次要终点包括盲法独立中央审查的PFS和ORR,以及不同PD-L1水平的疗效。
OS 的最短随访时间为24.4个月(数据库锁定:2021年2月18日),接受NIVO + IPI +化疗的患者继续获得OS获益与化疗相比,中位OS分别为15.8个月和11.0个月(HR,0.72 [95% CI,0.61–0.86]);2年OS率分别为38%和26%。NIVO + IPI +化疗与化疗的中位PFS分别为6.7个月和5.3个月(HR,0.67 [95% CI,0.56–0.79]);分别有8%和37%的疾病进展患者接受了后续免疫治疗。NIVO + IPI +化疗的ORR为38%,而化疗为25%。在所有随机患者和大多数亚组中,包括PD-L1表达水平(表)或组织学,观察到NIVO + IPI +化疗与化疗的相似临床益处。
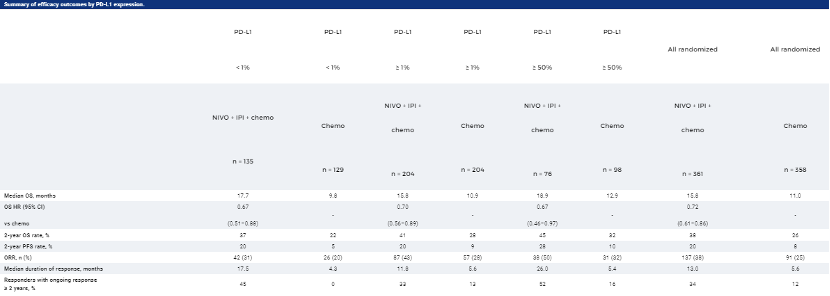
在最少2年的随访中,一线 NIVO + IPI + 化疗在晚期 NSCLC 患者中显示出与化疗相比的持久生存和获益;没有发现新的安全事件。
摘要介绍2
PD-L1评分1-49%的晚期非小细胞肺癌(NSCLC)一线 (1L)治疗的抗PD-(L1)联合化疗与单独免疫疗法(IO)的结果:FDA汇总分析
DOI:10.1200/JCO.2021.39.15_suppl.9001
IO +化疗±抗血管生成药物包括FDA批准的用于转移性NSCLC的1L方案,仅IO疗法仅批准用于PD-L1阳性NSCLC。PD-L1评分为1-49%的患者有许多治疗选择,但对不同治疗方案的患者亚组如何受益知之甚少。
数据来自8项随机对照试验,这些试验研究了抗PD-(L)1疗法作为仅IO或化疗IO方案用于晚期NSCLC患者的1L治疗。PD-L1评分定义为检测染色的肿瘤细胞比例,对肿瘤PD-L1评分为1-49%的患者进行分析。未考虑肿瘤浸润免疫细胞染色。通过汇总分析比较了化疗IO和单独IO之间的OS和PFS。使用Kaplan-Meier方法估计中位生存时间。使用通过试验分层并根据年龄、性别、种族、ECOG、组织学和吸烟状况进行调整的Cox比例风险模型估计风险比。
共有2108名NSCLC和PD-L1评分为1-49%的患者被确定用于该分析。基线特征是:37% 的年龄在65-74岁之间,12%的年龄在75岁以上;67%男性;79%白色;65% ECOG ≥ 1;和85%的吸烟者。中位随访时间为12.1个月。该汇总分析显示,与单独接受IO治疗的患者(N=529)相比,接受化疗IO的患者(N=639)具有更长的PFS和OS,中位PFS分别为7.7 和 4.2个月(HR 0.60;95% CI 0.48, 0.76 ) 和中位OS 21.4与14.5个月(HR 0.68;95% CI 0.52, 0.90)。呈现的所有结果都被认为是探索性的和假设生成的。

按亚组划分,化疗-IO与单独IO的疗效结果
这项探索性的集合分析表明,在PD-L1评分为1-49%的晚期NSCLC患者的大多数亚组中,化疗-IO可能比单独的IO改善疗效结果。75岁及以上的患者在各种治疗方案中的结果相似。
摘要介绍3
来自 3 期试验 IMpower130、IMpower132 和 IMpower150 的免疫相关不良事件 (irAE) 和疗效的汇总分析
DOI:10.1200/JCO.2021.39.15_suppl.9002
PD-L1/PD-1抑制剂已经改变了晚期NSCLC的治疗(tx)。有证据表明,使用这些药物发生irAE 可以预测癌症(如 NSCLC)的预后改善。Atezolizumab(atezo;抗 PD-L1)已在NSCLC 中显示出疗效和耐受性,目前已在1L和2L+环境中获得批准。第3期IMpower130、IMpower132和IMpower150 试验将atezo +化疗±贝伐单抗 (bev) 评估为1L NSCLC。我们在这些试验中探索了irAE与疗效之间的关联。
每项试验都招募了未接受过治疗的非鳞状第四期NSCLC患者(pts)。患者被随机分配到:IMpower130中的卡铂(carbo)+纳博-紫杉醇(nab-paclitaxel)单独使用或与阿替佐(atzo)一起使用;IMpower132中的carbo或顺铂单独使用或与阿替佐一起使用;IMpower150中的阿替佐(A)+贝弗(B)+carbo+紫杉醇(CP)、ACP或BCP。数据被汇集在一起(数据截止日期。2018年3月15日[IMpower130];2018年5月22日[IMpower132];2019年9月13日[IMpower150]),并按tx(含atezo vs对照)和irAE状态进行分析。使用时间依赖性的Cox模型和1、3、6和12 mo的地标分析来控制不朽的偏差。研究方案要求对≥3级(Gr)的irAEs中断/中止阿替唑类药物治疗。
2503名患者被纳入分析(特异性,n = 1577;对照,n = 926)。在两组中,有irAEs的病人(阿特佐,n = 753;对照组,n = 289)和没有irAEs的病人(阿特佐,n = 824;对照组,n = 637)的基线特征基本平衡。48%(阿特佐)和32%(对照组)的患者出现任何等级的irAEs;11%(阿特佐)和5%(对照组)出现3-5级的irAEs。最常见的irAEs(阿特佐与对照组)是皮疹(28% vs 18%)、肝炎(实验室异常;15% vs 10%)和甲状腺功能减退(12% vs 4%)。首次出现IRAE的中位时间为1.7(亚特佐)vs 1.4 mo(对照组)。从时间依赖的Cox模型来看,有与无irAEs的患者的OS HRs(95% CI)在阿特佐组为0.69(0.60,0.78),在对照组为0.82(0.68,0.99);在排除皮疹(被认为是最不特殊的irAE)后,OS HRs(95% CI)分别为0.75(0.65,0.87)和0.90(0.71,1.12)。OS的标志性数据见表。
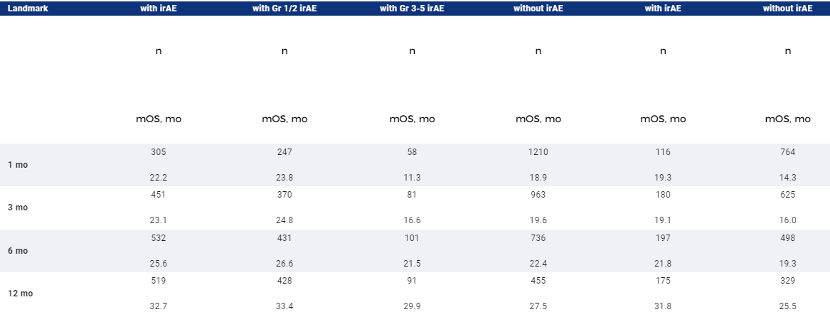
在这个探索性的综合分析中,根据时间依赖性的Cox模型和里程碑分析,在含阿替佐的治疗组和对照组中,有irAEs的患者与没有irAEs的患者相比,OS更长;在排除皮疹后,阿替佐治疗组仍有这种趋势。地标分析表明,在含阿特唑组中,有1/2级irAEs的患者的OS最长,有≥3级irAEs的患者的OS最短,可能是由于治疗中断/中止。
摘要介绍4
来自CodeBreaK 100 2期试验的总生存期和探索性亚组分析,评估sotorasib在预处理的KRAS p.G12C突变非小细胞肺癌中的疗效
DOI:10.1200/JCO.2021.39.15_suppl.9003
在注册第2期CodeBreaK 100试验中,索托拉西的客观缓解率 (ORR) 为37.1%(95% Cl: 28.6, 46.2),中位无进展生存期 (PFS) 为6.8个月(95% Cl: 5.1, 8.2) 在预先治疗过的KRAS p.G12C 突变非小细胞肺癌 (NSCLC) 患者中。在携带STK11共突变的患者中观察到肿瘤反应,这是标准护理下临床结果不佳的驱动因素。在这里,我们通过关键基线特征和生物标志物报告了一组扩展患者亚组的疗效。
Sotorasib以960毫克的剂量口服,每天一次,给符合条件的携带KRAS p.G12C并接受过标准疗法的晚期NSCLC患者服用。主要终点是通过中央审查评估的ORR。主要次要终点包括PFS、总生存期和安全性。KRAS p.G12C突变等位基因频率(MAF)和肿瘤突变负荷(TMB)通过使用组织样本进行下一代测序(NGS)分析。个别基因的突变状态是通过NGS使用组织和/或血浆样本确定的。在有相应结果的患者子集中,分析了反应与KRAS p.G12C MAF、TMB或共变之间的相关性。MAF和反应之间的关系通过几率(95%CI)报告,来自于逻辑回归,因变量为反应者的对数几率,自变量为MAF,单位为10%。


跨亚组的ORR 列于表中。反应与研究人群中的KRAS p.G12C MAF无关。
研究显示,在 CodeBreaK 100 2 期试验的探索性分析中,在患者亚组中观察到了索托拉西的临床益处。将介绍总生存期和更新的探索性分析。


