Alz Res Therapy:遗传变异或揭示AD发病的潜在机制
时间:2021-11-08 19:01:28 热度:37.1℃ 作者:网络
阿尔茨海默病(AD)具有高度的遗传性,晚发性AD(LOAD)的遗传率为58-79%。以前的大规模全基因组关联研究(GWASs)已经发现了超过20个AD基因变异,这些变异赋予了LOAD的风险。

APOE仍然是LOAD最强的遗传风险因素,导致风险增加3至15倍。然而,这些确认的变异体只占疾病遗传性的一小部分。在寻找额外的LOAD风险变异体的过程中,最近的GWAS荟萃分析发现了超过30个AD风险基因。这些新的基因变异体的鉴定可能会对在AD发病机制中具有重要作用的分子机制提供有价值的见解。
虽然迄今为止描述的大多数非APOE的AD相关基因变异位于内含子或非编码区,但这些变异仍可能影响附近的基因表达并发挥保护或诱发疾病的作用。
此外,AD的发展经历了一个漫长的临床前阶段,有异常的神经病理学生物标志物。最近,美国国家老龄化研究所和阿尔茨海默氏症协会(NIAAA)发布了一个最新的研究框架,为产生或测试有关AD不同病理过程的假设提供了一个灵活的平台,该框架通过神经病理学生物标志物将AD定义为三类。
淀粉样变生物标志物,特别是皮质淀粉样变-PET配体结合或低CSF Aβ42;tauopathy生物标志物,特别是CSF磷酸化tau(pTau)升高或皮质tau-PET配体结合;以及神经变性生物标志物,特别是CSF总tau(ttau)升高,18F-氟脱氧葡萄糖(FDG)-PET减弱,或MRI上脑结构萎缩。
许多早期发现的AD变异体与它们附近的基因表达水平有关,并与大脑淀粉样变和神经退行性有关。相对而言,较少的研究报告了这些顶级AD风险基因变体与脑部tauopathy的关联,而且这些研究大多集中在一个变体或几个变体上。
更重要的是,在最近的GWAS元分析中发现的新基因变异的精确疾病相关机制仍然是未知的。
藉此,复旦大学的Meng-Shan Tan等人,对目前大规模GWAS研究中排名前30位的非APOE AD风险基因中的变异体与转录物表达水平的关联,以及大脑淀粉样变、tauopathy和神经变性的病理过程的综合分析,使用了与AD相关的CSF、PET和MRI的基线和随访数据。
人脑基因表达数据来自英国脑表达联盟(UKBEC),而其研究中使用的其他数据则来自阿尔茨海默病神经影像倡议(ADNI)队列。
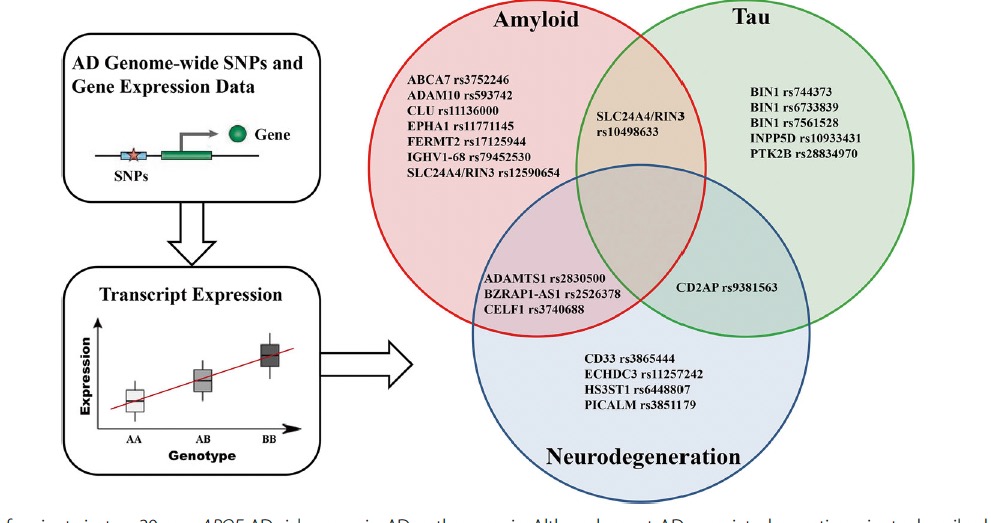
他们研究了AD风险等位基因携带者状态与血液和脑区基因表达水平的关联,并使用多变量线性回归模型测试了与基线时脑淀粉样变、tauopathy和神经退化的关联。他们用混合效应模型分析了这些变体对病理变化率的纵向影响。
他们总共检测到27个变异体与血液和脑区的21个附近基因的表达改变有关。11个变体(尤其是ADAM10、IGHV1-68和SLC24A4/RIN3的新变体)与脑淀粉样变性有关,7个变体(尤其是INPP5D、PTK2B)与脑tauopathy有关,8个变体(尤其是ECHDC3、HS3ST1)与脑神经变性有关。
ADAMTS1、BZRAP1-AS1、CELF1、CD2AP和SLC24A4/RIN3的变体参与了一个以上的脑部病理过程。
他们发现:遗传变异可能在AD发病机制中发挥功能作用并提出潜在机制。
原文出处:
Alzheimer’s Disease Neuroimaging Initiative, Tan MS, Yang YX, et al. Associations of Alzheimer’s disease risk variants with gene expression, amyloidosis, tauopathy, and neurodegeneration. Alz Res Therapy. 2021;13(1):15. doi:10.1186/s13195-020-00755-7



