Nat Commun:“以毒攻毒”,溶瘤病毒增强了对胶质母细胞瘤的抗肿瘤先天免疫反应
时间:2021-10-11 12:01:42 热度:37.1℃ 作者:网络
胶质母细胞瘤(GBM)是最常见和最具侵略性的原发性恶性脑肿瘤。接受标准治疗的GBM患者,包括手术切除、化疗和放疗,其中位生存期约为15个月。由于疾病的早期浸润性,GBM的完全手术切除基本上是无法实现的。GBM对化疗和放疗的内在抵抗力也导致了不良的临床结果。鉴于这些特性,人们迫切需要新的治疗药物来改善GBM患者的治疗效果。

肿瘤溶解病毒(OV)为GBM提供了一种潜在的独特治疗方法,因为它的作用机制与治疗GBM的标准方法完全不同。肿瘤溶解性单纯疱疹病毒-1(oHSV)是最广泛研究的溶瘤病毒之一,经过基因工程设计,它可以选择性地裂解癌细胞,而使正常细胞基本保持不变。像许多其他OVs一样,oHSV也可以激活病人的免疫系统,以攻击肿瘤细胞。
Talimogene laherparepvec (Imlygic)是FDA批准的第一个溶瘤病毒疗法,是基于oHSV载体。在已有的研究中,研究人员发现,oHSV治疗极大地增加了免疫细胞的瘤内浸润。然而,肿瘤细胞已经进化到可以参与免疫检查点,如CD47和PD-L1,并负调节免疫细胞,从而逃避抗肿瘤免疫反应。因此,通过工程设计,使oHSV表达能够增强免疫反应和/或阻断免疫检查点参与的转基因,可能是提高oHSV对GBM整体疗效的一种有效方法。
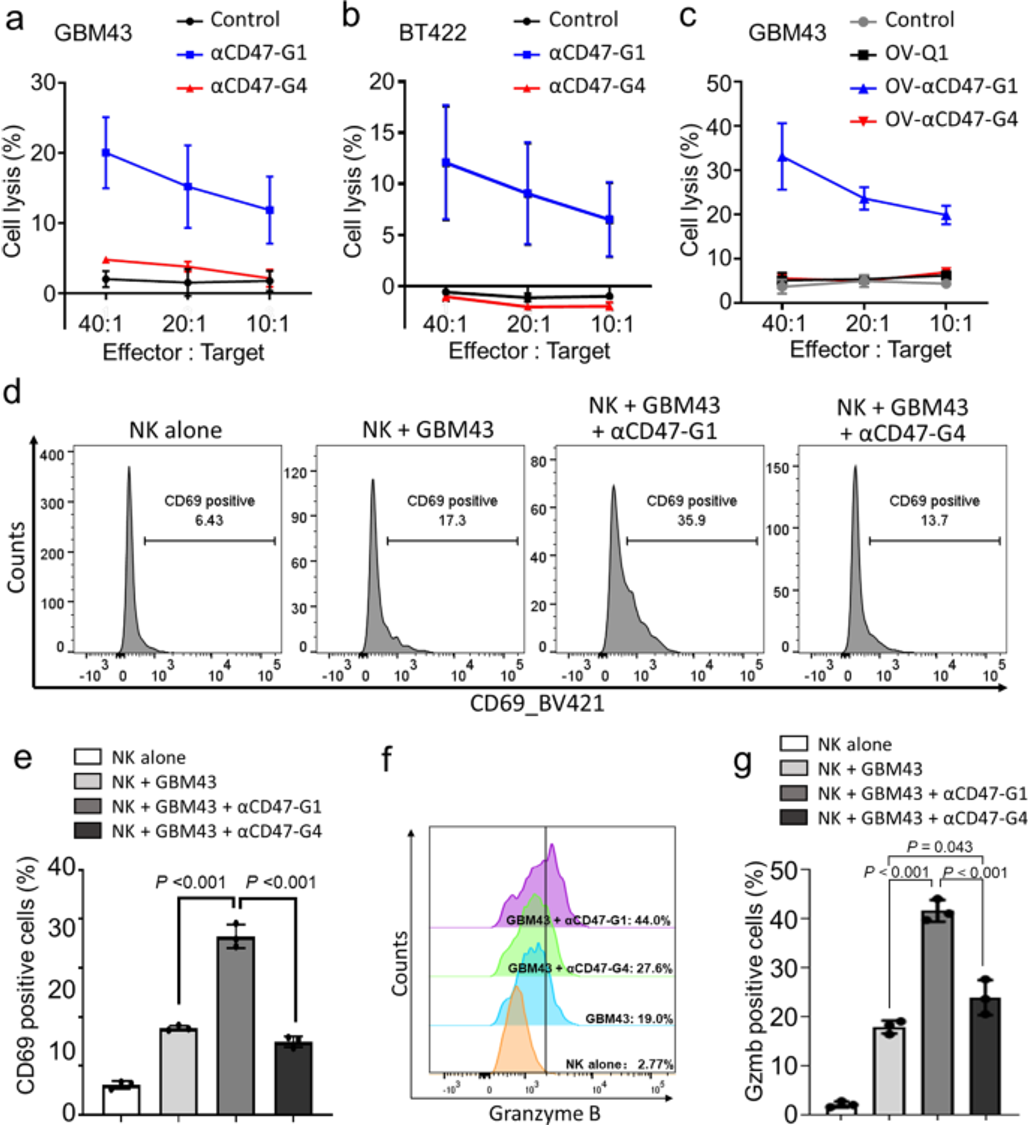
αCD47-G1,而不是αCD47-G4,能诱导人类NK细胞对GBM细胞的细胞毒性。
最近,研究人员构建了一种表达全长抗(α)-人CD47 IgG1或IgG4抗体的溶瘤疱疹病毒,以实现对胶质母细胞瘤的局部控制。由病毒感染的胶质母细胞瘤细胞分泌的抗体可以阻断CD47 "不要吃我 "的信号,而不依赖于亚型;然而,αCD47-IgG1比αCD47-IgG4具有更强的肿瘤杀伤力,这是由于巨噬细胞的额外抗体依赖性细胞吞噬作用和NK细胞的抗体依赖性细胞毒性。
颅内注射的αCD47-IgG1产生的病毒在肿瘤微环境中持续释放相应的抗体,但不进入全身循环;此外,产生αCD47-IgG1的病毒能够更好地提高肿瘤小鼠的生存率。来自免疫能力强的小鼠肿瘤模型的结果进一步证实,巨噬细胞,以及在较小程度上的NK细胞,介导了产生抗体的溶瘤疱疹病毒的抗肿瘤细胞毒性。
总的来说,编码全长抗体的单纯疱疹病毒-1可以改善胶质母细胞瘤的免疫-治疗方法。
原始出处:
Bo Xu al. An oncolytic virus expressing a full-length antibody enhances antitumor innate immune response to glioblastoma. Nature Communications (2021).



