Cancer Discov:阿替利珠单抗(atezolizumab)联合贝伐珠单抗(bevacizumab)治疗恶性腹膜间皮瘤(MPeM)的疗效
时间:2021-07-28 19:01:46 热度:37.1℃ 作者:网络
恶性腹膜间皮瘤(MPeM)是一种罕见的恶性肿瘤,发病率为0·11/100,000,但是恶性程度较高,5年生存低于20%。对于MPeM的治疗,大多数来源于恶性胸膜间皮瘤的治疗或是回顾性研究。目前NCCN治疗推荐培美曲塞联合铂类一线治疗恶性腹膜间皮瘤,但是一线治疗进展后的选择很少。50-60%的MPeM患者表达PD-L1。而且目前免疫检查点抑制剂对恶性胸膜间皮瘤有一定的疗效。因此,有团队开展研究评估PD-L1抑制剂阿替利珠单抗(atezolizumab)联合抗血管贝伐珠单抗(bevacizumab)在恶性腹膜间皮瘤(MPeM)的疗效,相关结果发表在Cancer Discovery杂志上。

研究纳入20例患者,中位年龄63岁,60%为女性,75%患者否认石棉暴露史。其中12例患者(60%)既往除了全身化疗外,还进行了肿瘤减瘤术(CRS)和腹腔热灌注化疗(HIPEC)。所有患者之前都接受过铂联合培美曲塞治疗(只有1例患者之前接受过贝伐单抗),8例(40%)患者在入组前接受过2种治疗。其中17例(85%)患者有疾病进展,3例(15%)不能耐受铂联合培美曲塞治疗。
数据截止时,中位随访23.5个月 (range:10.1-36.1),接受治疗的中位周期数为15周期 (range:4-38) 以及 6 (30%)例患者仍在继续接受治疗。治疗终止的原因为疾病进展(10 [50%]), 毒性 (2 [10%]), 死亡 (1 [5%]) 和退出(1 [5%])。20例可评估患者的客观缓解率(ORR)为40% (95%CI:19.1-64.0) (8/20例患者)。8例应答患者中仍有6例(75%)持续应答,应答时间>10个月。中位持续缓解时间(DoR)为12.8个月。12和18周的疾病控制率分别为95%和85%。中位无进展生存(PFS)为17.6个月(95%CI:9.1-not reached [NR]) ,1年PFS率为 61% (95%CI:35-80)。中位总生存 (OS)在数据截止时尚未达到,1年OS率为85% (95%CI:60-95)。
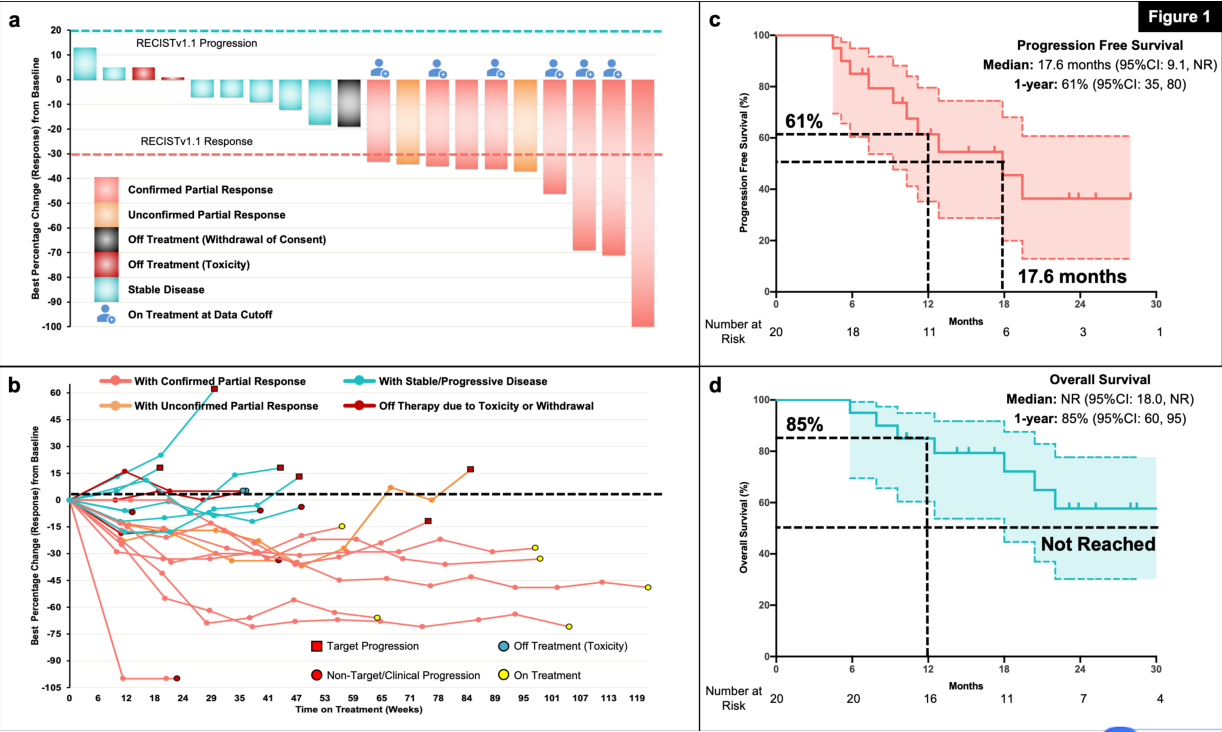
疗效和生存
任何级别的治疗相关不良事件(TRAEs) 的发生率为85%(17/20例)。10例(50%)患者发生3级TRAEs,最常见的是高血压(40%)和贫血(10%)。没有发生4/5级不良事件。2例(10%)患者有3级免疫相关AEs、需要激素治疗的胰腺炎和血小板减少症,最终需要中止治疗。
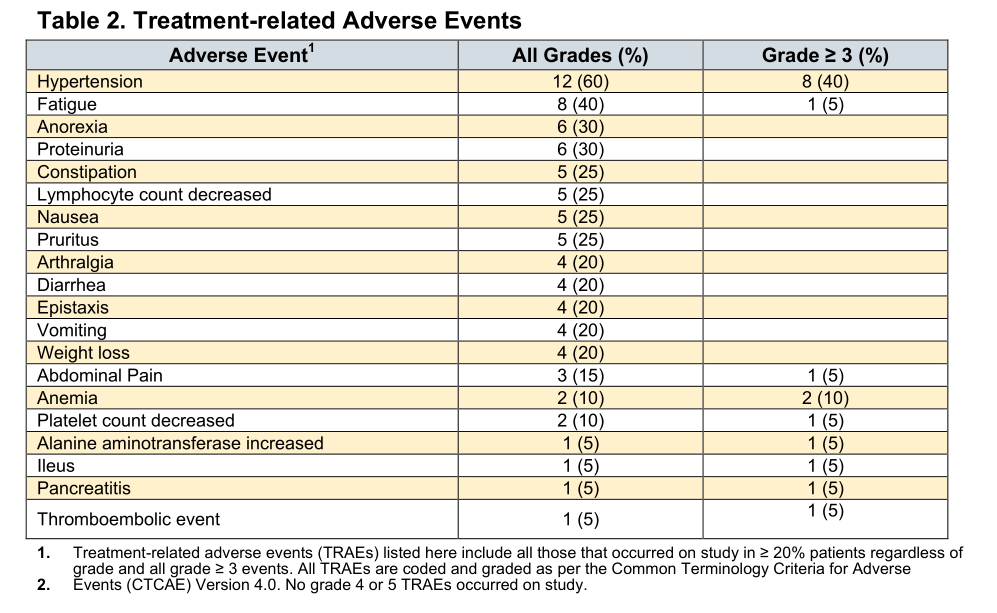
治疗相关不良事件
PD-L1和TMB状态分别在13例(65%)和14例(70%)患者中进行检测。PD-L1表达为0%、1-50%和50%的患者分别有4例(31%)、6例(46%)和3例(23%)。PD-L1阳性和阴性患者中均有应答(44.5% vs. 25.0%; OR= 2.4, 95%CI:0.2-38.0; p>0.99),中位的PD-L1表达水平在应答者和无应答者之间没有差异。中位TMB水平在应答者和无应答者之间没有差异(0.8 vs. 0.8; P=0.83)。应答患者的EMT相关基因集评分较无应答患者的低(中位数:-0.4 vs. 0.8),且与应答程度相关(spearman r: 0.8;95%CI:0.5—-0.9;P = 0.0010)。EMT相关基因的高表达跟较差的ORR相关(14% vs. 86%; OR 0.03, 95%CI:0.0-0.6; P=0.029)。重要免疫效应细胞的密度,如总淋巴细胞(CD3+)、细胞毒性T细胞(CD3+CD8+)、调节性T细胞(FOXP3+)和巨噬细胞(CD68+),以及效应/抑制细胞的比例在应答者和非应答者之间没有显著差异。
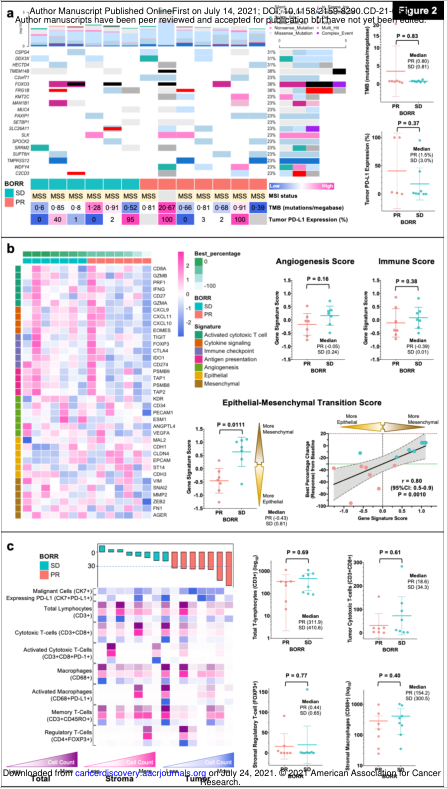
疗效相关生物标志物探索
综上,阿替利珠单抗(atezolizumab)联合贝伐珠单抗(bevacizumab)治疗恶性腹膜间皮瘤(MPeM)具有良好的应答以及耐受性,值得进一步的探索。
原始出处:
Raghav K, Liu S, Overman MJ, et al. Efficacy, Safety and Biomarker Analysis of Combined PD-L1 (Atezolizumab) and VEGF (Bevacizumab) Blockade in Advanced Malignant Peritoneal Mesothelioma. Cancer Discov. 2021 Jul 14:candisc.0331.2021. doi: 10.1158/2159-8290.CD-21-0331. Epub ahead of print. PMID: 34261675.


