【论肿道麻】不同麻醉方式对癌症手术患者长期预后的影响
时间:2025-03-07 12:11:03 热度:37.1℃ 作者:网络
围手术期癌症转移防控这一前沿领域,正引发麻醉学与肿瘤学的深度对话。尽管外科手术仍是多数癌症的最佳治愈手段,但术后转移却成为癌症相关死亡的首要元凶。即使采用精密的手术操作,仍可能存在微小残留病灶的播散风险,而手术应激导致的免疫抑制与炎症激活更为肿瘤细胞逃逸提供了可乘之机。当前主流的麻醉镇痛方案虽能有效维持术中生理稳态,但其对肿瘤转归的潜在影响尚未明确。2025年1月,Lucillia Bezu等人在《Anaesthesia》发表题为《The effect of the type of anaesthesia on long-term outcomes after cancer rep surgery: an arrative review》的综述,通过系统分析2020-2024年间的相关临床前及临床研究,探讨围手术期麻醉和镇痛干预对癌症复发和转移的潜在影响。

大量研究表明,不同的麻醉药物和技术会影响癌症的预后,包括挥发性麻醉剂、丙泊酚全凭静脉麻醉、局部麻醉剂、区域麻醉和阿片类药物。本综述重点关注这五种常用的麻醉方法,并评估它们对癌症进展的潜在影响。
挥发性麻醉药物
多项研究揭示了挥发性麻醉剂潜在的促肿瘤特性:在临床相关浓度下,异氟烷、七氟烷或地氟烷暴露可浓度依赖性增强多种肿瘤细胞的体外增殖能力。其促瘤机制涉及多维度调控,人们提出了许多机制来解释这些肿瘤效应,包括HIF-1a(缺氧诱导因子1a)和PI3K(磷酸肌肽3-激酶)/蛋白激酶B (Akt)/mTOR(哺乳动物雷帕霉素靶点)信号通路的激活,促进肿瘤进展;此外,表观遗传变化,如组蛋白去乙酰化酶6的上调,被假设为在癌变过程中,由于血管内皮生长因子(VEGF)和基质金属蛋白酶(MMP)的下游激活,加速血管新生与肿瘤增殖;此外还包括七氟醚通过降低自然杀伤细胞群2成员D(NKG2D)介导的细胞毒性,削弱机体固有抗肿瘤免疫应答。最新实验证据表明,七氟醚可以通过调节各种类型癌症中的非编码RNA来抑制肿瘤的发生,七氟烷可通过circRNA/miRNA调控网络发挥抗肿瘤作用。在神经胶质瘤中,七氟烷通过下调circ_0012129、circ_0037655等环状RNA对miR-124-3p、miR-34a-5p等微小RNA的海绵吸附作用,恢复这些抑癌miRNA的表达水平,从而抑制肿瘤恶性生物学行为。值得注意的是,挥发性麻醉剂与传统化疗联用可能产生细胞类型依赖性效应:在神经母细胞瘤中,七氟烷可逆转顺铂耐药性;但在食管腺癌细胞中,反而降低对顺铂的敏感性(图1)。
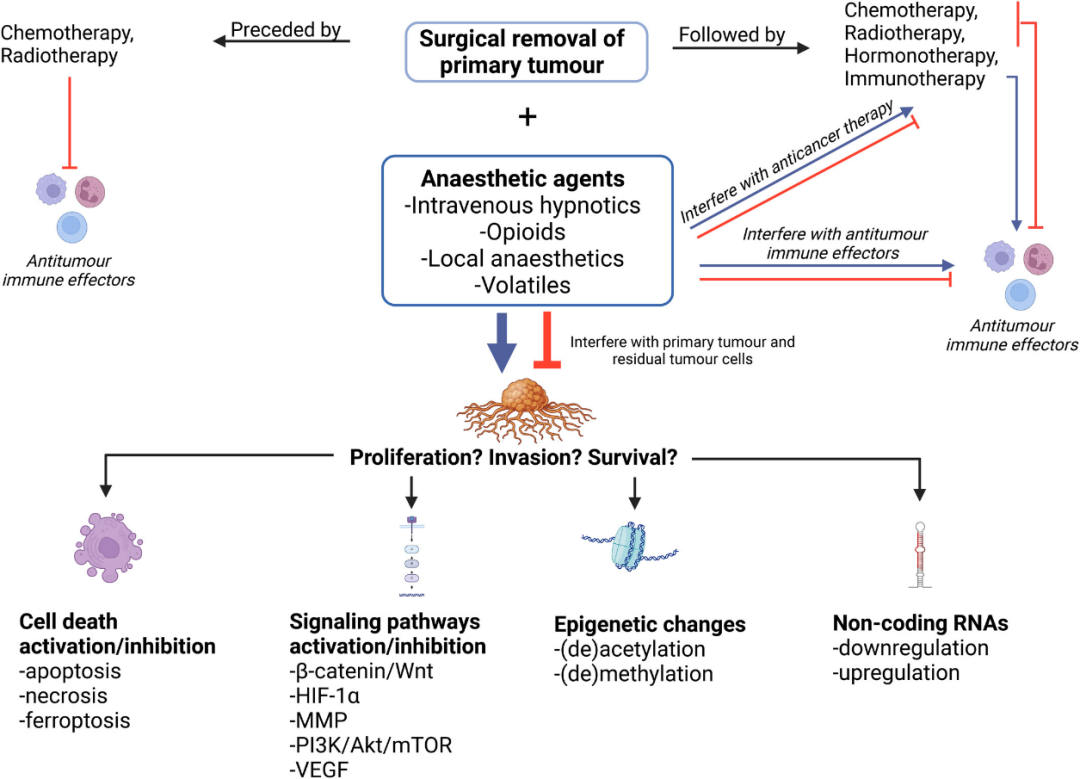
图1:麻醉剂可能诱导抗肿瘤或促肿瘤作用的常见分子机制
丙泊酚全凭静脉麻醉
与挥发性麻醉剂不同,实验室研究普遍支持丙泊酚具有抗肿瘤特性,它可以通过多途径抑制肿瘤细胞存活。在多种化疗耐药肿瘤细胞系中,丙泊酚通过剂量依赖性方式激活内源性及外源性凋亡信号通路来抑制肿瘤细胞的存活,包括蛋白酶水解caspase级联反应或通过促进其他形式介导的细胞死亡,如自噬或铁死亡等非典型的细胞死亡形式。此外,丙泊酚还能抑制肿瘤细胞的转移,如通过增加E-cadherin的表达来阻止恶性细胞的迁移(E-cadherin是一种参与阻止细胞解离的细胞粘附分子)。它还可能通过抑制STAT3/HOTAIR/WIF-1(转录信号转导和激活因子3/HOX基因座转录而来的反义RNA/Wnt抑制因子1)信号轴及其下游Wnt通路、NRF2通路、VEGF受体信号、MEK/ERK(丝裂原活化蛋白激酶/细胞外信号调节激酶)激酶级联反应、mTOR/eIF4E(真核生物翻译起始因子4E)翻译起始调控网络等,全面阻断肿瘤细胞存活、侵袭与转移。此外,异丙酚可降低对5-氟尿嘧啶的耐药性(通过减少双调节蛋白的分泌);增强顺铂的敏感性(通过抑制炎症因子NF-kB核转位)和提高替莫唑胺的疗效(通过抑制巨噬细胞活化和HIF-1a表达)等。丙泊酚还增强了紫杉醇和阿霉素的细胞毒性作用,上调抑癌蛋白p53表达和下调铁死亡抑制蛋白FSP1(成纤维细胞特异性蛋白1)表达水平(图1),进一步证明了丙泊酚的化疗增敏效应。
临床观察性研究的矛盾发现:
观察性临床研究通常基于大型数据库,如国家或国际登记处,其中有大量接受手术切除特定肿瘤的患者,他们以非随机方式接受吸入麻醉或基于异丙酚的TIVA,其研究结果呈现异质性。丹麦的一项研究发现,8700例结直肠癌手术队列显示,与吸入麻醉相比,丙泊酚组复发风险较吸入组轻微降低(风险比1.12,95%CI 1.02–1.23,p=0.05);在瑞典的一项回顾性研究中,7500例膀胱癌手术登记研究未发现麻醉方式对总生存期的影响[14];在另一项瑞典更广泛的回顾性、倾向性评分匹配研究中,对13873名接受乳腺癌手术的患者进行了研究,在肿瘤学结局方面显示肿瘤预后无组间差异;此外,一项规模最大的、基于日本登记的回顾性分析(n = 196303)表明,丙泊酚和七氟醚在消化道肿瘤手术中总生存期无差异(总生存风险比1.02,95%CI 0.95-1.09,p = 0.65),但在工具变量分析中,丙泊酚与无复发生存率的改善存在微弱关联(风险比0.92,95%CI 0.87-0.98, p = 0.01)。
随机对照试验的否定性结论:
观察性研究从未证实麻醉技术与癌症结局之间存在因果关系。由于前瞻性随机对照试验(RCT)需要长时间(长达5年)的随访,因此具有挑战性。现有的研究均未证实丙泊酚的生存优势。在CAN-study对1,670例乳腺癌/结直肠癌根治性手术患者5年随访显示,丙泊酚全麻与七氟醚全麻的总生存率无差异(风险比0.97,95%CI 0.72-1.29, p = 0.829)。另一项随机试验,对1228例老年肿瘤大手术患者(大于65岁)长期随访研究(中位43月)同样无生存差异(校正风险比1.02,95%CI 0.83–1.26,p=0.834)。同样,迄今最大规模的一项研究麻醉技术与乳腺癌复发的随机对照试验证实,在2100名接受区域阻滞联合丙泊酚TIVA与吸入麻醉的肿瘤患者中,癌症复发率相当。
Meta分析的启示与局限:
对现有数据进行进一步的尝试,通过荟萃分析综合不同的结果。其中一项分析包括42项回顾性队列研究和两项随机对照试验。它指出,回顾性数据支持丙泊酚改善总生存期,但多中心研究未能复现(总生存期风险比0.98,95%CI 0.94–1.03,p=0.51;无复发生存期风险比0.95,95%CI 0.87–1.04,p=0.26)[20]。此类综合证据价值有限。在这一点上,目前对于丙泊酚或吸入麻醉的RCT谁更有优势缺乏合理依据(图2)。
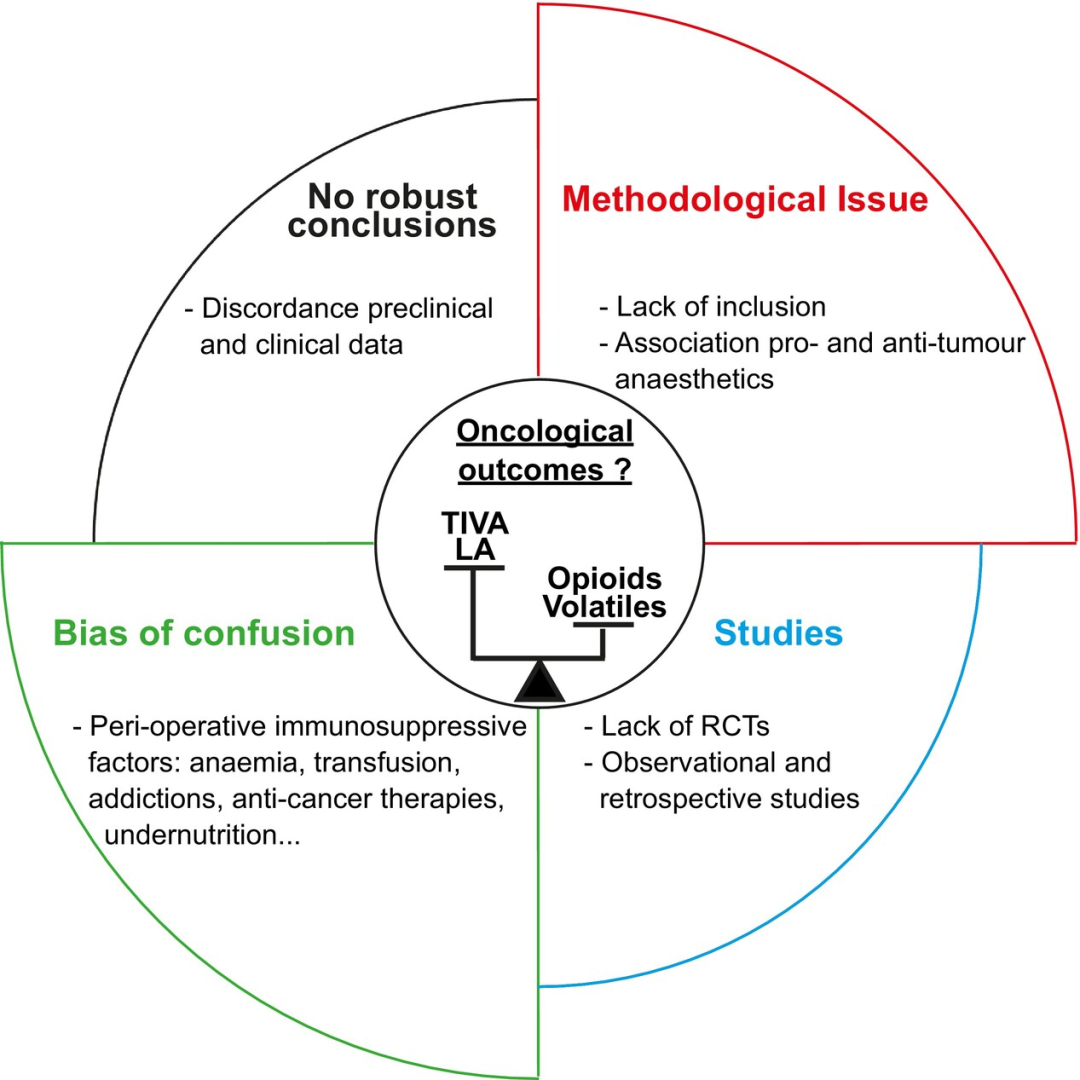
图二:临床研究概述
局部麻醉药物
实验研究表明,酰胺类局部麻醉药具有抗肿瘤效应。其作用机制包括直接与间接抗肿瘤途径。
直接细胞毒性作用:
酰胺类局部麻醉剂通过激活细胞凋亡和铁死亡信号通路诱导肿瘤细胞死亡。局部麻醉剂引发癌细胞线粒体毒性,改变跨膜电位,阻断呼吸链和ATP合成,产生活性氧(ROS)、释放促凋亡分子(Bax、Bak、细胞色素c)来促进肿瘤细胞死亡。此外,局部麻醉剂对肿瘤细胞的直接作用还涉及通过多种分子机制在体外抑制肿瘤细胞增殖、侵袭和迁移,通过抑制细胞周期蛋白使细胞周期停止;改变细胞内Ca2+水平进而改变细胞骨架;靶向致癌相关的非编码RNA和DNA甲基转移酶;干扰基质金属蛋白酶(MMP 2/9)介导的细胞外基质侵袭;抑制PI3K/Akt/mTOR致癌信号轴;并减少促血管生成因子VEGF分泌。在动物模型中,酰胺类局麻药可抑制实体瘤生长、降低远处转移率并延长生存期。
免疫调节效应:
此外,局部麻醉通过增强免疫系统介导间接抗肿瘤作用。由于其抗炎和镇痛特性,局部麻醉剂抑制了伤害感觉信号通路的激活,减弱了手术应激诱导的促皮质轴的刺激,进而抑制肿瘤细胞膜α-肾上腺素受体介导的儿茶酚胺促增殖效应。局部麻醉药还可以降低糖皮质激素的释放,保护自然杀伤细胞(NK细胞)与T细胞等的抗肿瘤免疫效应功能。此外,局部麻醉可诱导癌细胞内质网应激和自噬,导致损伤相关分子模式(DAMPs)的释放,然后损伤相关分子模式招募并刺激宿主-树突状细胞,进而吞噬肿瘤抗原并将其暴露于T细胞,活化的T细胞浸润肿瘤床及其微环境,释放细胞因子干扰素-γ并建立抗肿瘤免疫记忆(图1)。利多卡因治愈的肿瘤小鼠在再接触癌细胞时不再产生肿瘤可证实这一观点。
临床转化突破:
1.肿瘤局部浸润
有趣的是,一些体内实验数据观察到局部麻醉可以增强抗肿瘤治疗,可能是通过使肿瘤细胞对免疫原性和非免疫原性药物(如紫杉醇)、5-氟尿嘧啶、阿霉素、铂盐、蛋白激酶抑制剂、或去甲基化剂5-aza-20-脱氧胞苷敏感(图1)。利多卡因(0.5%)围手术期肿瘤周围浸润可影响乳腺癌手术患者长期肿瘤预后,这是第一个表明单次围手术期干预对长期癌症预后有积极影响的实例。在印度进行的一项大规模多中心RCT研究中,有近1600名接受乳腺癌手术的女性可入组,随机将患者分为两组,一组在手术切除前7-10分钟对肿瘤周围浸润利多卡因(0.5-4.5mg.kg-1体重),另一组未干预。中位随访时间超过5.5 y(68个月)。利多卡因组5年后无病生存率为87%,对照组为83%(风险比0.74,95%CI 0.58-0.95, p = 0.017)。同样,利多卡因组患者的5年总生存率为90%,对照组为86%(风险比0.71,95%CI 0.53-0.94, p = 0.019)。利多卡因的有益效果在各个亚组中是一致的,包括绝经期;肿瘤大小;淋巴结转移;激素受体状态;以及人表皮生长因子受体2状态。该研究未报道利多卡因的不良反应。
腹腔注射罗哌卡因的初步研究结果也令人鼓舞。一项前瞻性RCT研究,40名卵巢癌妇女接受开放式腹部卵巢癌瘤体减灭术,随机分配患者围手术期接受罗哌卡因或生理盐水(安慰剂)腹腔浸润。研究发现,术后72小时罗哌卡因腹腔浸润可显著缩短肿瘤治疗的预期康复指标RIOT(因肿瘤治疗返回就医,该指标用于评价患者在术后阶段是否“恢复”到足以耐受术后辅助治疗)时间,从对照组的29(21 - 40[13-49])天减少到罗哌卡因组的21(21 - 29[8-35])天(p = 0.021),表明患者对化疗的准备状态提高。这一发现值得进一步研究。
2.静脉输注探索:
关于静脉注射利多卡因,其在肿瘤治疗中的价值仍有待确定。一项涉及2239例接受胰腺癌手术的患者的回顾性研究表明,静脉输注利多卡因可显著提高1年(68%对63%,p < 0.001)和3年(34%对27%,p = 0.011)患者的总生存率。在该特定疾病的第一项前瞻性RCT中,563名胰腺癌患者在手术切除期间接受围手术期静脉注射利多卡因与安慰剂的对比,发现3年随访时总生存率和无病生存率未受影响。
但是,静脉注射利多卡因可能对其他类型的癌症有益,因为胰腺癌是具有侵袭性且对治疗反应差的类型。小型随机对照试验表明,静脉注射利多卡因可能影响癌症预后。68名接受乳腺癌手术的患者在围手术期随机分配接受静脉输注利多卡因或安慰剂。该研究检测了手术前后的自然杀伤细胞和T细胞亚群,发现利多卡因与自然杀伤细胞和T细胞免疫功能的保存作用有关,这表明利多卡因具有潜在的抗癌作用。另一项150名计划进行结直肠癌手术的患者的试点研究随机分配接受七氟醚麻醉,同时接受或不接受48小时利多卡因输注。静脉输注利多卡因组加速了患者术后恢复,改善了患者的术后活动(p = 0.001)。此外,它还降低了1年癌症复发率(p = 0.03),但未改善1年生存率(p =0.22)。
因此,现有证据提示,利多卡因通过调控肿瘤微环境可能产生抗癌作用。鉴于不同实体瘤的敏感性差异,亟待开展多中心随机对照试验(RCT)以进一步评估。
区域麻醉
早期一项针对接受乳房切除术及腋窝淋巴结清扫患者的回顾性分析显示,椎旁区域麻醉与无复发生存期的延长存在关联,由此学界曾推测区域麻醉可能改善乳腺癌复发预后,但高质量RCT证据否定了区域麻醉对肿瘤预后的特异性影响。
乳腺癌手术(n=2100):该领域的随机对照试验纳入了2100例在椎旁镇痛联合丙泊酚全凭静脉麻醉下行乳腺肿瘤切除术的女性患者,结果显示其3年随访期间的复发率约为10%,与吸入麻醉联合阿片类镇痛组无显著差异。
亚组分析(按雌激素受体状态):一项亚组研究进一步分析了区域麻醉与全身麻醉对早期乳腺癌复发的潜在影响(基于雌激素受体状态分层),发现两组间复发率无统计学差异(19% vs. 23%,校正风险比0.80,95%CI 0.50-1.30,p=0.38)。三项其他随机对照试验:分别针对1712例腹部肿瘤患者、400例肺癌患者和221例结直肠癌患者,均证实硬膜外联合全身麻醉与单纯全身麻醉相比,在总生存期或肿瘤特异性结局上无显著差异。
证据整合与共识:尽管针对该主题的系统综述与Meta分析持续发表,但若原始研究本身无法确立麻醉技术与癌症转归的因果关系,仅汇总回顾性研究数据(无论样本量大小或统计分析质量如何)的科学价值有限。四项关键RCT已充分证明,在肿瘤手术中区域麻醉与吸入麻醉的长期影响相似,此问题似已形成定论(图2)。
阿片类药物
作为肿瘤治疗与术后镇痛的核心药物,阿片类药物的潜在促癌效应引发广泛关注。阿片类药物是肿瘤治疗中应用最广泛且高效的镇痛剂,亦是术后镇痛(包括肿瘤切除术后)的核心药物。
实验室证据的双面性
促肿瘤机制:有观点认为围术期治疗剂量的阿片类药物可能通过非预期途径增强肿瘤细胞生物学活性,进而增加复发风险。实验室证据显示,阿片类药物在体外可促进多种癌细胞增殖与扩散,并在三阴性乳腺癌异种移植小鼠模型中通过激活PI3K/Akt信号通路及其下游靶基因mTOR与c-Myc,加速转移灶形成。吗啡还可抑制抗血管生成基因TSP-1,促进肿瘤生长所需的新生血管生成,并通过激活MMP9增强远端器官侵袭能力。此外,吗啡具有免疫调节特性,可减弱抗PD-L1免疫治疗及多柔比星等化疗药物的作用,从而降低传统抗肿瘤疗法的疗效及其诱导远端效应(abscopal effect)与免疫记忆的能力。远端效应指针对某一部位肿瘤的抑制性治疗对其他未治疗部位的肿瘤亦产生抑制作用,其机制可能与治疗释放的免疫活性分子有关,这些分子不仅作用于远处肿瘤,还可形成免疫记忆以防止肿瘤复发(图1)。
抗肿瘤潜力:曲马多与舒芬太尼等阿片类药物可能具有抗肿瘤效应。在胰腺导管腺癌的体内外模型中,曲马多通过μ-阿片受体降低炎性细胞因子与增殖标志物(Ki-67、细胞周期蛋白),同时增加抗肿瘤M1型巨噬细胞。舒芬太尼联合帕瑞昔布(COX-2选择性抑制剂)可下调细胞周期蛋白、MMP、VEGF及致癌标志物(Snail),从而抑制人表皮生长因子受体2阳性乳腺癌细胞的增殖与存活,并在原位小鼠模型中显著延缓肿瘤生长与转移发生。
临床研究的矛盾性结论
现有临床证据对阿片类药物是否影响癌症转归呈现复杂结果,需注意多数研究为观察性设计。尽管阿片类药物通常被认为具有免疫抑制作用,可能无意中促进癌症复发或进展,但术后疼痛本身亦具有免疫抑制与促瘤特性,因此阿片类通过缓解急性疼痛或产生保护性抗癌效应。此外,由于多种肿瘤表达阿片受体,药物可能通过直接作用于肿瘤细胞影响转归。对不同肿瘤切除组织的基因组分析表明,阿片类药物的整体效应可能呈抗癌或促癌性,取决于特定肿瘤的基因表达谱。
潜在获益证据:术中高剂量阿片类药物使用与部分肿瘤转归改善的关联可能与肿瘤内阿片受体差异表达有关。首项针对1143例三阴性乳腺癌患者的回顾性分析发现,术中阿片类用量较高者无复发生存期更优,且与促瘤/抑瘤受体表达相关。另一项针对1-4期肺腺癌患者的回顾性研究显示,特定基因表达背景下,术中高剂量阿片类可改善转归,而其他基因型则预后恶化。此外,一项结直肠癌手术观察性研究提示术中高阿片类用量与复发率降低相关。
中性或负面结果:其他研究未发现阿片受体表达与癌症转归的关联。基于癌症基因组图谱中8000余例样本的大规模分析显示,阿片受体表达与转归无相关性。一项针对366例卵巢癌手术患者的回顾性研究中,μ-阿片受体表达与总生存期或无病生存期无关。另有一项回顾性研究纳入239例肝细胞癌患者,术后吗啡需求较高者的总生存期略差,但复发率与低剂量组相似。一项针对146名患者的随机对照试验表明,使用阿片类药物麻醉和不使用阿片类药物麻醉,在生化指标上前列腺癌复发情况并无差异(P=0.54),但该研究样本量不足,无法充分证实这个结论。
现有临床证据主要基于回顾性研究,混杂因素(如疼痛强度、肿瘤异质性、合并用药)难以完全校正。尽管初步数据显示阿片类效应具有肿瘤类型与分子分型依赖性,但目前仍缺乏阿片类影响癌症转归的强证据,未来需通过精心设计的大规模前瞻性RCT明确围术期阿片类是否真正影响癌症长期转归(图2)。
结论
近20年来,一些实验室与观察性临床数据提示麻醉可能会影响癌症转归。现有科学理论支持酰胺类局麻药与丙泊酚的抗肿瘤作用,但新出现的随机试验显示麻醉技术对癌症转归呈中性影响。唯一的例外是一项关于肿瘤周围注射利多卡因的单中心试验显示其可改善乳腺癌患者术后5年的预后,但此孤立性发现需进一步验证方可改变临床实践。当前,若某种治疗相对安全且符合临床指征,应常规用于癌症患者,无需考虑对癌症预后的潜在影响。目前,没有哪种麻醉或镇痛药物及技术是癌症患者绝对不能使用的,也没有哪种技术被明确证实对肿瘤学预后有益。


