【衡道丨病例】病理诊断——炎性纤维性息肉
时间:2025-02-28 12:11:15 热度:37.1℃ 作者:网络
临床资料
患者女,年龄61,2023年1月主因“头晕、乏力1月,排黑便3天”,就诊我院,门诊行相关检查后予以收住入院治疗。入院后积极完善各项辅助检查,血常规提示患者重度贫血症,在排查病因、积极改善贫血的同时,予进一步完善胃肠镜检查。
胃镜提示:胃窦黏膜呈红白相间,以红为主,后壁见巨大肿物凸向腔内(图1),直径约5.3cm,表面糜烂,蠕动尚可,肿物周围的胃黏膜隆起,内镜初步诊断考虑胃窦间质瘤?伴出血。
CT平扫示胃窦黏膜下层见低密度病灶区域,结节状,呈息肉样突出腔内,增强后病变呈中度不均匀强化,内见不规则片状低密度影。
因肿物较大,考虑消化内镜下切除创面大、出血严重以及不易完整切除等因素,遂经科室讨论后拟定行腹腔镜下胃部分切除术。患者在抑酸护胃、输血纠正贫血等对症支持治疗一周,排除手术禁忌、复查血红蛋白基本正常后行手术切除肿物。
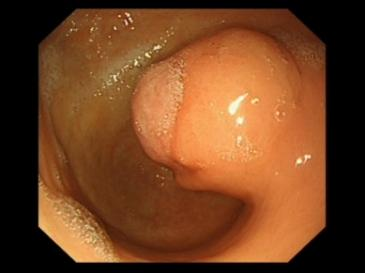
图1 内镜下示胃窦后壁巨大肿块,凸向腔内,肿物周围的胃黏膜隆起
大体检查
病理送验标本大体示灰红色肿物一个,大小5.3X4.8X3.8cm,表面灰红色,光滑,肿块外周附一圈胃黏膜(图2),切面灰黄灰红色,质地细腻,胃黏膜灰黄色,有皱襞。
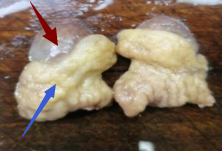
图2 灰黄灰红色肿物一个,大小5.3X4.8X3.8cm,表面灰红色,光滑,肿块外周附一圈胃黏膜(红色箭头示肿物,蓝色箭头示肿物外周附胃黏膜)
镜下所示
低倍镜下示瘤组织位于黏膜下层,并向上累及黏膜,部分黏膜上皮坏死脱落,形成溃疡(图3-1),溃疡周边及深部可见组织水肿,瘤细胞呈星芒状、短梭形围绕血管排列(图3-2),呈旋涡状/洋葱皮样(图3-3),背景中可见网状纤维和胶原纤维混杂分布,并可见大量炎细胞浸润,以嗜酸性粒细胞为主(图3-4)。高倍镜下示肿瘤细胞形态温和,均匀一致,细胞核胞核染色质细腻,未见明确核分裂象。
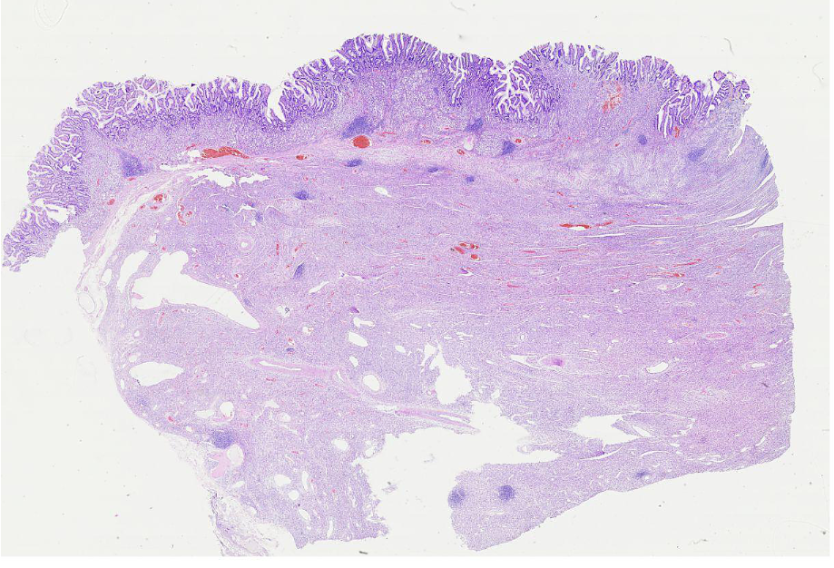
图3-1 瘤组织位于黏膜下层,并向上累及黏膜,部分黏膜上皮坏死脱落(HEx100)
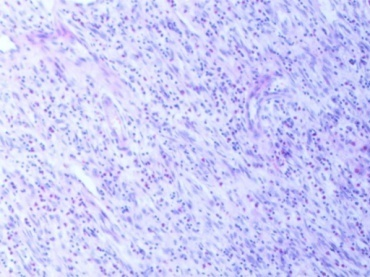
图3-2 瘤细胞呈星芒状、短梭形(HEx100)
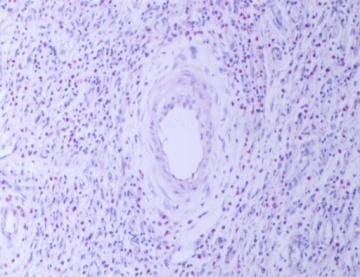
图3-3 肿瘤细胞围绕血管呈旋涡状/洋葱皮样排列(HEx100)
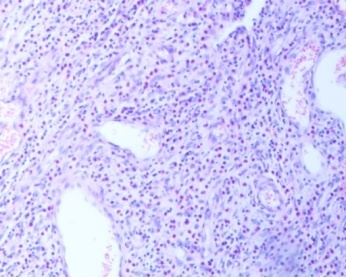
图3-4 可见大量炎细胞浸润,以嗜酸性粒细胞为主(HEx100)
免疫组化:
CD34(+)(图3-5),SMA(1A4)(平滑肌+)(图3-6),CD68(组织细胞+),CD117(-)(图3-7),S100(-)(图3-8),DOG1(-),STAT6(灶+),AE1/AE3(-),ki67增殖指数低(+2%)。
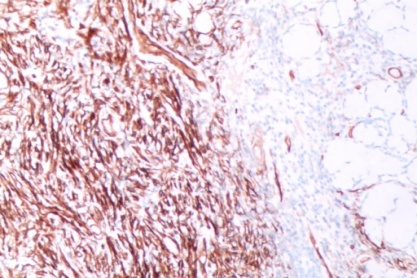
图3-5 CD34肿瘤弥漫阳性,周边胃黏膜未见表达(SPx100)
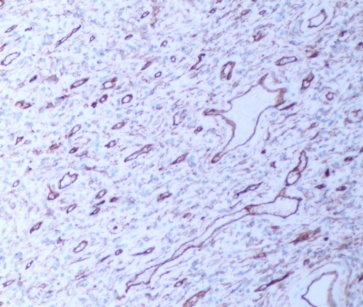
图3-6 SMA平滑肌阳性(SPx100)
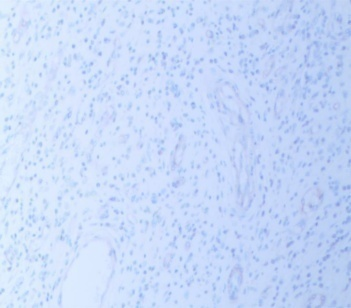
图3-7 CD117阴性(SPx100)
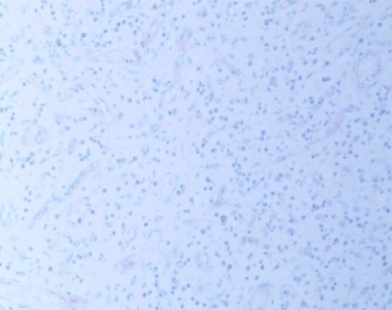
图3-8 S100阴性(SPx100)
最终诊断
胃窦炎性纤维性息肉。基因检测结果未查见PDGFRA基因突变。
讨论
炎性纤维性息肉(inflammatory fibroid polyp,IFP)是好发在胃肠道中罕见的良性间叶源性肿瘤,发病率极低、国内少有大宗病例报道[1-2],故临床医师对IFP多认识不足,较易误诊为胃肠间质瘤等其他疾病。
临床特征:
IFP内镜外观多表现为半球形隆起的病变,多数病灶最大径<5cm,原则上可首选内镜下切除治疗。IFP病因不明、发病机制也尚未阐明,由Helwing和Ranier在1953年首先以IFP的名称报道[3],IFP>4cm被命名为巨大炎性纤维性息肉,而>5cm的更为罕见。本身IFP的临床表现、病理及内镜特征与发生在消化系统黏膜下的肿瘤、及非肿瘤疾病十分相似,所以该病极易误诊。IFP好发于成年女性(平均在55岁),发病部位可在整个消化道,常见的部位是胃,其次是小肠、食道、结肠、直肠和阑尾[4-5],其临床症状与IFP发生位置及大小密切相关,发生在胃肠道IFP患者,会出现消瘦、贫血、黑便等症状,且治疗方式的选择也取决IFP的位置、大小及生物学特性。我院此例就以重度贫血、黑便入院,全面查体后,建议胃肠镜探查遂发现胃窦后壁巨大占位性病变,因肿物巨大,综合考虑建议采取腹腔镜下手术切除。最终病理诊断结合免疫组化示胃窦炎性纤维性息肉,患者贫血、黑便的“元凶”就是它,分析其原因可能是此例IFP体积巨大,经胃消化的食物与其反复摩擦,导致其表面黏膜糜烂、慢性渗血有关。目前,关于IFP病因的起源存在两种学术观点[6]:观点1认为IFP来源于肌纤维母细胞,观点2认为IFP源于树突状细胞。
镜下特征:
镜下病理特征示肿瘤无包膜,位于黏膜下层,并延伸至全黏膜层,表面糜烂,上皮缺失,瘤细胞形态温和、分布均匀,呈短梭形、星芒状增生,肿瘤间质疏松、水肿,内可见大量的嗜酸性粒细胞浸润,可见大小不等、厚薄不均的血管和纤细胶原纤维素增生;并可见瘤细胞围绕血管呈“旋涡状/洋葱皮”样同心圆状排列结构。
免疫组化特征:
免疫组化表型:CD34、SMA、Vimentin阳性表达,不表达CD117、S100、DOG1、STAT6、AE1/AE3。
分子遗传学特征:
分子遗传学:55%的IFP分子可查见PDGFRA基因突变,胃的炎性纤维性息肉主要是PDGFRA基因18号外显子突变[7]。
治疗和预后
IFP的治疗方式有外科手术、内镜切除。一般内镜切术多以小的肿瘤(<2cm)为主,假若肿物体积较大、发生位置较深,外科手术切除则为第一首选,避免过大肿瘤采用内镜切除造成的大出血等并发症,切除彻底极少数复发,未见远处转移报道,本例患者术后半年复查CT,一年复查胃镜均未发现异常,术后恢复良好,暂无复发迹象,(随访至2023年底)。
鉴别诊断
1、胃肠道间质瘤:
IFP与胃肠道间质瘤的免疫组化标记、及基因突变有部分重叠,如果病理诊断医生经验不足,就会误诊为胃肠道间质瘤,从而导致临床的过度治疗。本例临床术前及术中就拟诊为间质瘤,患者术前虽然在胃镜探查时行了病理活检,但因其肿物巨大,仅在黏膜表面和糜烂交界处多点取材,但病理结果并无特异性发现,仅提示慢性浅表性胃炎改变,故术前未能明确肿物性质,临床医师结合患者症状等表现考虑间质瘤可能性大。故IFP的明确诊断需依赖手术病理,而内镜下小标本的组织学活检对确诊的价值有限,其原因在于因内镜活检取材有限,不能全部取材,所以多数病理报告均提示慢性浅表性胃炎、萎缩性胃炎等非特异性表现。而当内镜下EMR/ESD整体切除或者胸腔镜下手术切除标本时,临床则较易误诊的为息肉、腺瘤、神经鞘瘤、胃肠道间质瘤(GIST)等,尤其是GIST,二者具有相似的好发年龄、发病部位、胃镜形态,尤其在遇到肿瘤细胞弥漫表达CD34的病例,诊断医生较易诊断为CD117-/CD34+的间质瘤,且两者肿瘤镜下都由梭形细胞组成,但IFP的肿瘤细胞形态比GIST的短、纤细而稀疏,同时IFP梭形肿瘤细胞围绕血管排列呈旋涡状/洋葱皮样、及间质多有血管及大量嗜酸性粒细胞等特点,此外,免疫表型肿瘤细胞只表达CD34,而CDll7和Dog-1不表达,均可以帮助IFP的诊断。日常诊断中对于直径较小的病例,内镜医师镜下钳取要想到有IFP的可能,而病理医生则要仔细观察其形态特点,避免误诊。
2、炎性肌纤维母细胞瘤
(inflammatory myofibroblast tumor,IMT):
该病好发年龄在20岁的女性,好发在网膜、腹腔等腹部软组织,光镜下IMT肿瘤细胞呈束状、编织状、席纹状的排列,显著与IFP瘤细胞的排列不同,且间质多以淋巴细胞和浆细胞浸润为主,有时浸润的淋巴细胞可聚集呈生发中心样,偶尔间质也可见组织细胞样细胞或节细胞样大细胞浸润其内,免疫组化表达ALK而IFP不见其表达,虽然本例与IFP形态学有类似之处,但免疫组化不支持。
3、神经鞘瘤:
此肿瘤多为边界清楚的有完整包膜的实性肿块,光镜下特征性病变示肿瘤细胞具有丰富的束状/栅栏状区(Antoni A区)和疏松黏液样的网状区(Antoni B区),且两种形态交替组合,间质多具有不规则的厚壁血管、常发生出血、囊性变,且肿瘤周围多见淋巴细胞套围绕,此特点易与IFP鉴别。免疫组化示肿瘤表达S-100、Sox-10、CD56等。
4、平滑肌瘤:
此病变多发生在食管而IFP常发生在胃肠道,多在壁内生长,平滑肌瘤的瘤细胞成束或编织状排列,与正常平滑肌细胞形态相似,瘤细胞呈梭形、核呈长杆状、且两端钝圆,胞质呈嗜伊红色,间质内无IFP特征性的纤维母细胞围绕血管形成洋葱皮样结构、和嗜酸性粒细胞浸润,免疫组化表达SMA、Desmin、Actin、H-caldesmon等,不表达CD34,本例形态及免疫组化均不支持。
5、滤泡树突细胞肿瘤
(follicular dendritic cell tumor,FDCT):
此肿瘤瘤细胞呈梭形、卵圆形,有时细胞可成合体细胞样,呈弥漫片状、交错的束状、席纹状排列,可形成车辐或漩涡状结构,但瘤细胞有异型性,可与IFP鉴别。此外间质内可见大量淋巴细胞和浆细胞而少见嗜酸性粒细胞浸润也是与IFP鉴别的要点,免疫组化表达表达CD21、CD23、CD35。
参考文献及书籍
[1]牛朝荣,李道明.胃肠道炎性纤维性息肉28例临床病理学分析[J].实用医学杂志,2018,34(2):289-292
[2]刘丹,王坚,陈淼,等.胃肠道炎性纤维性息肉37例临床病理学观察[J].中华病理学杂志,2016,45(6):381-386DOI:10.3760/cma.j.issn.0529-5807.2016.06.006.
[3]Vanek J,Gastric submucosalgranulomawitheosinophilic infiltralion [J].Am J Pathol,1949,25(3):397-411
[4]武迪,祁晓莉,乔星,等.回肠浸润性炎性纤维性息肉临床病理观察[J].诊断病理学杂志,2022,29(7):635-639 DOI:10.3969/j.issn.1007-8096.2022.07.015
[5]沈国菊,徐嘉忆,彭川,等.消化道炎性纤维性息肉临床病理分析[J].医学信息,2019,32(22):43-46.DOI:10.3969/j.issn.1006-1959.2019.22.053.
[6]彭芳,张功亮,王建,等.胃肠道炎性纤维性息肉5例临床病理分析[J].临床与实验病理学杂志,2019,35(12):1477-1478.DOI:10.13315/j.cnki.cjcep.2019.12.023.
[7]孙琦,孟凡青,樊祥山.炎性纤维性息肉发病机制的研究进展[J].国际病理科学与临床杂志,2011.DOI:CNKI:SUN:WYSB.0.2011-05-022.


