Nat Commun:殷青青/陆林/郝峻巍合作研究证明SGK1驱动小鼠海马脱髓鞘和糖尿病相关认知功能障碍
时间:2025-02-27 12:33:28 热度:37.1℃ 作者:网络
糖尿病相关认知功能障碍(DACD)越来越被认为是糖尿病的关键并发症。DACD的复杂病理学仍然未知。
2025年2月17日,山东省立医院神经内科殷青青、北京大学陆林、首都医科大学郝峻巍共同通讯在Nature communications 上在线发表题为“SGK1 drives hippocampal demyelination and diabetes-associated cognitive dysfunction in mice”的研究论文。研究进行了单核RNA测序(snRNA-seq),以证明糖尿病小鼠模型中海马体的独特细胞和分子模式。
对少突胶质细胞(OLs)的更深入分析区分了5个子簇,表明OLs的不同功能状态和每个亚簇中的转录变化。基于snRNA-seq和体内实验的结果,研究观察到雄性糖尿病小鼠的脱髓鞘和少突胶质细胞谱系细胞组成的不协调。血清/糖皮质激素调节激酶1(SGK1)在雄性糖尿病小鼠海马OLs中的表达显著增加,海马SGK1敲低通过N-myc下游调节基因1(NDRG1)介导的通路逆转脱髓鞘和DACD。研究结果说明了海马OLs的转录景观和DACD中证实的髓鞘形成受损。研究结果提供了直接证据,表明抑制SGK1或促进髓鞘形成可能是DACD的潜在治疗策略。

由于糖尿病(DM)患病率上升和复杂的并发症,糖尿病(DM)已成为一个全球性的公共卫生问题。糖尿病相关认知功能障碍(DACD)很常见,但在DM的各种并发症中很容易被忽视。流行病学研究已确定,与非糖尿病个体相比,DM参与者发生全因认知障碍的风险更高(约20%至60%)。DM个体,尤其是2型糖尿病(T2DM)个体的认知功能障碍主要表现在记忆力、执行功能、处理速度、注意力等认知领域。DACD的病因是多因素的。然而,一项随机临床试验表明,控制血糖的标准治疗策略对T2DM诱导的认知能力下降的有益影响有限。因此,阐明DACD的病理机制并探索有效的预防和治疗策略是当务之急,需要采取进一步行动。
高血糖、胰岛素缺乏和肥胖引起的有髓神经纤维丢失被认为是糖尿病神经病变发生和发展的驱动力,尤其是在周围神经中。过去十年的新证据表明,脱髓鞘也参与了临床和实验糖尿病研究的中枢神经系统(CNS)。此外,人们已广泛认识到髓鞘和少突胶质细胞谱系细胞对调节认知功能障碍和神经退行性疾病具有关键影响。尽管如此,已经发现了表明脱髓鞘和少突胶质细胞(OL)状态参与DACD的直接证据,潜在机制仍然未知。
海马体是学习、记忆和认知能力的关键区域,分析海马体的分子特征反应是阐明DACD病理过程的适当途径。单核RNA测序(snRNA-seq)是一种新颖的实用方法,可对每个单核进行转录组学分析,识别细胞亚簇并定义其区别特征。在本研究中,进行了snRNA-seq以全面表征糖尿病小鼠模型海马组织的组成和转录变化。基于整合数据,研究鉴定了海马体中的不同细胞类型,并过滤了不同细胞类型中的差异表达基因(DEG)。在揭示了OLs的基因异质性和多样性后,研究者证实脱髓鞘可能是DACD进展的关键病理生理驱动因素,包括少突胶质细胞前体细胞(OPC)分化和OL细胞凋亡。有趣的是,DACD的髓鞘缺陷与OLs中的血清/糖皮质激素调节激酶1(SGK1)和N-myc下游调节基因1(NDRG1)信号通路有关。
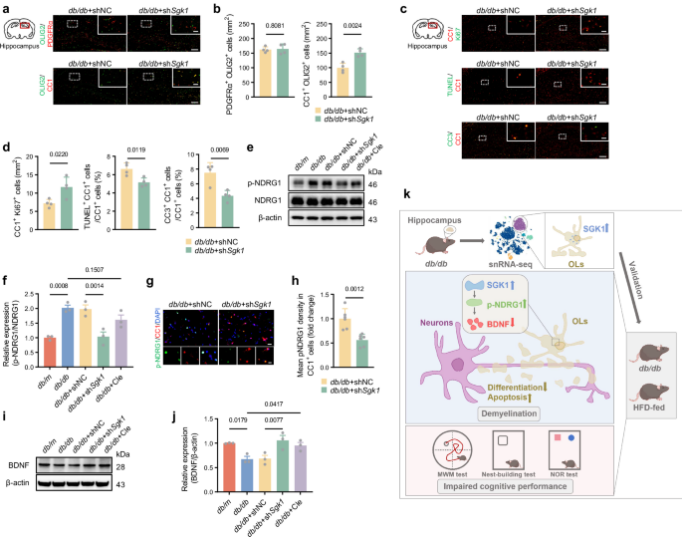
图1 OLs中的特异性SGK1敲低抑制NDRG1磷酸化,促进db/db小鼠的髓鞘形成(摘自Nature communications )
参考消息:
https://doi.org/10.1038/s41467-025-56854-2


