特别关注|瑞美替罗(Resmetirom)治疗代谢相关脂肪性肝炎的临床试验进展
时间:2025-02-21 12:08:40 热度:37.1℃ 作者:网络
随着肥胖、糖尿病和代谢综合征的全球化流行,非酒精性脂肪性肝病(NAFLD)及其严重类型非酒精性脂肪性肝炎(NASH)已成为目前世界慢性肝病最主要的病因,其患病率在全球范围内持续增加,严重危害公众健康。根据文献报道,全球25%的成人患有NAFLD,其中10%~30%为NASH,1%~2%的NAFLD患者伴有严重肝病(肝硬化、肝功能失代偿和肝细胞癌)。为解除西方语境中的污名化问题并明确诊断,2023年6月,美国肝病学会、欧洲肝病学会联合拉丁美洲肝病学会等组织成立了NAFLD更名专家顾问组,将NAFLD更名为代谢功能障碍相关脂肪性肝病(MASLD),NASH更名为代谢相关脂肪性肝炎(MASH)。MASLD的定义基本涵盖并扩大了原NAFLD定义的患者群体,诊断标准更重视代谢紊乱的存在,且可与酒精性肝病以及其他病因的慢性肝病共存,此新的定义更加综合、全面,积极推动了临床诊疗机制的更新,提高了公众对疾病的认识。
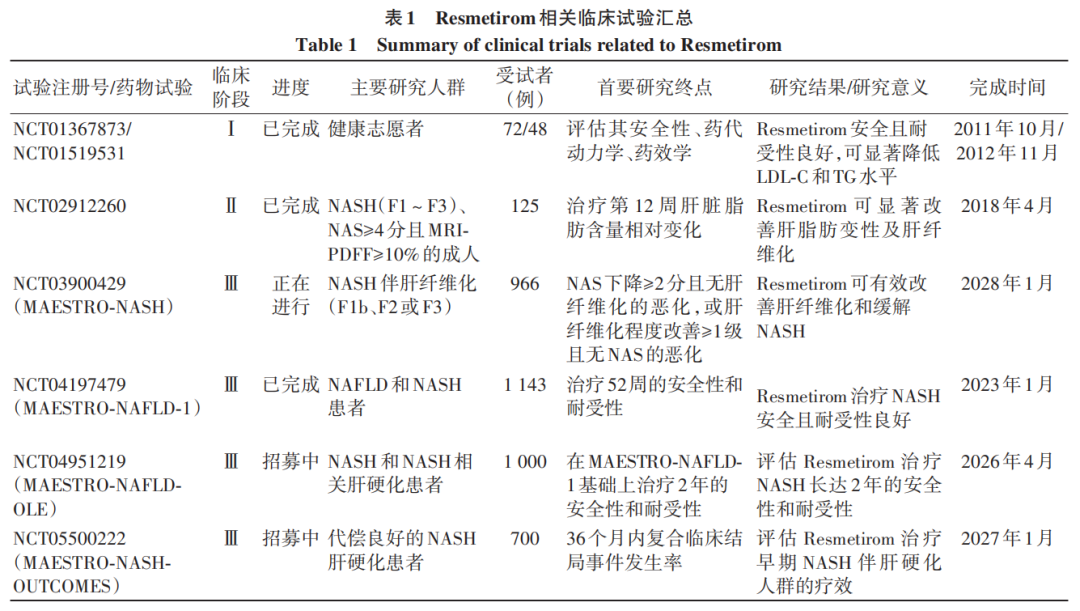
Resmetirom(瑞美替罗)是美国Madrigal公司研制的一款针对甲状腺激素受体-β(THR-β)选择性激动剂的原研新药,该药物可被肝细胞特异性摄取,通过THR-β调控多个肝脏代谢通路(图1),从而减少脂肪堆积、促进脂肪酸代谢、减少肝脏炎症和调节胆固醇代谢。2023年4月18日,Resmetirom获得美国食品药品监督管理局(FDA)认定;2023年9月,FDA正式受理其新药上市申请。2024年3月14日,Madrigal 公司宣布,FDA批准Rezdiffra(Resmetirom)联合饮食和运动,用于治疗患有中重度肝纤维化(F2~F3期)的非肝硬化MASH成人患者。Resmetirom的成功获批,是MASH治疗领域的重大突破,对长达40余年的MASH药物研发领域而言是一项重要的里程碑。本综述旨在总结Resmetirom相关临床试验研究概况(表1),为临床治疗提供理论参考。
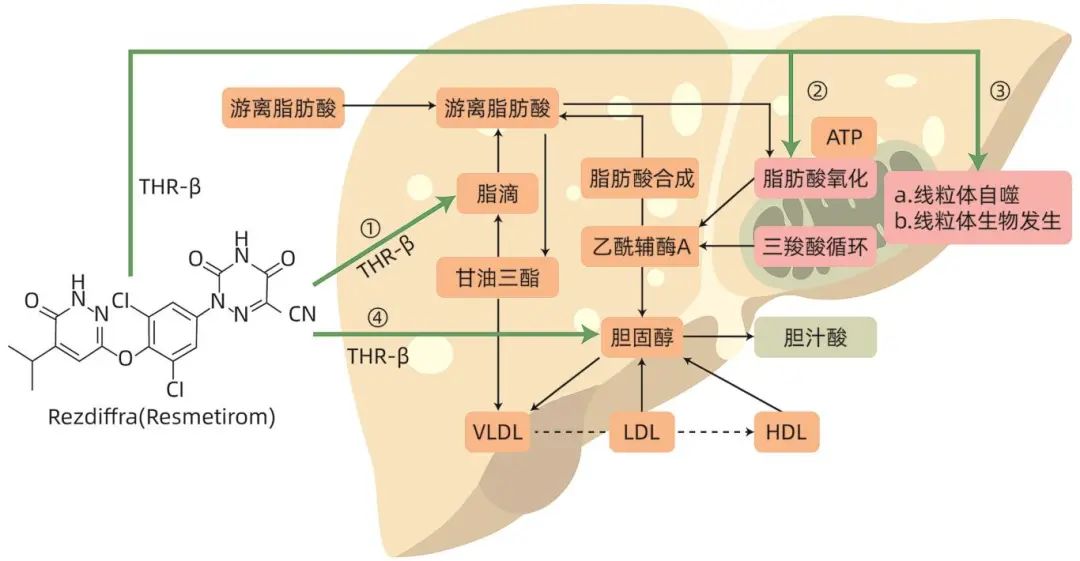
注:VLDL,极低密度脂蛋白;LDL,低密度脂蛋白;HDL,高密度脂蛋白。①通过调节甲状腺激素信号通路促进外源及内源脂肪降解为游离脂肪酸;②增加脂肪酸氧化;③促进线粒体生物发生和线粒体自噬,进而增加肝脏处理游离脂肪酸的能力;④通过减少VLDL的产生,增强肝内LDL受体的表达,调节胆固醇代谢,从而改善NASH。
图1 Resmetirom的作用机制
1Ⅰ期临床试验
Resmetirom(MGL-3196)首次公开亮相是在2012年的美国心脏协会科学年会,其Ⅰ期临床包括一项针对72例健康志愿者的单次剂量递增研究(NCT01367873)和一项在48例低密度脂蛋白胆固醇(LDL-C)轻度升高的健康志愿者中开展为期2周的多剂量研究(NCT01519531),主要评估MGL-3196的安全性、药代动力学和药效学。单次递增剂量试验中,治疗组按0.25、1.00、2.50、5.00、10.00、20.00、50.00、100.00和200.00 mg MGL-3196的剂量递增方案给药;多剂量试验中,治疗组随机给予5、20、50、80、100或200 mg MGL-3196。结果显示,MGL-3196在所有剂量下安全且耐受性良好,不良事件轻微,对肝酶、心电图、生命体征以及中枢甲状腺轴均没有影响;多剂量试验给药2周后,50~200 mg剂量之间,治疗组相较于安慰剂组均有显著的降脂效果,LDL-C、非高密度脂蛋白胆固醇、甘油三酯(TG)水平下降分别高达30%、28%和60%,且80 mg的Resmetirom对脂质参数的影响最大。
2 Ⅱ期临床试验
基于Ⅰ期临床数据,Madrigal公司启动了MGL-3196在NASH患者中的Ⅱ期临床研究(NCT02912260),这是一项在美国25个中心进行的为期36周随机、双盲、安慰剂对照试验。受试者按照2∶1随机分组,治疗组84例,安慰剂组41例,分别接受每日1次口服Resmetirom 80 mg或安慰剂。在第12周和第36周采用磁共振成像质子密度脂肪分数(MRI-PDFF)连续测量肝脏脂肪含量,在第36周进行了第二次肝活检,试验主要终点是第12周时治疗组与安慰剂组的肝脏脂肪含量相对变化。结果显示,第12周时治疗组肝脏脂肪含量下降32.9%,安慰剂组下降10.4%(P<0.000 1);第36周时,治疗组肝脏脂肪含量下降37.3%,安慰剂组下降8.9%(P<0.000 1)。与安慰剂组相比,治疗组可显著降低致动脉粥样硬化脂质(LDL-C、TG)和脂蛋白(载脂蛋白B、脂蛋白a、载脂蛋白CⅢ)、肝酶、肝纤维化等相关指标。两组不良事件发生率相似,严重不良事件很少(治疗组6%,安慰剂组5%),多为轻中度不良事件,以短暂性轻度腹泻(治疗组33%,安慰剂组7%)和恶心(治疗组14%,安慰剂组5%)较常见。
3 Ⅲ期临床试验
基于Ⅱ期阳性临床试验结果,为全方面验证Resmetirom治疗NASH的安全性和有效性,Madrigal公司共设计了4项Ⅲ期临床试验,其中,MAESTRO-NASH探索Resmetirom治疗NASH伴肝纤维化成人患者的疗效;MAESTRO-NAFLD-1和MAESTRO-NAFLD-OLE探索Resmetirom的长期安全性及耐受性;MAESTRO-NASH-OUTCOMES探索Resmetirom对早期NASH肝硬化患者的治疗作用。以下将详细介绍这4项Ⅲ期临床研究。
3.1 MAESTRO-NASH(NCT03900429)
NCT03900429是FDA批准上市的核心Ⅲ期试验,旨在评估口服Resmetirom治疗成人NASH伴肝纤维化的疗效,详细研究方案见图2。前期结果显示,在第52周时,低剂量组(80 mg)和高剂量组(100 mg)有25.9%与29.9%的患者实现NASH缓解[NAFLD活动度评分(NAS)降低≥2分]且肝纤维化未恶化,而安慰剂组为9.7%(P值均<0.001);低剂量组和高剂量组患者有24.2%与25.9%实现了肝纤维化改善至少一个阶段且NAS没有恶化,而安慰剂组为14.2%(P值均<0.001)。此外,次要终点LDL-C下降幅度方面,与基线相比,第24周低剂量组和高剂量组LDL-C水平分别降低了13.6%和16.3%,安慰剂组则增加了0.1%(P值均<0.001)。该项研究还达到了多个次要终点,Resmetirom显著降低致动脉粥样硬化脂质和脂蛋白、肝酶、肝纤维化生物标志物和影像学检查指标。安全性方面与前期研究结果类似,不良事件以腹泻和恶心更常见,各研究组的严重不良事件发生率相似:低剂量组为10.9%,高剂量组为12.7%,安慰剂组为11.5%。
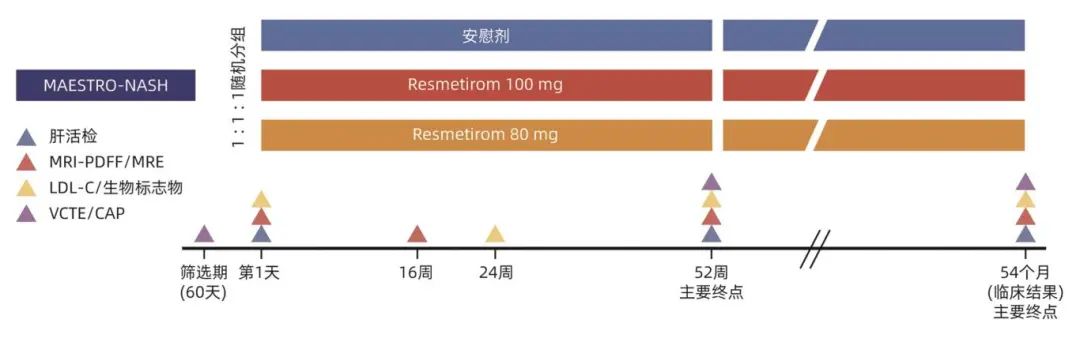
注:MRE,磁共振弹性成像;VCTE,振动控制瞬态弹性成像;CAP,受控衰减参数。
图2 MAESTRO-NASH研究设计
所有受试者在最初的52周后继续接受长达54个月的治疗,以累积和测量肝脏临床结果事件,包括活检进展为肝硬化、肝移植、肝脏失代偿事件和全因死亡率以及终末期肝病模型评分从<12分增至≥15分,该临床试验54个月的长期结果数据暂未发布。
3.2 MAESTRO-NAFLD-1(NCT04197479)
NCT04197479是一项为期52周的非侵入性Ⅲ期试验,旨在评估Resmetirom在高危NAFLD和NASH人群中的安全性和耐受性,具体研究方案详见图3,结果显示,治疗组和安慰剂组的不良事件发生率分别为86.1%~88.4%和81.8%(P>0.05),多数不良事件为轻中度,常见不良事件有腹泻、恶心、皮肤瘙痒、腹痛、呕吐、头晕等,以腹泻和恶心最为常见,治疗组腹泻发生率为23.5%~31.2%,安慰剂组为13.8%;治疗组恶心发生率为11.9%~18.2%,安慰剂组为7.9%。
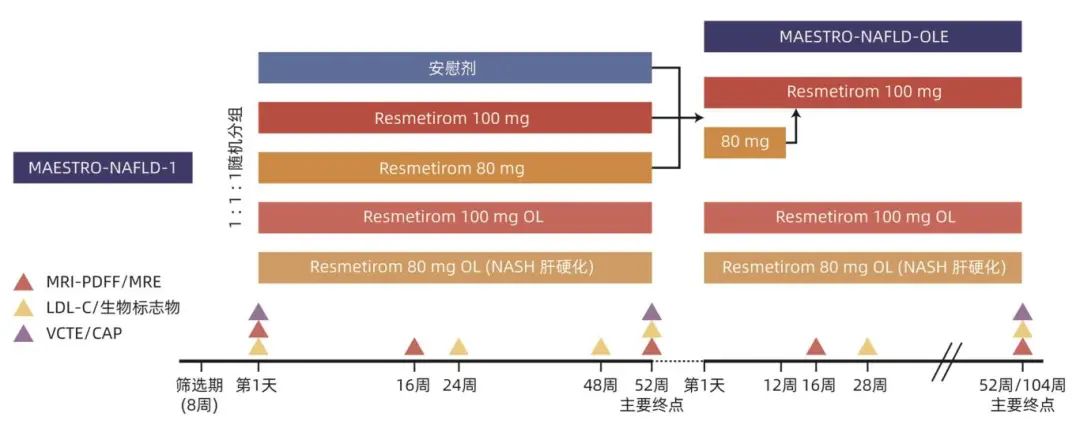
图3 MAESTRO-NAFLD-1/MAESTRO-NAFLD-OLE研究设计
3.3 MAESTRO-NAFLD-OLE(NCT04951219)
NCT04951219是在MAESTRO-NAFLD-1的基础上继续开展的多中心Ⅲ期临床试验,即MAESTRO-NAFLD-1的开放标签(open label, OL)扩展研究(图3),旨在进一步评估Resmetirom的长期安全性和耐受性,为监管申报提供长达2年的安全数据,预计于2026年4月完成。
3.4 MAESTRO-NASH-OUTCOMES(NCT05500222)
NCT05500222是一项为期36个月针对早期NASH肝硬化患者的随机、双盲、安慰剂对照的跨国、多中心临床研究,旨在评估Resmetirom对代偿良好(Child-Pugh A)的NASH肝硬化患者临床结局的影响,详细研究方案见图4。这项持续2~3年的事件驱动试验需监测的复合临床结局包括全因死亡率、肝移植和重大肝脏事件,如潜在的肝失代偿事件(腹水、肝性脑病或胃食管静脉曲张出血)、肝细胞癌以及终末期肝病模型评分从<12分增加至≥15分。积极的研究结果将支持Resmetirom用于治疗代偿良好的NASH伴肝硬化适应证的批准,预计于2027年1月完成。
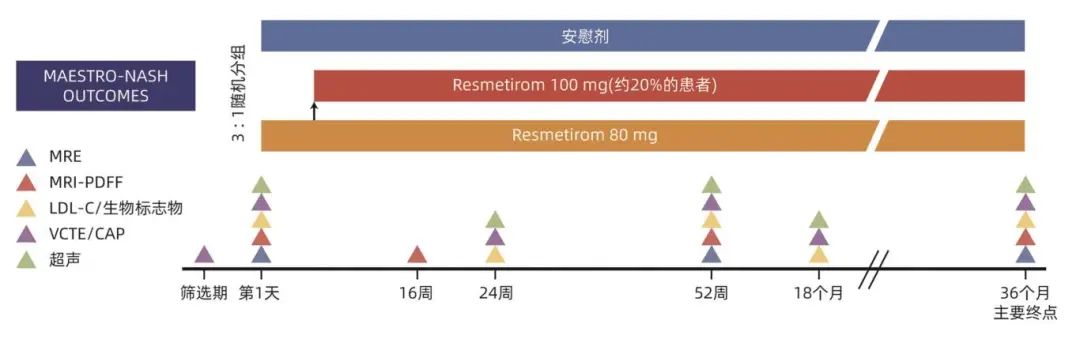
图4 MAESTRO-NASH-OUTCOMES研究设计
4 小结与展望
MASH是一种累及全身各系统器官的慢性进展性肝病,患者基数大,药物市场空间广阔,除发病机制复杂、缺乏有效的评估手段等问题外,FDA对MASH治疗的临床终点认定非常严格:(1)需要肝穿刺的病理学评价,影像学和血清学评价均不能作为上市审批的主要终点;(2)考虑只有肝纤维化分期与MASH的远期预后相关,若要取得病理学验证的成功,需要达到NAS改善和肝纤维化无恶化的双重标准,即NAS改善且肝纤维化无进展或肝纤维化改善且NAS无恶化。自1980年至今,所有针对MASH的药物研发几乎都以失败告终。在Resmetirom获批前,MASH治疗领域备受关注的是法尼醇X受体激动剂奥贝胆酸(OCA)。OCA是全球第一个进入Ⅲ期临床(NCT02548351)的NASH治疗药物,与安慰剂相比,OCA(25 mg/d或10 mg/d)组中分别有23%和18%的患者达到肝纤维化改善终点且NASH无恶化,而安慰剂组只有12%(P值均<0.05),但OCA在NASH消退且肝纤维化无恶化方面并未显著优于安慰剂。此外,OCA的常见副作用包括瘙痒和LDL-C水平升高,尤其是后者,心血管疾病风险可能随之增加,严重影响MASLD的临床结局,暴露出安全隐患,加之组织学终点数据获益的不确定性,影响其获批用于MASH,已被FDA拒绝批准。
Resmetirom是继OCA失败后试验进展最快的创新药,由于在NAS和肝纤维化改善方面均有良好表现,成为首个获得FDA批准用于治疗MASH的药物,该药于2024年4月在美国上市供应,且确定了治疗前不再需要进行肝穿刺活检,极大地方便了患者的使用。然而,新的MASH治疗药物也面临一系列问题:(1)由于MASH常无症状,导致部分患者未能及时得到治疗。(2)Resmetirom属于新上市药物,最新的定价为47 400美元/年,价格昂贵,加之需要长期治疗,用药患者需要承担很大的经济压力。(3)除去安慰剂效应,Resmetirom高剂量100 mg治疗MASH改善率仅为20.2%,肝纤维化改善率为11.7%,有效率偏低,需要进一步提升。MASH其他新靶点药物均处于Ⅱ期临床试验阶段,部分药物呈现非常高的有效率,如成纤维细胞生长因子21类似物Efruxifermin治疗24周肝纤维化改善且NASH无恶化的比例为21%,NASH症状缓解且肝纤维化没有恶化的比例为61%;Pegozafermin治疗24周肝纤维化改善且NASH无恶化的比例为19%,NASH症状缓解且肝纤维化无恶化的比例为21%。此外,胰高血糖素样肽-1受体激动剂索马鲁肽(0.4 mg)治疗72周NASH消退且肝纤维化未恶化的比例为42%,虽然对肝纤维化无效,考虑MASH常合并2型糖尿病,故也是值得关注的药物。期待上述药物的Ⅲ期临床试验获得良好的结果。(4)Resmetirom应答不佳的患者其后续治疗如何开展?是否联合胰高血糖素样肽-1受体激动剂或胰岛素增敏剂?(5)52周的短期临床试验结果提示有效,但其长期疗效如何?如何监测治疗反应?何时可以停药?停药后是否会反弹?潜在的甲状腺、性腺及骨骼等器官代谢副作用的概率有多大?以上问题均有待于Ⅲ期54个月的临床试验结果发布。综上,Resmetirom的成功获批固然可喜,但其在应用于MASH治疗的道路上仍将面临不少挑战。
全文下载
https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH250122



