EML4-ALK V3型和TP53共突变肺癌患者对ALK-TKI耐药,初诊14个月后小肠转移去世!
时间:2024-11-23 16:00:34 热度:37.1℃ 作者:网络
尽管间变性淋巴瘤激酶酪氨酸激酶抑制剂(ALK-TKI)提高了ALK融合肺癌患者的生存率,但其疗效在不同亚型之间差异很大。本文报告了一例肺腺癌患者在对ALK-TKI有明显反应后发生小肠转移的病例,该患者同时存在EML4-ALK V3融合和TP53突变。在接受恩沙替尼初始治疗后,患者出现颅内疾病进展。随后进行放疗(RT)。尽管颅内疾病对放疗反应良好,但原发肿瘤增大。因此,患者接受口服恩沙替尼同时联合化疗,原发肿瘤和颅内转移均获得部分缓解。然而,经过三个周期的治疗后,患者因急性肾损伤停止化疗。随后的胸部放疗使原发肿瘤获得部分缓解;然而,检测到新的脑和骨转移,改用洛拉替尼。患者在初次诊断后 14 个月出现肠梗阻症状。手术发现患者为空肠上段存在低分化转移性肺腺癌,基因检测证实携带EML4-ALK V3和TP53共突变,且PD-L1高表达。尽管患者接受了帕博利珠单抗治疗,但病情仍持续恶化,最终去世。总之,本文报道了一例罕见的肺腺癌小肠转移病例,该患者携带EML4-ALK V3/TP53共突变,不同病变对ALK-TKI的反应不同。本文研究结果显示ALK融合对ALK-TKI的反应存在异质性,因此需要密切监测基因亚型和相关突变,以制定个性化治疗策略。还应保持对潜在肠转移的高度警惕,监测肠道症状和腹部转移对于治疗晚期肺腺癌至关重要。
背 景
肺癌是癌症相关死亡的主要原因。其中主要包括非小细胞肺癌(NSCLC),占所有肺癌病例的 85%。NSCLC的主要组织学亚型是鳞状细胞癌和腺癌。大多数NSCLC患者在确诊时已是晚期,并有远处转移。肺癌患者经常转移到肝脏、骨和脑。胃肠道转移的发生率相对较少,约为 0.3%–1.7%,下消化道转移则更为罕见。值得注意的是,尸检调查显示NSCLC患者小肠转移的发生率为 4.6%。尸检病例中肠道转移率较高可能由多种因素造成。首先,肿瘤转移到肠道往往没有明显的症状,只有出现肠梗阻、穿孔等严重并发症时,才会引起医生的关注。其次,随着科学技术和药物的进步,患者生存期延长,远处器官转移风险也随之增加。有报道称,肺癌肠转移患者的预后不佳。
基因检测和靶向治疗已显著改善携带驱动基因突变的肺癌患者的生存结局。约 3%–7% 的肺腺癌病例中发现有间变性淋巴瘤激酶(ALK)驱动基因。全球已有多种间变性淋巴瘤激酶酪氨酸激酶抑制剂(ALK-TKI)获批用于治疗此类肺癌。第一代ALK-TKI克唑替尼取得突破性进展,总生存期显著延长至 4 年以上。第二代ALK-TKI包括塞瑞替尼、阿来替尼、布格替尼。其中,阿来替尼和布格替尼疗效优于克唑替尼,中位无进展生存期(PFS)>2 年。此外,洛拉替尼作为一种新型第三代ALK-TKI,对某些ALK耐药突变表现出更广泛的活性和有效性。然而,由于洛拉替尼的特定不良事件可能会影响患者的生活质量,因此其是否可以作为一线治疗药物存在争议。恩沙替尼是一种新型、强效的第二代ALK-TKI,旨在克服克唑替尼耐药。全球随机eXalt3试验证明,对于未经治疗的晚期ALK阳性NSCLC患者,恩沙替尼的全身(PFS 31.3 个月 vs. 12.7 个月)和颅内(ORR:63.6% vs. 21.1%)疗效优于克唑替尼。基于这些数据,恩沙替尼已于 2022 年在中国获批作为ALK阳性NSCLC的一线治疗药物。
然而,ALK-TKI的疗效在ALK阳性NSCLC的不同亚型中可能存在差异。V3变异患者的反应比V1变异患者差。存在ALK共突变的患者,尤其是ALK和TP53共突变的患者,也显示出较差的预后,同时存在V3和TP53突变的患者的预后更差。本文介绍了一例肺腺癌患者,该患者同时发生ALK V3和TP53突变。尽管最初接受恩沙替尼治疗,但患者仍出现颅内疾病进展。随后接受洛拉替尼治疗,但效果有限。患者在诊断 14 个月后出现小肠转移并最终去世。
病 例
患者女,45 岁,无吸烟史,于 2022 年 2 月 24 日因持续咳嗽和胸部不适就诊。PET-CT(图1A)显示右下叶肺门附近有一个高度代谢肿块,远端肺塌陷,胸腔积液,纵隔、右肺门和锁骨上区域有多个高代谢淋巴结。头颅磁共振成像(MRI)显示左额叶皮质内有散在异常信号及增强,提示潜在的转移性病变(图1A)。CT上没有内脏转移的证据。根据右锁骨上淋巴结活检(cT2N3M1,IV期)确定了肺腺癌的病理诊断。右锁骨上淋巴结HE染色呈阳性(×200,图2A)。免疫组织化学分析显示转录因子-1(TTF-1,图2B)和NapsinA(图2C,×100)染色呈阳性。2022 年 3 月 9 日进行的下一代测序(NGS)表明EML4 6号外显子与ALK 20号外显子融合(V3,突变丰度:淋巴结 1.4%,血浆 0.8%)。尽管信号较弱(在ALK端有一个read,在EML4端有两个read),但在血浆样本中检测到了ALK相互易位;而在组织样本中未检测到此类信号。在血浆中检测到TP53突变(0.7%),但在组织样本中未检测到。组织PD-L1检测显示肿瘤阳性评分(TPS)为 60%。
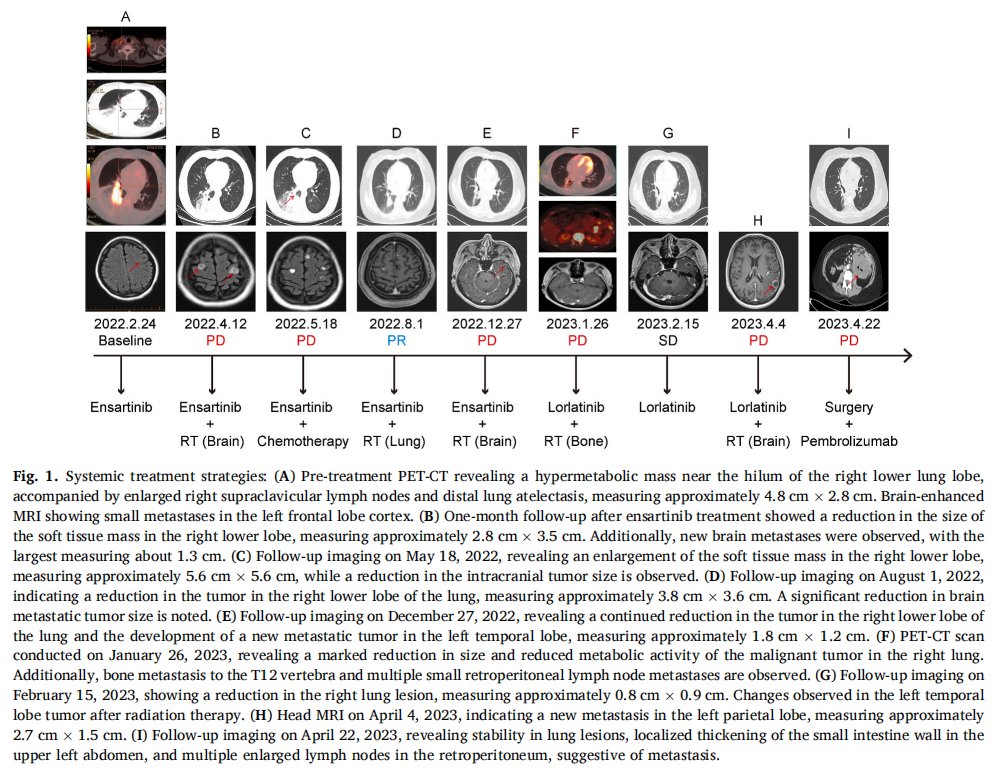
▲图1 系统性治疗策略
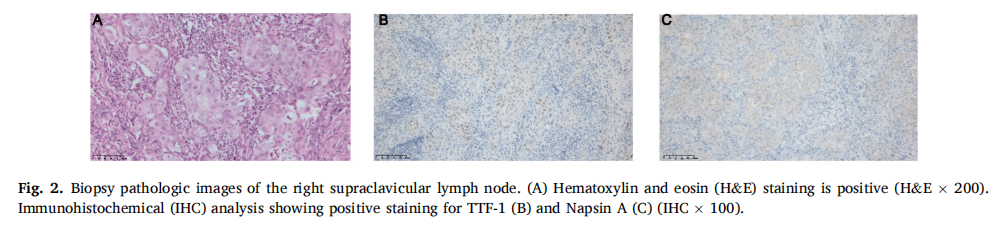
▲图2 右锁骨上淋巴结病理活检
2022 年 3 月 10 日,患者开始每日一次口服 225 mg恩沙替尼。一个月后,疗效评估显示颅内疾病进展,而原发肿瘤显示部分缓解(图1B)。NGS显示血浆EML4-ALK融合突变丰度为 0.1%;然而,在脑脊液中未检测到。此外,未发现TP53突变。因此,患者接受了放疗(RT),处方剂量为 45.5 Gy,分 10 次(45.5 Gy/10f)针对原发肿瘤,30 Gy/10f针对整个大脑。2022 年 5 月 18 日进行的影像学分析(图1C)表明原发肿瘤的大小增加,颅内肿瘤的大小减小。患者在口服恩沙替尼的同时,接受了三周期培美曲塞和卡铂化疗方案。2022 年 8 月 1 日,随访影像学显示原发性肺病灶和脑转移灶缩小,评价为部分缓解(图1D)。但三周期治疗后,患者出现急性肾损伤。停止化疗,患者继续口服恩沙替尼。2022 年 8 月 17 日,患者接受针对原发肿瘤和相应淋巴引流区的局部放疗,总剂量为 59.92 Gy/28f。四个月后,随访评估显示原发肿瘤缩小,但颅内疾病进展,左颞叶发现新的转移性病变(图1E)。随后,患者因新诊断的脑病变接受立体定向放疗,总剂量为 27Gy/3f。2023 年 1 月 26 日的PET-CT扫描(图1F)显示原发肿瘤和颅内肿瘤明显减少。然而,在没有腹部异常的情况下观察到骨转移至T12,以及多个小的腹膜后淋巴结转移。考虑到第十二胸椎的剧烈疼痛,患者接受了 30 Gy/10f 剂量的放疗以及口服洛拉替尼(100 mg,每日一次)。治疗耐受性良好,患者没有出现任何副作用。随后于 2023 年 2 月 15 日进行的随访检查(图1G)提示颅内病变情况稳定,原发肿瘤体积进一步缩小。2023 年 4 月 4 日,患者突然出现表达性失语。MRI显示左顶叶新发转移性病灶(图1H)。患者接受立体定向放疗,处方剂量 27 Gy/3f。失语症状逐渐缓解。2023 年 4 月 22 日,患者出现腹胀、排气、排便困难。CT扫描(图1I)显示左上腹部小肠壁增厚,腹膜后多个淋巴结肿大,怀疑为转移性肿瘤。腹腔镜手术显示肿瘤浸润肠系膜和空肠上段管腔,存在多个直径约 1-3 cm结节,位于距离Treitz韧带 30-100 cm处。术后病理检查提示为低分化转移性肺腺癌(图3A)。免疫组化分析显示甲状腺转录因子-1阳性表达(图3C),细胞角蛋白7、细胞角蛋白20、CDX-2表达阴性(图3B)。约 80% 的细胞P53染色阳性(图3D),70% 的细胞Ki-67染色阳性(图3E)。2023 年 5 月 17 日通过NGS进一步评估,证实了EML4-ALK V3(血浆 17.15%,组织 54.51%)和TP53(血浆 10.88%,组织 55.56%)共突变。患者PD-L1表达较高,TPS为 70%。尽管给予帕博利珠单抗(200 mg)治疗,患者病情仍恶化,出现明显腹胀、腹水、肺部感染、贫血、低白蛋白血症和凝血功能障碍。患者于 2023 年 6 月 14 日去世。
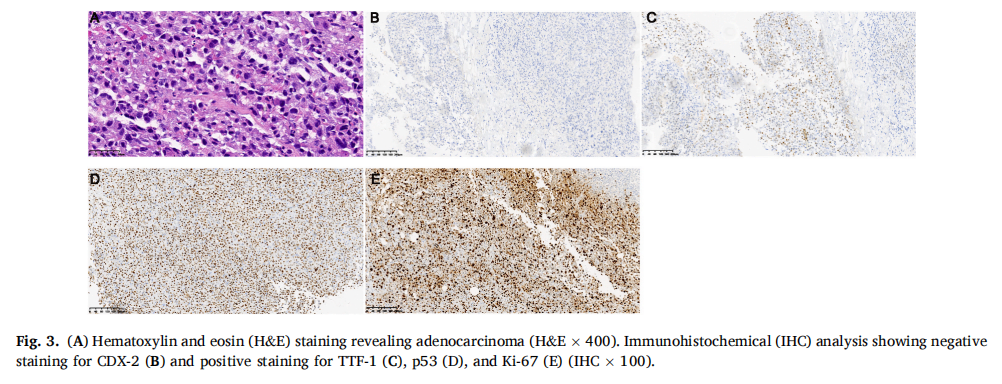
▲图3 HE染色和免疫组织化学结果
讨 论
据研究人员所知,这是首例在接受ALK-TKI治疗的患者中发现EML4-ALK V3和TP53共突变肺腺癌伴小肠转移的病例。考虑到这种情况的罕见性和对靶向治疗的反应有限,研究人员建议临床医生更多地关注TP53和EML4-ALK V3共突变的NSCLC患者。此外,临床应对原发性NSCLC转移到肠道的可能性保持警惕,早期有效治疗对于诊断至关重要。
肺癌转移到肠道的症状常表现为出血、梗阻或穿孔,偶尔会伴有疲劳、腹痛和体重减轻等非特异性症状。因此,这些病例经常被错误地归因于抗肿瘤治疗的不良反应或其它疾病,导致一些病例的肠道转移被延迟诊断甚至漏诊,直到尸检时才发现。另外,胃肠道转移通常发生在患者的治疗过程中,特别是在疾病晚期。这导致基线报告的病例数量有限,也导致了有关该主题的文献相对稀缺。一项对 2066 例患者的研究报告称,从诊断肺癌到发现胃肠道转移的平均时间为 13.5 个月(范围:3–49 个月)。与其他远处转移患者相比,胃肠道转移患者的预后较差,从发现胃肠道转移开始平均生存期为 100.6 天。该患者基线时无胃肠道转移症状。11 个月后发现多个腹膜后淋巴结转移,14 个月时发现肠梗阻。随后的手术病理证实转移至小肠,患者又存活了 49 天。因此,当肺癌患者出现胃肠道症状时,应在综合评估中认真考虑胃肠道转移的可能。对于腹膜转移,必须密切监测消化系统症状。
肺癌胃肠道转移瘤易被误诊为原发性胃肠道肿瘤、肠结核或憩室。早期往往没有症状,必须依靠CT和PET-CT等影像学检查,但这些检查的敏感性可能有限。内镜检查和组织病理学是金标准;然而,在黏膜完整的黏膜下层转移会导致活检结果不佳,尤其是在小肠深层。TTF1、CDX2、细胞角蛋白7和细胞角蛋白20的免疫组化检测有助于提高原发性和转移性小肠肿瘤的诊断准确性,从而为后续治疗奠定基础。本病例腹部CT显示左上腹小肠壁增厚,提示可能有转移性肿瘤。免疫组化结果支持肺腺癌转移的诊断。目前肺癌胃肠道转移尚无标准治疗方法,考虑到患者病情及多学科团队建议,研究人员选择了姑息手术。术后病理证实为低分化转移性肺腺癌,伴有EML4-ALK融合。虽然目前尚无关于肺癌胃肠道转移途径的具体报道,但血液和淋巴播散被认为是最可能的途径。值得注意的是,本文回顾的所有研究都是回顾性的,存在数据选择偏差。
已发现数种ALK融合伴侣,其中EML4-ALK融合最为常见,主要见于年轻非吸烟肺腺癌患者。根据EML4-ALK融合所涉及的外显子不同,该融合类型可进一步分为不同的亚型。其中,V1(涉及EML4 13 号外显子和ALK 20 号外显子)和V3a/3b(涉及EML4 6a/b 外显子和ALK的 20 号外显子)最为常见,分别占ALK阳性NSCLC的 43% 和 40%。V3疗效较差,69% 的患者在初次诊断时出现转移。在EML4-ALK阳性NSCLC患者中,约 20% 表现出TP53突变。值得注意的是,TP53突变以及EML4-ALK V3与转移性播散增加和预后不良相关。TP53突变同时发生是ALK阳性患者的一个不良预后因素。与TP53野生型患者相比,ALK/TP53共突变患者的中位PFS(3.9 个月vs 10.3 个月)和总生存期(15.0 个月vs 50.0 个月)显著减少。治疗期间TP53表达持续为阴性的NSCLC患者预后最好,而最初TP53表达为阳性的患者预后最差。据报道,对于同时存在ALK和TP53突变的NSCLC患者,洛拉替尼会导致较差的PFS。eXalt3试验中亚洲队列的亚组分析表明,基线脑转移患者接受恩沙替尼治疗后中位PFS为 11.8 个月,显著超过克唑替尼的 7.5 个月。根据本文患者的基因检测结果,恩沙替尼作为一线治疗。患者最初对恩沙替尼治疗有反应,肺部病变部分减少,但颅内疾病进展。脑脊液ALK融合阴性。脑转移瘤放疗后颅内病变改善。患者肺和脑病变表现出异质性。因此,虽然靶向药物对脑转移患者原发性肿瘤有效,但仍需密切监测颅内进展。脑脊液基因检测的敏感性不容忽视。随后,尽管换用第三代ALK-TKI洛拉替尼,脑转移瘤仍继续进展,进一步证实了肿瘤的异质性。诊断肠转移后,动态NGS显示持续的V3/TP53共突变和TP53丰度增加。推测虽然第三代TKI对ALK V3突变有效,但TP53突变成为优势亚克隆,导致疾病持续进展。对于该特定亚型,患者对恩沙替尼和化疗同时治疗有一定反应,但由于肾功能受损而不得不停止治疗。此外,在疾病相对稳定期,仅肺部有残留病变,给予局部放疗,导致胸腔内病变部分缓解,直至患者死亡。脑转移瘤对放疗也反应良好,凸显了综合治疗方法的优势。
虽然患者PD-L1高表达,但研究人员最初按照优先靶向治疗的原则,先进行了靶向治疗。由于病情进展,研究人员打算进行免疫治疗,但患者新冠病毒检测结果呈阳性,检测结果转阴后病情迅速恶化,虽然进行了免疫治疗,但效果不佳。因此优先进行一线靶向治疗,还是联合或不联合化疗进行一线免疫治疗,仍然是一个难题。
Zhang等人先前的研究表明,ALK非相互/相互易位患者占ALK重排NSCLC患者的 18.7%。与仅有3′- ALK融合的患者(6.1 个月 vs. 12.0 个月,p = 0.001)或仅有EML4-ALK融合的患者(6.1 个月 vs. 12.6 个月,p = 0.001)相比,这些患者接受一线克唑替尼治疗后的中位PFS明显较短。非相互/相互ALK易位的发生是克唑替尼治疗效果的独立预测因素(p = 0.0046)。此外,非相互/相互ALK易位患者的脑转移率更高。本病例的血浆样本中发现了ALK相互易位,尽管信号较弱。相反,在组织样本中未检测到易位。这种差异可能导致对ALK-TKI的反应不佳。然而,目前尚不清楚其他第二代ALK-TKI是否会产生类似的结果,值得进一步研究。
总之,本文报道了一名患有晚期肺腺癌的中年女性,该患者携带EML4-ALK V3和TP53共突变,在对ALK-TKI产生明显反应后出现小肠转移。肺癌对ALK-TKI的原发性耐药罕见且复杂,可能是由于肿瘤异质性、基因共突变、ALK相互易位和患者免疫特征所致。研究这些机制至关重要。临床医生应考虑肿瘤组织学和基因检测以制定个性化治疗方案。及时诊断肺癌肠转移对于个性化治疗至关重要。进一步完善ALK融合阳性患者的管理具有临床意义。
参考文献:
Lingling Zhu, Yingchun Zhao, Yongqian Zhang, Zhai Liu, Wenhua Ma, Ying Guo, Qian Wang, Yan Guo, Hengxu Lv, Min Zhao,Small intestinal metastasis in a lung adenocarcinoma patient with concurrent EML4-ALK V3 and TP53 mutations after distinct responses to tyrosine kinase inhibitors: A case report,https://doi.org/10.1016/j.heliyon.2024.e38839.



