张真发教授组稿|李跃:新辅助免疫联合化疗治疗肺上沟瘤的手术经验分享
时间:2024-11-09 17:03:13 热度:37.1℃ 作者:网络
编者按:新辅助免疫治疗在胸外科领域正受到广泛关注,尽管目前尚存在一些未解之谜,但它在临床上已得到了广泛的应用,并为众多患者带来了显著的益处。对于局部晚期肺癌患者,新辅助免疫治疗能够提高他们获得手术机会的可能性。在肺小结节的肺段切除手术中,天津医科大学肿瘤医院肺部肿瘤外科提出了“动脉先行——以动脉为核心的解剖性肺段切除”技术。随着时间的推移,他们越来越认识到这种技术对于肺段切除手术的重要性,它能够使手术过程更加简单和准确。此外,在肺小结节的定位方面,该中心已经完成了近千例磁导航定位切除手术,积累了丰富的经验,希望这些经验能够为大家提供有价值的参考。
本期「专家组稿」由天津医科大学肿瘤医院张真发教授担任执行主编,与天津医科大学肿瘤医院李跃教授共同分享《新辅助免疫联合化疗治疗肺上沟瘤的手术经验》,为医者和患者提供更多参考。
肺上沟瘤是指原发在肺尖部的支气管肺癌,是原发性肺癌中的特殊类型,占总体的5%,常常侵犯第1肋骨、椎体、锁骨下血管、臂丛神经、交感神经链和星状神经节等胸廓入口结构。由于肿瘤位于胸腔入口处,为数众多的重要血管、神经在狭窄的空间里纵横交错,解剖极其复杂(图1)。放射学家Pancost HK首次详细描述了这类特殊的肿瘤,故也称Pancoast瘤。
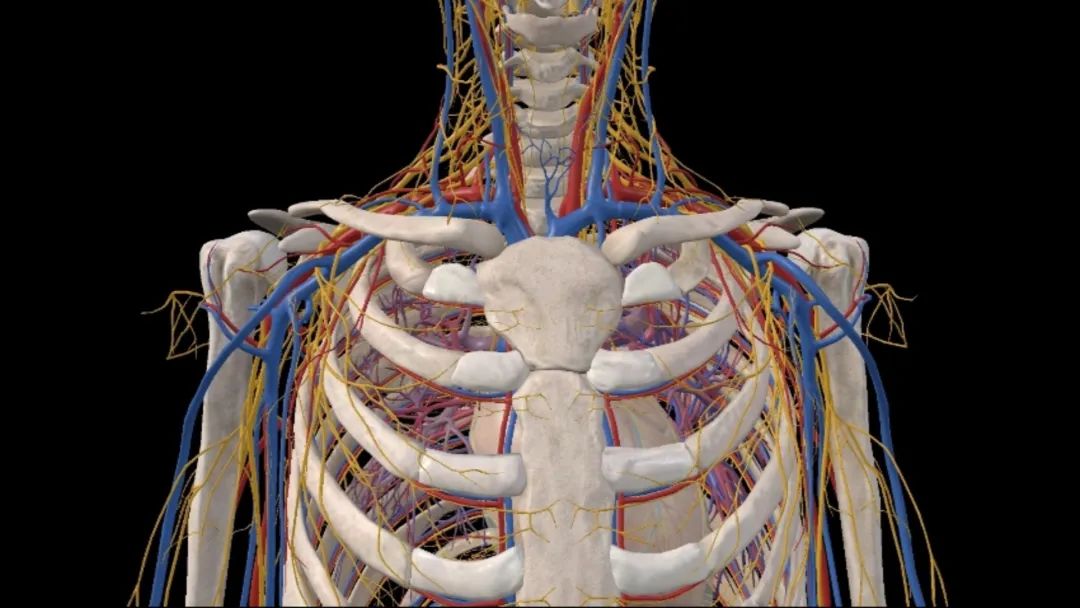
图1.颈胸部交界解剖示意图
在1950年以前,肺上沟瘤被认为是无法切除的。1954年Haas等首先报道采取姑息性外照射疗法治疗Pancoast瘤,结果4例患者疼痛得到了明显缓解。1956年,Chardark等率先报道了1例肺上沟瘤手术切除的病例,患者接受根治性切除结合术后放疗,生存5年,复查时未见肿瘤复发或转移。Shaw和Paulson对18例患者采取局部放疗30 Gy后再后路行根治性手术,较以往的治疗方式获得更高的年生存率和局部控制率。此后,这种治疗方案得到迅速推广和改进,并作为肺上沟瘤的标准治疗模式沿用数十年。在过去的几十年间,各种新技术不断被开发应用,为肺上沟瘤的切除提供了更加安全有效的方法,在处理那些侵犯锁骨下血管、臂丛神经、椎体等结构的肿瘤时,安全性得以提高。
01 手术策略及入路
肺上沟瘤患者在下列条件下均应考虑手术治疗:
适应症:无远处转移,非小细胞肺癌,能够达到根治性完全切除,脏器可耐受;
禁忌症:臂丛神经、椎间孔、椎体或椎板广泛受肿瘤侵犯,小细胞肺癌,纵隔淋巴结转移或远处转移,侵犯上腔静脉并有上腔静脉综合征,锁骨下动脉受侵。
常用的手术入路主要有高后外侧入路、前胸入路等。
高后外侧入路:1961年,Shaw和Paulson利用后胸切口进行肺上沟肿瘤切除,这是最早报道的肺上沟瘤手术方式,后被称为Shaw-Paulson术式(图2 A),是肺上沟瘤的经典术式。随后,Niwa和Masaoka对Shaw-Paulson术式的切口进行了钩形修改,方便对锁骨下血管、臂丛神经、淋巴结以及椎体进行操作。Shaw-Paulson术式以及钩形修改术式,至今仍被频繁地用于切除位于胸腔入口后方的肺上沟肿瘤。
前胸入路:1979年,Masaoka等提出了一种前路治疗侵犯胸廓入口并累及血管的肺上沟肿瘤的方法(图2 B)。Dartevelle等1993年提出了经颈胸前路切口(图2 C),切口沿胸锁乳突肌的前缘延伸到锁骨的外侧,需切除锁骨的内侧部分。Grunenwald和Spaggiari对前入路改良为种经胸骨柄L形入路(图2 D)。此入路将经锁骨切口发展为经柄切口,可以很好地进入锁骨下区域,安全地切除神经、血管出口结构,从而避免了锁骨切除造成的外观和功能破坏,降低了术后发病率。该类切口的缺点在于对于后胸壁、肺门血管显露差,通常还需要再行后外侧切口来协助完成肺叶切除术。
半蛤壳切口和活板门切口最初常用于纵隔肿瘤或锁骨下血管创伤的治疗,Rusca和Bains利用这两种前入路术式治疗肺上沟瘤,半蛤壳状切口加胸骨上延伸即为活板门切口。(图2 E)
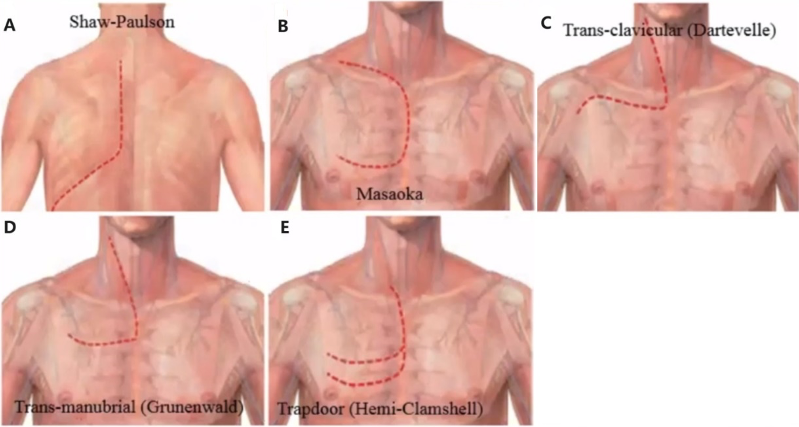
图2.常见肺上沟瘤手术入路
笔者也将上述几种手术入路的优缺点总结于表1。
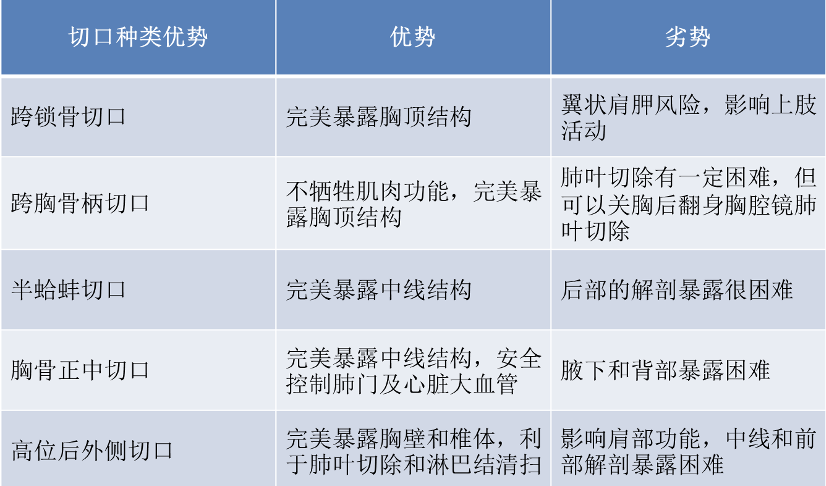
表1.肺上沟瘤手术切口优略势比较
02 肺上沟瘤治疗模式的演变
1953年,Chardack和MacCallum发表了第1例完整切除肺上沟瘤并进行术后辅助放射治疗的病例报告,且患者在术后获得了超过5年的生存时间。Shaw等随后提出了双联疗法(放疗+手术,通过后外侧入路)的治疗模式,并从此成为了标准的治疗方式。三联疗法(同步放化疗+手术)能够取得更高的手术切除率和病理缓解率。两项著名的肺上沟瘤临床试验SWOG9416和JC09806证实,三联疗法(术前同步放化疗+手术)的完全切除率(分别达到94%和89%)和放化疗的病理缓解率都有所改善,5年生存率也有所提高(分别为44%和56%)。随着微创手术的逐渐成熟和免疫时代的到来,给肺上沟瘤有了更多的选择,更好的治疗结果以及更小的创伤。
03 治疗模式的经验分享
我中心近年来结合以往的经验及免疫治疗,提出了新的治疗经验,即以新辅助免疫联合化疗为手段,前入路切口联合胸腔镜为主要术式的治疗理念。基于一系列经典新辅助免疫联合化疗的临床试验数据(包括CheckMate 816研究、CheckMate 77T、KEYNOTE-671、RATIONALE-315、Neotorch研究等)的公布,奠定了围术期免疫联合化疗治疗局部晚期非小细胞肺癌的地位,尤其是对于肺上沟瘤这样一种特殊的肺癌,局部解剖结构复杂,手术难度高,如能使肿瘤大幅度降期,必将提高患者生存,降低手术难度,减轻患者的痛苦。治疗流程上,全面评估患者的身体情况和影像学资料,组织多学科会诊MDT,如有手术机会能够实施R0切除,可考虑进行转化治疗后进行手术切除。明确的病理诊断是治疗的基础,对于免疫优势人群,如鳞状细胞癌、驱动基因阴性的腺癌患者,首选新辅助免疫联合化疗作为术前治疗的方案。接受3-4周期后,进行肿瘤术前评估,符合手术指标,行择期手术治疗。术后再进行术后免疫辅助治疗。
04 手术中的经验分享及注意事项
我中心目前主要采用Grunenwald入路联合胸腔镜进行手术治疗。
步骤一:平卧位Grunenwald入路手术。首先Grunenwald入路既可以很好地进入锁骨下区域(图3),最重要的是能很好地显露斜角肌间隙(图4),安全切除神经、血管出口结构,此为手术的关键和难点,即使需要进行锁骨下动脉的操作,如血管置换,可以在控制血管的远心近心端后从容操作,又避免了Dartevelle切口锁骨切除造成的外观和功能的破坏,降低了上肢活动障碍的发生率。
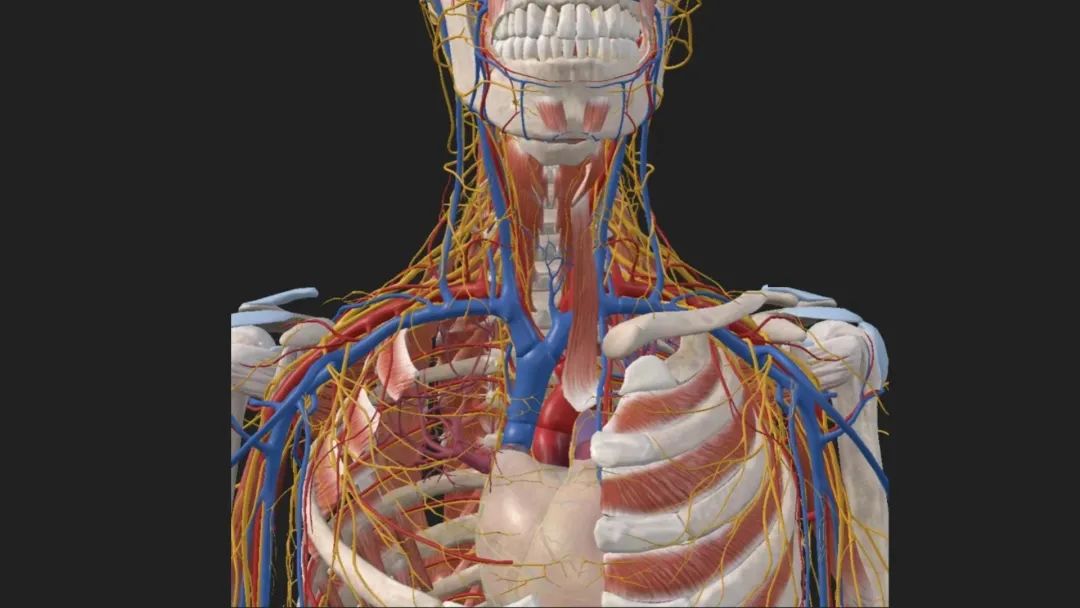
图3.Grunenwald 入路后对锁骨下区域的暴露示意图
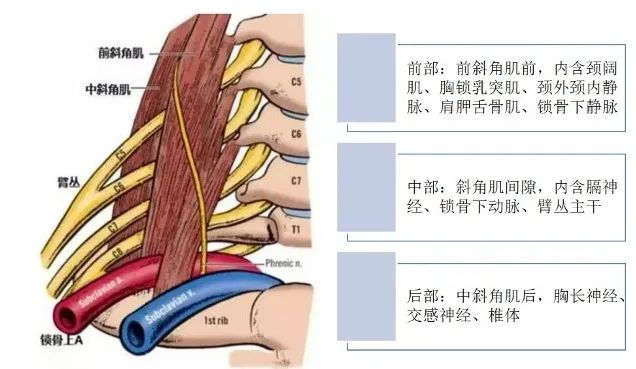
图4.斜角肌间隙局部解剖
解剖及手术要点:
1.由颈内静脉解剖开始,向下暴露到静脉角,解剖颈总动脉向近心端暴露与同侧锁骨下动脉的交汇处;
2.同时保护性解剖膈神经和迷走神经总干,有利于解剖标识的确认,也避免膈神经、喉返神经等重要神经损伤;
3.尽早切断第一肋及第二肋胸骨侧连接处,利于提升肌骨瓣,暴露前斜角肌间隙,离断前斜角肌,暴露臂丛及锁骨下动脉;
4.充分地解剖血管利于牵拉和暴露尽量;
5.由于椎动脉对大脑供血的重要作用,对其应尽量予以特殊保护;
6.由于肿瘤位于肺上沟这一特殊的颈胸交界区,患侧下颈部淋巴结及脂肪垫应该常规清扫;
7.如患侧锁骨下静脉、颈内静脉或无名静脉受侵,可毫不犹豫地结扎切断,如左右无名静脉汇入上腔静脉交汇的“三岔路口”受侵犯,可进行一侧无名静脉与右心耳做人工血管搭桥后再切除受侵无名静脉及上腔静脉。在Grunenwald入路下安全切除肿瘤侵犯的胸壁、肋骨甚至血管,并能在此切口下完成对上纵隔(1-4区)、肺门淋巴结的彻底清扫,完成对上叶动脉、静脉甚至气管的离断,标本的移除(图5)。
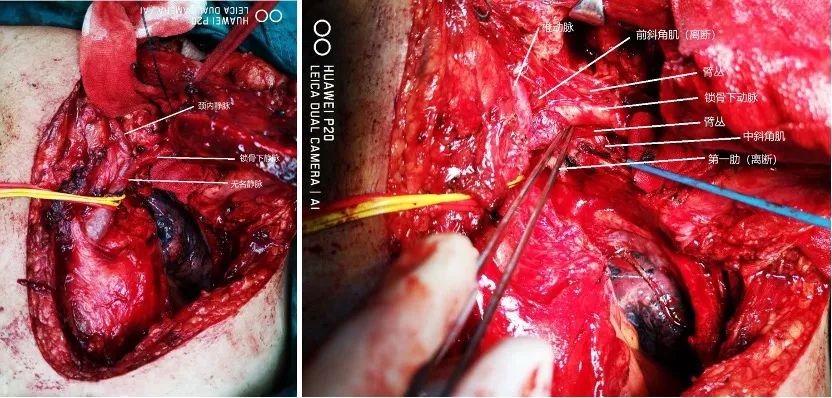
图5.Grunenwald 入路下对锁骨下区域重要解剖结构的良好暴露
联合胸腔镜手术,由于缺点在于对于后胸壁、肺门血管显露差,通常还需要再行后外侧切口来协助完成肺叶切除术。但随着胸腔镜微创时代的到来,胸腔镜可弥补这一不足,进一步减小患者的损伤。胸腔镜可以在Grunenwald入路操作完成后进行,我中心一般采用纯单孔胸腔镜或单操作孔胸腔镜方式进行,对后纵隔、下纵隔淋巴结(7、8、9区)进行彻底清扫。既保证了手术的彻底性,又避免了二次后外侧切口的巨大创伤。(图6)
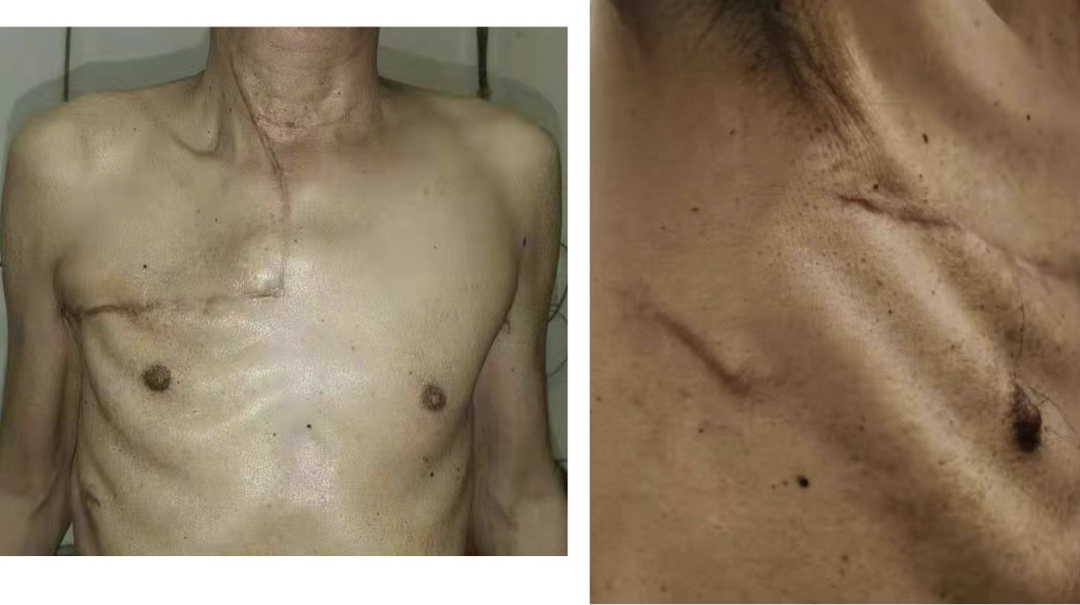
图6.Grunenwald 入路联合单操作孔胸腔镜手术切口
对于新辅助免疫联合化疗这一模式治疗肺上沟瘤,我中心目前已完成4例患者(图7),总结手术难度没有因为化疗及免疫治疗增加,仅仅与肿瘤基线期情况及手术难度相关;很多基线期显示肿瘤侵犯锁骨下动脉等重要血管的患者,由于肿瘤的退缩,手术中探查及血管周边组织术中冰冻均为阴性,避免了对血管的骚扰及处理,降低了手术难度,减少了长时间手术患者心脑血管意外的发生,目前该10例患者均健在,可能获得长期生存。
随着免疫时代的到来,尤其是PD-1/PD-L1药物临床试验及数据的报道,相较于传统的三联疗法的同步放化疗模式,新辅助免疫联合化疗对患者的安全性、有效性、降期率较高,不良反应较为可控,术中组织黏连可接受,尤其是对需要解剖的锁骨下动脉,锁骨下静脉,上腔静脉等重要血管黏连较轻,即使需要进行锁骨下动脉人工血管置换,由于未经过放疗影响,组织弹性较好,吻合血管较为容易。新辅助免疫联合化疗后,Grunenwald入路联合胸腔镜手术这一治疗模式给了肺上沟瘤围术期患者一个较为理想的治疗手段。
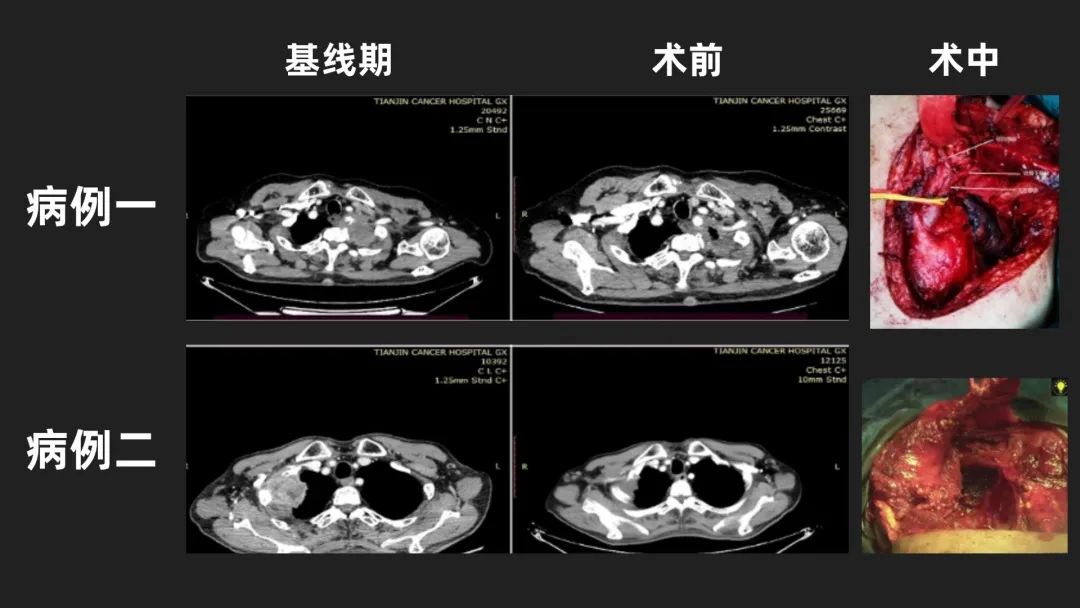
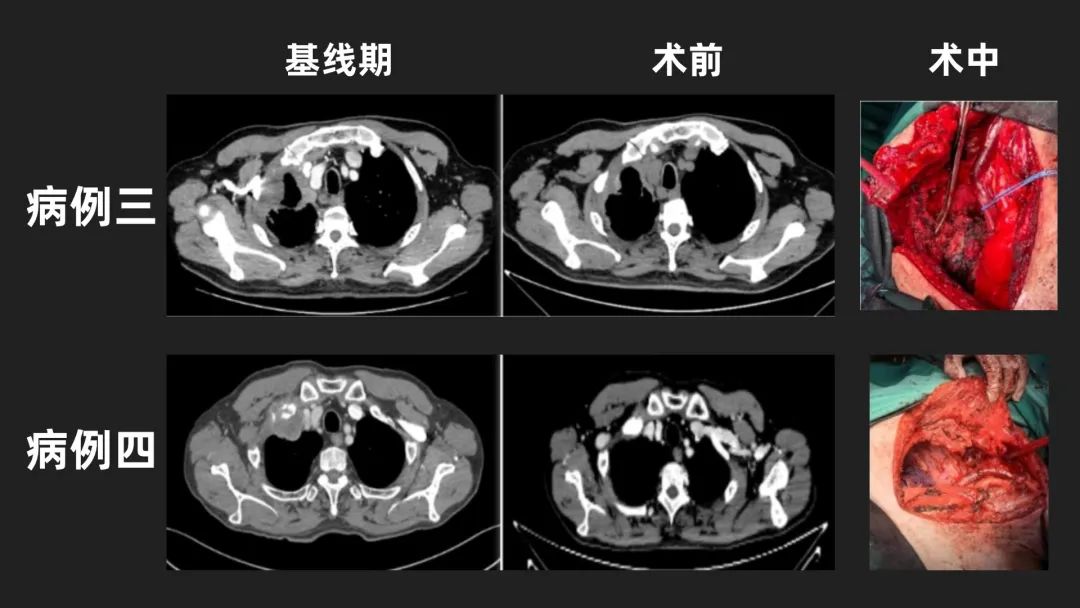
图7 我中心肺上沟瘤患者影像资料及术中照片
主编评语
肺上沟瘤的手术治疗比较复杂,以往的治疗往往采取新辅助化(放)疗的形式,手术仍然比较困难。随着免疫治疗时代的到来,开始采用新辅助免疫加化疗的方法,对一些患者取得比较好的疗效,而且手术难度可以下降。对于一些需要锁骨下动脉置换的患者,经新辅助化疗加免疫后,可能免除锁骨下动脉置换,降低了手术难度和风险。我们的经验,不推荐术前的新辅助放疗,纤维化黏连严重,手术难度大。


