Adv Sci:空军军医大学孙冬冬团队研究确定了糖尿病中心脏血管内皮损伤的新机制
时间:2024-11-06 06:02:56 热度:37.1℃ 作者:网络
心血管疾病仍然是糖尿病患者高死亡率的主要原因。内皮损伤是糖尿病血管功能障碍的主要诱因。然而,糖尿病中内皮细胞损伤及其异质性的确切机制仍然难以捉摸。
2024年10月30日,空军军医大学孙冬冬通讯在Advanced Science 在线发表题为“Single-Cell RNA Sequencing Uncovers Pathological Processes and Crucial Targets for Vascular Endothelial Injury in Diabetic Hearts”的研究论文。该研究中,对处于不同病理阶段的瘦素受体敲除(db/db)糖尿病小鼠的心脏组织进行了单细胞测序。通过细胞簇识别、差异基因分析、细胞间通讯分析、伪时间分析和转录因子分析,确定了糖尿病中心脏血管内皮损伤的新机制。
具体而言,在db/db小鼠中呈现了心脏血管内皮细胞的单细胞转录图。发现各种细胞簇在糖尿病引起的损伤下发挥着重要作用,突出了参与调节它们的关键转录因子。此外,发现必需的转录因子Ets1可保护db/db小鼠免受血管内皮损伤。综上所述,本研究对糖尿病心脏血管内皮损伤的发展过程及其细胞的异质性提供了全面的认识,为糖尿病心血管内皮损伤的潜在治疗和评估提供了宝贵的见解。

根据国际糖尿病联盟(IDF)最近的流行病学调查,估计2021年全球约有5.36亿成年人患糖尿病,到2045年,这一数字预计将超过7亿。糖尿病的惊人患病率不仅带来了沉重的医疗负担,而且是全球主要的死亡原因,强调了更好地管理糖尿病及其相关并发症的迫切需要。
众所周知,1型和2型糖尿病都会对多个器官的血管产生不利影响。心血管异常仍然是糖尿病患者死亡的主要原因。相反,糖尿病患病率的急剧上升也是导致心血管疾病高发的重要因素。心脏组织含有丰富的血管网络,血管功能障碍往往是糖尿病患者的早期症状。早期血管异常逐渐发展为不可逆的结构性疾病。这一进展主要涉及血管稀疏和小动脉的不良重塑,导致心脏舒张和收缩功能受损。
内皮细胞(EC)是心脏中的主要非肌细胞。EC通过调节血管壁的厚度和直径来应对血流施加的剪切应力,同时控制免疫细胞和分子进入内皮下组织。为了满足血管系统的不同需求,EC 通常由具有不同功能的异质簇组成。
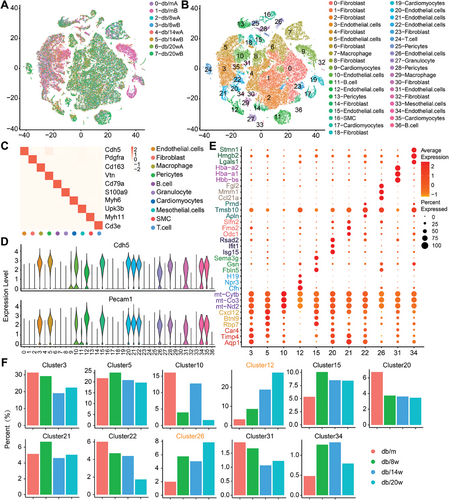
心脏血管内皮细胞异质性的表征(图源自Advanced Science )
内皮损伤是糖尿病血管功能障碍的主要原因,其特征是血管收缩因子分泌增加、细胞活力降低、内皮通透性升高、一氧化氮(NO)生成受损和血栓形成。在早期暴露于高血糖水平的情况下,即使在严格控制血糖的条件下,EC也会遭受持续损伤。然而,糖尿病损伤中EC的异质性及其潜在机制仍不清楚,阻碍了糖尿病心血管损伤的有效预防和治疗。
单细胞测序能够在单个细胞水平上识别多种细胞类型及其基因表达,为生物发育和疾病进展提供独特的见解。该技术揭示了特定微环境中的细胞序列差异,准确表示了给定样本中的细胞异质性。在作者的研究中,作者使用瘦素受体敲除(db/db)小鼠作为糖尿病模型,并在不同病理阶段对这些小鼠的心脏进行测序。通过细胞簇识别、差异基因分析、细胞间通讯分析、伪时间分析和转录因子分析,作者揭示了糖尿病心脏血管内皮损伤的基本机制。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202405543


