重庆医科大郭风劲教授团队《自然·通讯》:揭示天然小分子药物10-HDA在骨关节炎进展中的保护作用和机制
时间:2024-09-06 12:00:50 热度:37.1℃ 作者:网络
骨关节炎(Osteoarthritis, OA)是一类以软骨纤维化、软骨丢失、关节疼痛为主要症状的退行性关节疾病,其主要病理变化包括软骨退化、合成代谢减少、软骨下骨重塑、滑膜炎症和骨赘形成,导致关节活动受限和疼痛。由于骨关节炎的复杂性和异质性,临床上迄今缺乏有效的缓解骨关节炎的个性化药物。细胞衰老是影响关节组织稳态并加剧骨关节炎进展的重要因素之一。软骨细胞是成熟软骨中唯一有助于维持关节组织完整性和稳态的细胞,衰老软骨细胞的逐渐积累导致细胞代谢和功能发生改变,最终引起软骨细胞稳态失衡。因此,靶向软骨细胞衰老是治疗骨关节炎的一个有前景的策略。

9月4日,重庆医科大学基础医学院郭风劲教授团队在国际知名期刊《NATURE COMMUNICATIONS》在线发表了题为“10-hydroxy-2-decenoic acid prevents osteoarthritis by targeting aspartyl β hydroxylase and inhibiting chondrocyte senescence in male mice preclinically”的最新研究成果。该研究发现并证实一种来源于蜂王浆的天然小分子化合物10-羟基-2-癸烯酸(10-HDA)具有软骨保护作用,分别从细胞、组织、临床样本、不同小鼠模型等多个层面证实10-HDA能够抑制软骨退化并缓解小鼠的疼痛,同时确定10-HDA通过靶向天冬酰胺β-羟化酶(ASPH)的Asp_Arg_Hydrox结构域的糖基化位点调节软骨代谢、发挥保护作用,通过ERK/p53/p21和GSK3β/p16途径抑制软骨细胞衰老进而延缓软骨的退化。
随着人口老龄化的加剧,骨关节炎的发病率逐年增加。目前在全球范围内影响已超过2.5亿人,严重影响着患者的生活质量。研究表明,在50岁以上人群中,OA可导致长期残疾,最终致死率高达53%。随着人口老龄化加剧和平均寿命的延长,骨关节炎对全球卫生和社会保健系统带来重大挑战。郭风劲教授团队多年来致力于骨与关节功能损伤与重塑机制及药物研发的基础、临床研究,利用我国丰富的中医药资源,创新性的发现一种来源于营养制剂蜂王浆的天然小分子化合物10-HDA具有保护软骨的新型生物学作用。这些发现不仅明确10-HDA可以通过抑制软骨细胞衰老有效治疗骨关节炎,为未来关于10-HDA/ASPH相互作用的研究奠定基础,而且拓宽了我国中医药传统医学的研究视野,揭示10-HDA可能是一种有前途的治疗骨关节炎的靶向药物。
本研究首先证实10-HDA促进软骨细胞的增殖和合成代谢,抑制软骨细胞的凋亡和分解代谢;同时在人体软骨组织中证实,10-HDA增强软骨细胞的合成代谢并抑制分解代谢。接下来研究者构建DMM小鼠OA模型,分别采取关节腔注射和口服饲喂10-HDA的方法,检测并验证了关节腔注射和口服饲喂10-HDA均可以显著促进软骨合成代谢、抑制分解代谢、缓解DMM小鼠的骨关节炎进展和减轻疼痛,对骨关节炎具有一定保护作用(图1,2)。
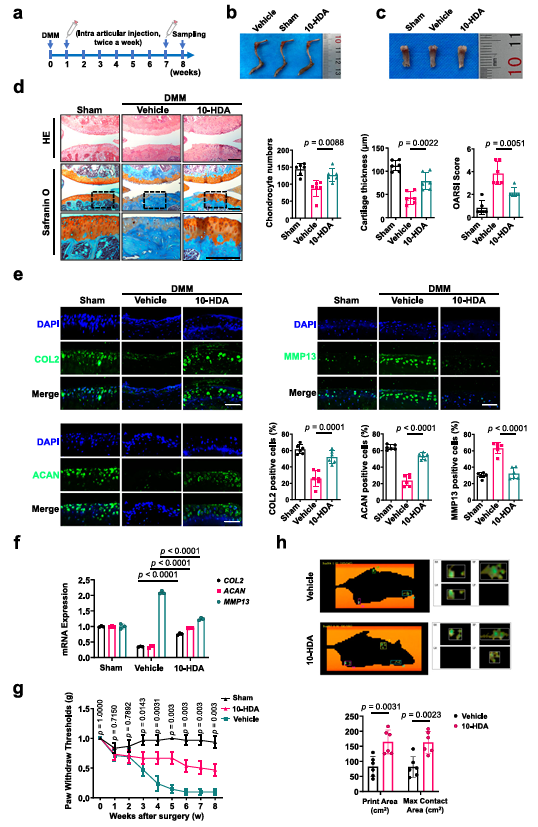
图1. 关节腔注射10-HDA缓解 OA 进展和疼痛。
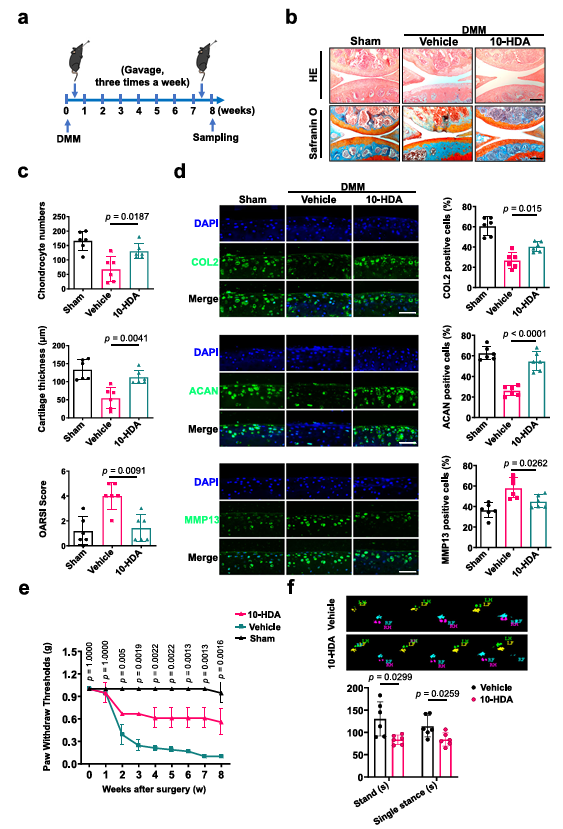
图2.口服饲喂10-HDA缓解 OA 进展和疼痛
为了进一步探究10-HDA保护软骨、缓解OA进展的具体机制,研究者采用药物亲和反应的靶点稳定性实验(DARTS)联合蛋白质质谱分析、细胞热位移(CETSA)、等温剂量反应(ITDR)等方法阐明和鉴定10-HDA靶向天冬酰胺β-羟化酶(ASPH)发挥保护软骨、抑制衰老、调控软骨合成与分解、促进关节软骨的再生修复、缓解 OA 进展的作用和具体机制,并针对ASPH不同结构域构建截短体,联合DARTS验证和确定10-HDA通过靶向ASPH的Asp_Arg_Hydrox结构域的糖基化位点调节软骨代谢、发挥保护作用(图3,4);运用Crispr cas9技术构建ASPH缺陷软骨细胞同时联合高通量RNAseq技术分析ASPH缺陷后,与细胞衰老及衰老相关信号ERK/p53/p21和GSK3β/p16显著富集,研究者进一步在体内、体外验证了10-HDA通过ASPH抑制软骨细胞衰老进而缓解OA进展。衰老小鼠表现出自发性骨关节炎的进展,研究者运用关节腔注射和口服饲喂10-HDA两种不同的方法分别治疗自然衰老小鼠,检测并验证了关节腔注射和口服饲喂10-HDA均可以显著抑制软骨细胞衰老、促进软骨合成代谢、抑制分解代谢、缓解DMM小鼠的骨关节炎进展和减轻疼痛,对骨关节炎具有一定保护作用(图5,6),且10-HDA发挥上述作用依赖于ASPH的Asp_Arg_Hydrox结构域的糖基化位点。
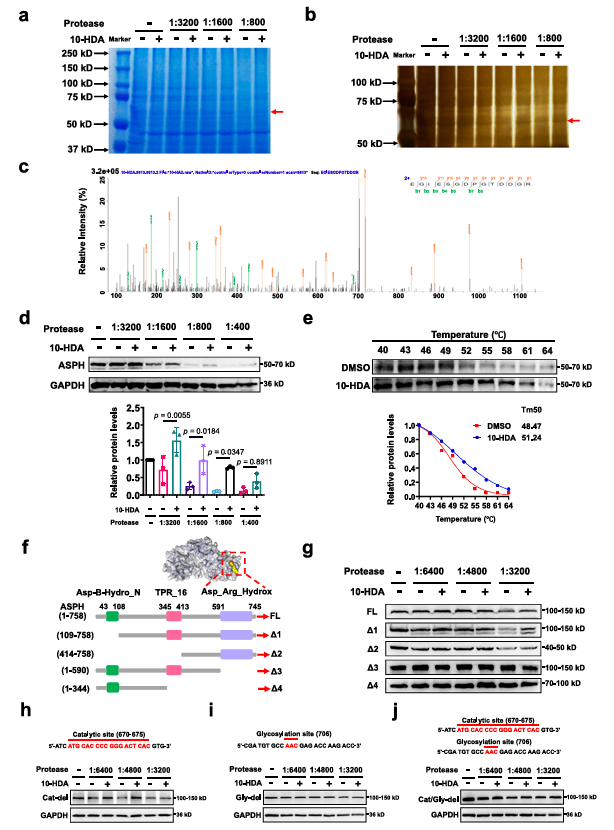
图3. DARTS鉴定ASPH作为10-HDA的新靶点及功能域。
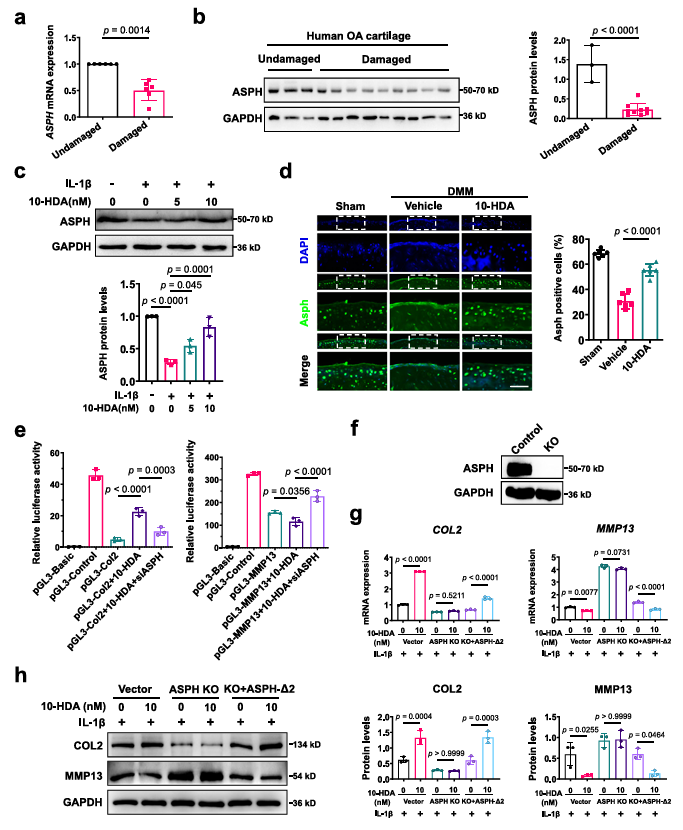
图4. 10-HDA通过ASPH的Asp-Arg-Hydrox结构域调控软骨细胞的合成、分解代谢。
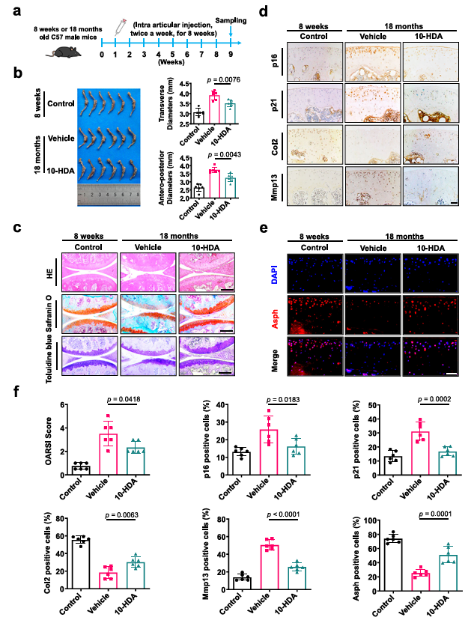
图5. 关节腔注射10-HDA抑制自然衰老小鼠的软骨细胞衰老和软骨退化。
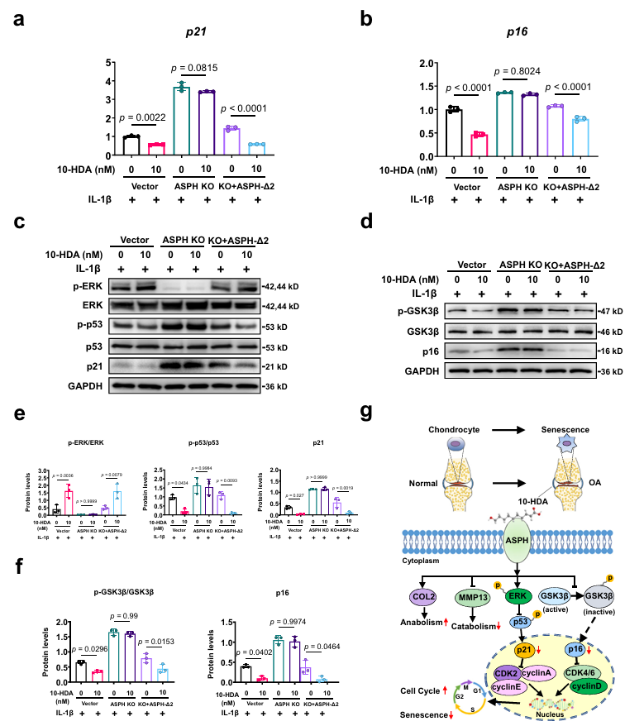
图6. 10-HDA通过调控ASPH/ERK/p53/p21和ASPH/GSK3β/p16信号通路抑制软骨细胞的衰老。
文章结论与讨论,启发与展望
综上所述,研究人员综合利用临床前动物模型、细胞生物学、分子生物学方法、生物信息学分析方法等技术手段,证实了来源于蜂王浆的天然小分子化合物10-羟基-2-癸烯酸(10-HDA)具有新型的软骨保护作用,10-HDA能够抑制软骨退化并缓解OA小鼠的疼痛,同时确定天冬酰胺β-羟化酶(ASPH)是10-HDA在软骨细胞中的新型作用靶点,10-HDA通过靶向ASPH的Asp_Arg_Hydrox结构域的糖基化位点调节软骨代谢、发挥保护作用,通过ERK/p53/p21和GSK3β/p16途径抑制软骨细胞衰老进而延缓软骨的退化。该研究有望为骨关节炎的抗衰老药物研发提供重要的新靶点。
重庆医科大学基础医学院(附属第二医院双聘)郭风劲教授为该论文唯一通讯作者,基础医学院博士后耿娜娜、青年教师范梦恬为论文并列第一作者。该研究工作得到超声医学工程国家重点实验室、重医附属第二医院、重医附属第一医院、陆军军医大学附属大坪医院陈林教授研究团队的大力协助。同时得到国家自然科学基金、重庆市自然科学基金、重庆市留学回国创业创新支持计划、重庆医科大学特聘教授、重庆医科大学未来医学青年创新团队等多项基金的资助。
原文链接:
https://www.nature.com/articles/s41467-024-51746-3.pdf


