Nat Cardiovasc Res 陆军军医大学曾春雨教授团队发现α-酮戊二酸能够促进心肌再生以及成年心肌细胞增殖
时间:2024-09-06 06:00:28 热度:37.1℃ 作者:网络
心肌梗死是当今社会人类死亡的主要病因。心肌梗死后大量心肌细胞发生坏死和凋亡,因成年心肌无法通过自我增殖进行修复,心功能不断恶化,最终发展为心力衰竭。目前临床上所采用的药物治疗、介入治疗和冠脉旁路搭桥术等方法有助于改善患者的症状,恢复血供,但都不能从根本上更新和修复坏死心肌。因此,心功能的修复最终还需依靠于心肌再生。然而长时间以来,成年哺乳动物心脏一直被认为是终末分化器官,不具有再生能力。但是,近年来对于心肌细胞中C14以及胸苷类似物碘脱氧尿苷的追踪证实了成年人心肌细胞存在低频更新,每年仅以1~2%的速率进行缓慢更替,远不能修复心梗后大量心肌坏死所导致的心功能损伤。因此,如何促进成年心肌细胞增殖并阐明其中机制是心肌再生领域的关键。
柠檬酸循环,也被称为三羧酸循环(tricarboxylic acid (TCA) cycle),能够将营养物质转化为能量和生物合成所需的重要代谢物,在细胞的各种生物过程中都扮演着重要角色。虽然TCA循环代谢产物在维持癌细胞和干细胞的细胞活力以及增殖中的作用已被报道,但其对心肌细胞增殖的影响仍知之甚少。
2024年9月2日,陆军军医大学大坪医院心血管内科曾春雨教授团队在Nature Cardiovascular Research上发表题为“α-Ketoglutarate promotes cardiomyocyte proliferation and heart regeneration after myocardial infarction”的研究论文。该研究揭示了代谢产物α-酮戊二酸在促进成年心肌细胞增殖以及修复心梗心肌中的作用,进一步研究分子机制发现,α-酮戊二酸通过激活去甲基化酶JMJD3活性、增强其对H3K27me3的去甲基化作用,从而解除H3K27me3对细胞周期调节基因的抑制。这一发现为促进内源性心肌再生以治疗心肌梗死提供新的方向。

哺乳动物在出生早期仍具有较强心肌增殖能力,研究发现出生后1天(P1)的小鼠心尖部分切除后可通过心肌细胞增殖实现心肌再生,但该能力在出生后第7天(P7)急剧下降。基于此,本研究首先利用已发表的新生(P0.5)和出生后7天(P7)小鼠的心脏代谢组学数据,对心脏中的差异TCA代谢产物进行筛选,发现α-酮戊二酸含量在P7小鼠心脏中的含量显著减少。为了明确补充α-酮戊二酸是否能够促进发育过程中小鼠的心肌细胞增殖,研究者外源给予小鼠α-酮戊二酸,结果发现给予P7小鼠腹腔注射α-酮戊二酸后,其心肌细胞增殖能力明显增强,提示α-酮戊二酸是调控心肌细胞增殖的重要因子(图1)。
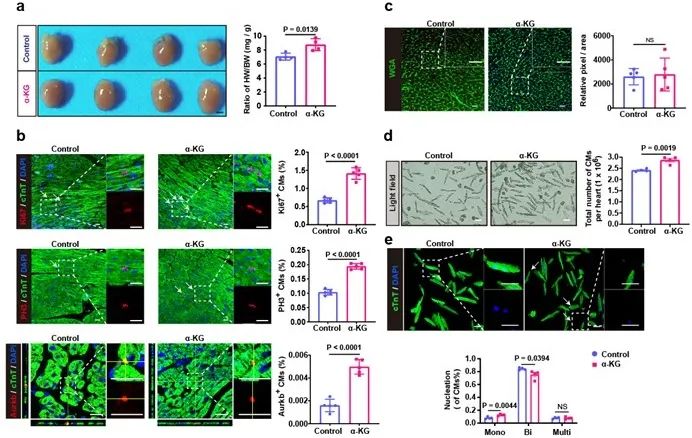
图1. α-酮戊二酸促进发育期小鼠心肌细胞增殖
为进一步探明α-酮戊二酸能否在心肌梗死中发挥保护作用并促进成年心肌细胞增殖,研究者构建了小鼠心肌梗死模型并外源给予α-酮戊二酸。发现补充α-酮戊二酸能够改善梗死后心功能,减小梗死面积并促进成年心肌细胞增殖。这一结果表明,外源补充α-酮戊二酸能够有效促进成年心肌细胞增殖,并促进梗死后心肌修复(图2)。
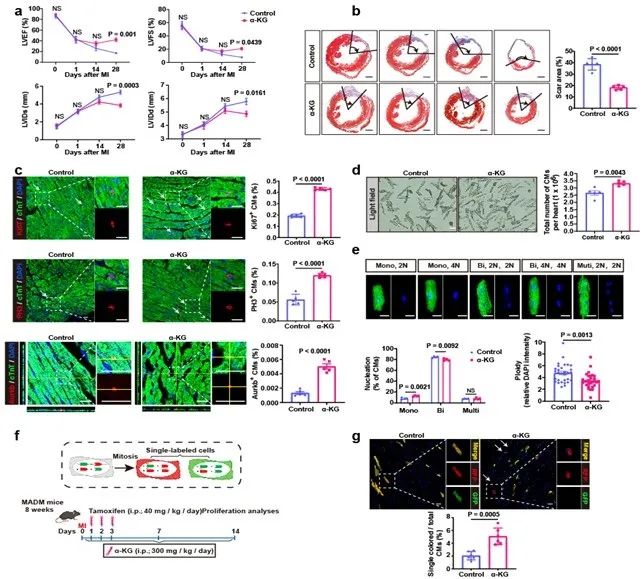
图2. α-酮戊二酸促进心肌梗死小鼠心肌再生以及成年心肌细胞增殖
为了深入了解α-酮戊二酸促进心肌细胞增殖的潜在途径,研究者对α-酮戊二酸注射组和对照组小鼠分离的心肌细胞进行了RNA测序分析。GO分析结果显示,上调的差异基因富集于细胞增殖相关通路,包括细胞增殖、有丝分裂细胞周期以及细胞增殖的正向调控等。基因热图进一步显示,α-酮戊二酸注射后,大部分细胞周期和细胞分裂基因转录增加(图3)。
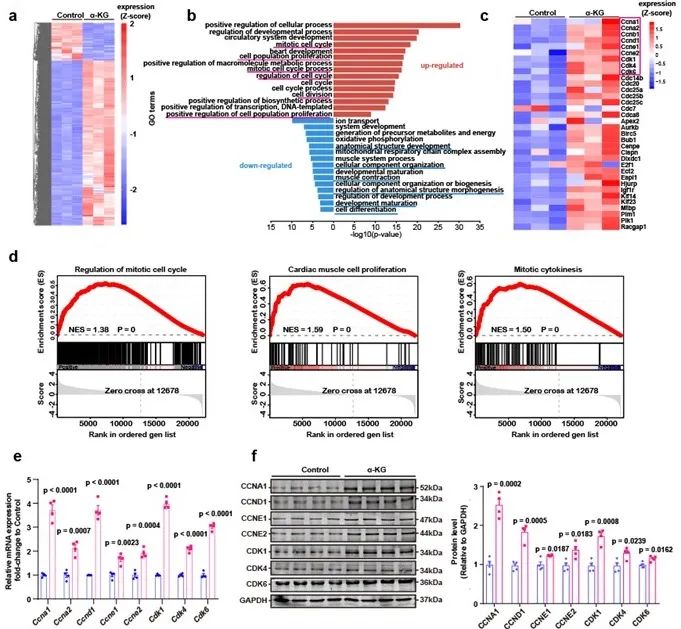
图3. α-酮戊二酸促进心肌细胞中细胞周期基因的转录表达
既往研究表明,α-酮戊二酸能够通过影响H3K4me3、H3K9me3、H4K20me3、H3K27me3和H3K36me3等组蛋白赖氨酸甲基化来调节染色质可及性,从而维持胚胎干细胞的多能性。并且,近年来大量证据显示,组蛋白修饰在调控心肌细胞增殖中发挥着重要作用。因此,为了探明α-酮戊二酸影响心肌细胞增殖的分子机制,研究者对P1和P28小鼠心脏中的组蛋白修饰水平进行检测,发现P28小鼠心脏中的H3K27me3表达量显著升高。而且,给予α-酮戊二酸可明显逆转H3K27me3的水平。染色质免疫共沉淀测序(ChIP-seq)结果进一步证明,α-酮戊二酸能够减少H3K27me3在细胞周期基因上的富集(图4)。
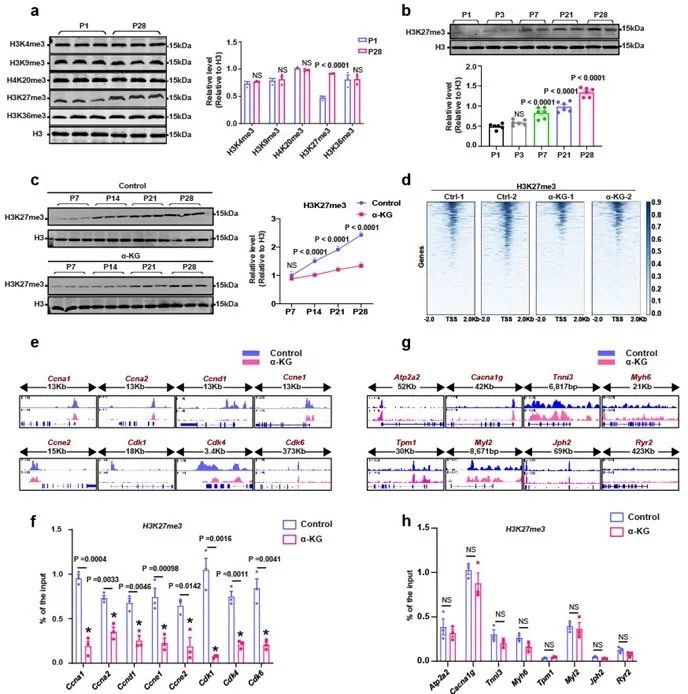
图4. α-酮戊二酸处理减少H3K27me3在细胞周期基因上的富集
JMJD3是催化H3K27me3去甲基化的酶,而作为JMJD3的共因子,α-酮戊二酸能够激活JMJD3的去甲基化效应。为进一步明确JMJD3是否作为α-酮戊二酸促进心肌细胞增殖的靶点,研究者利用JMJD3的小分子抑制剂GSK-J4抑制其活性,并发现GSK-J4可有效阻断α-酮戊二酸促进梗死后成年心肌细胞增殖的作用。此外,细胞实验结果显示,过表达JMJD3不仅能够促进心肌细胞增殖,还能够放大α-酮戊二酸的促心肌细胞增殖效应。上述结果从正反两个方向说明JMJD3介导的H3K27me3的去甲基化可能是α-酮戊二酸促进心肌细胞增殖的潜在靶点(图5)。
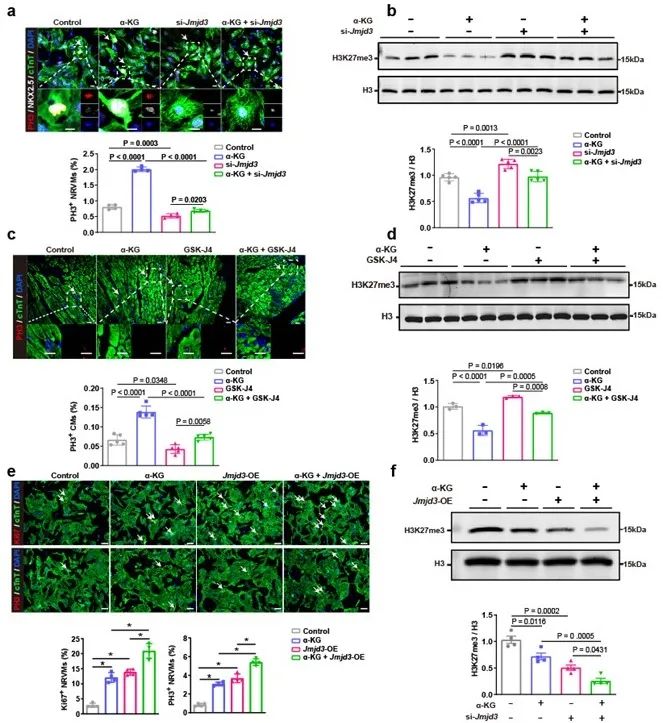
图5. α-酮戊二酸通过激活JMJD3促进心肌细胞增殖
进一步对已发表的P1、P4、P9和P23小鼠心脏转录组测序和蛋白质组学数据进行分析,发现α-酮戊二酸脱氢酶(α-KG-dehydrogenase, OGDH)在心脏中的表达量随年龄逐渐升高,提示OGDH调控的α-酮戊二酸分解代谢可能是成年心肌细胞内源性α-酮戊二酸水平降低的原因。因此,研究者利用AAV9-shRNA特异性敲低小鼠心肌细胞中的OGDH并构建心肌梗死模型,发现敲低OGDH能够增加心肌细胞中的内源性α-酮戊二酸,并促进梗死后心肌再生以及成年心肌细胞增殖。上述结果表明,通过敲低OGDH,阻断α-酮戊二酸的去路、增加内源性α-酮戊二酸含量能够促进梗死后心肌修复以及成年心肌细胞增殖(图6)。
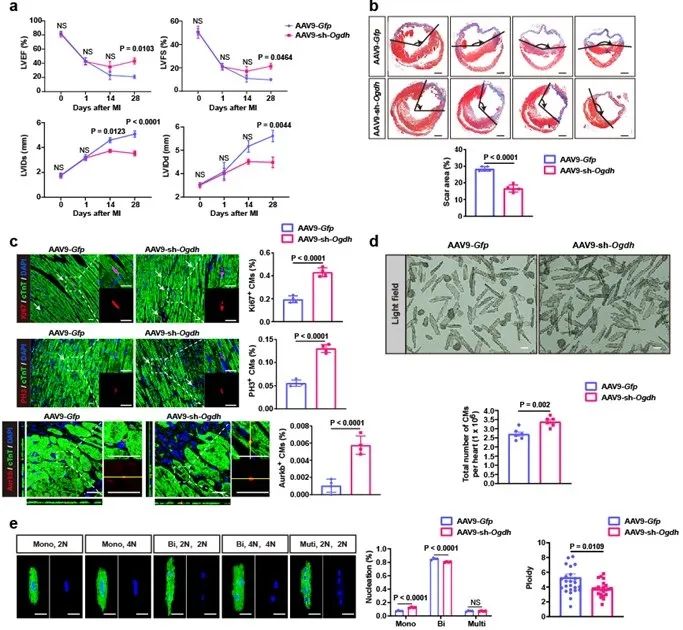
图6. 敲低OGDH促进心肌再生以及成年心肌细胞增殖
综上所述,本研究发现α-酮戊二酸能够促进发育期小鼠心肌细胞增殖;促进梗死后心肌再生以及成年心肌细胞增殖。分子机制层面,α-酮戊二酸激活JMJD3的去甲基化活性,解除H3K27me3对细胞周期调节基因的抑制,进而促进心肌细胞增殖(图7)。
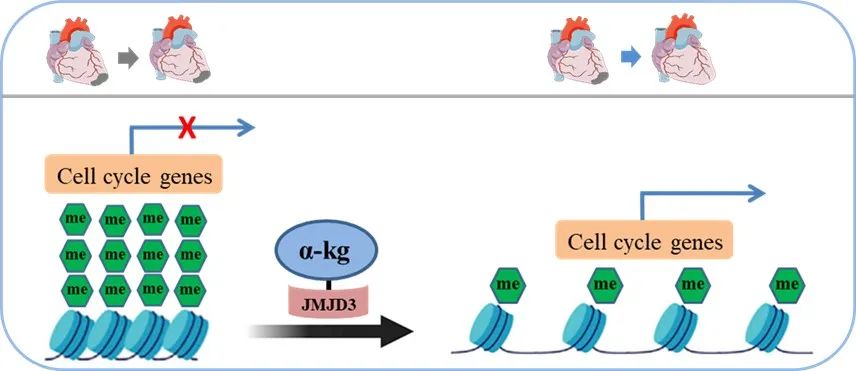
图7. α-酮戊二酸促进心肌再生以及心肌细胞增殖示意图
陆军军医大学大坪医院心血管内科曾春雨教授为本文通讯作者。时宇、田苗、唐陆勋博士以及赵小芳硕士为本文第一作者。本研究得到国家重点研发计划项目(2022YFA1104500)、国家自然基金重点项目(81930008)、面上项目(82170288)的支持。此外,本研究还得到乔治华盛顿大学Pedro A. Jose教授的大力支持。
原文链接:
https://www.nature.com/articles/s44161-024-00531-y


