最新Nature大子刊:启动全身抗肿瘤免疫!
时间:2024-08-13 15:00:57 热度:37.1℃ 作者:网络
系统性施用的细胞因子是有效的免疫疗法,但会引起严重的剂量限制性毒性。为了克服这一挑战,细胞因子可被设计为局部递送并在肿瘤内滞留。然而,尽管诱导了治疗病变的消退,但肿瘤局部细胞因子在远端未治疗的肿瘤中通常只能引起较低的反应。
在此,麻省理工学院Darrell J. Irvine和K. Dane Wittrup等人报告了一种局部细胞因子疗法,该疗法通过靶向无处不在的白细胞受体CD45安全地引发全身抗肿瘤免疫。研究发现,CD45靶向免疫细胞因子的内化率低于野生型,导致淋巴细胞之间持续的下游顺式和反式信号传导。在多个同基因小鼠肿瘤模型中,单次瘤内注射αCD45白细胞介素(IL)-12,然后注射单次αCD45-IL-15,可根除治疗过的肿瘤和未治疗的远端病变,且无毒性。从机制上讲,靶向CD45的细胞因子重新编程了肿瘤引流淋巴结中的肿瘤特异性CD8+T细胞,使其具有抗病毒转录特征。CD45锚定代表了宿主免疫细胞用于免疫治疗的蛋白质保留的广泛平台。相关工作以“Local delivery of cell surface-targeted immunocytokines programs systemic antitumor immunity”为题发表在Nature Immunology。

【文章要点】
本文报告了一种针对通用白细胞受体CD45的细胞因子的局部免疫治疗方案。作者之前已经证明,针对无处不在的白细胞表面受体CD45的抗体会结合T细胞和其他淋巴细胞的表面,而不会引发内化。因此,作者假设,与这些细胞因子的天然形式相比,使用抗CD45靶向锚定在细胞表面的细胞因子可能表现出新的生物学效应。为了测试这一点,作者生成了αCD45免疫细胞因子与IL-15的融合物作为试验台有效载荷。将小鼠超促性腺激素IL-15(IL-15与其受体α链结构域IL-15Rαsushi连接)羧基末端融合到携带LALA-PG效应器衰减突变的抗CD45免疫球蛋白(Ig)G2c抗体的重链上(以下简称αCD45-IL-15)。此外,作者还将这种细胞表面靶向应用于细胞因子IL-12。CD45靶向免疫细胞因子保留在细胞表面,并相对于其天然细胞因子对应物触发增强和延长的信号传导(图1)。
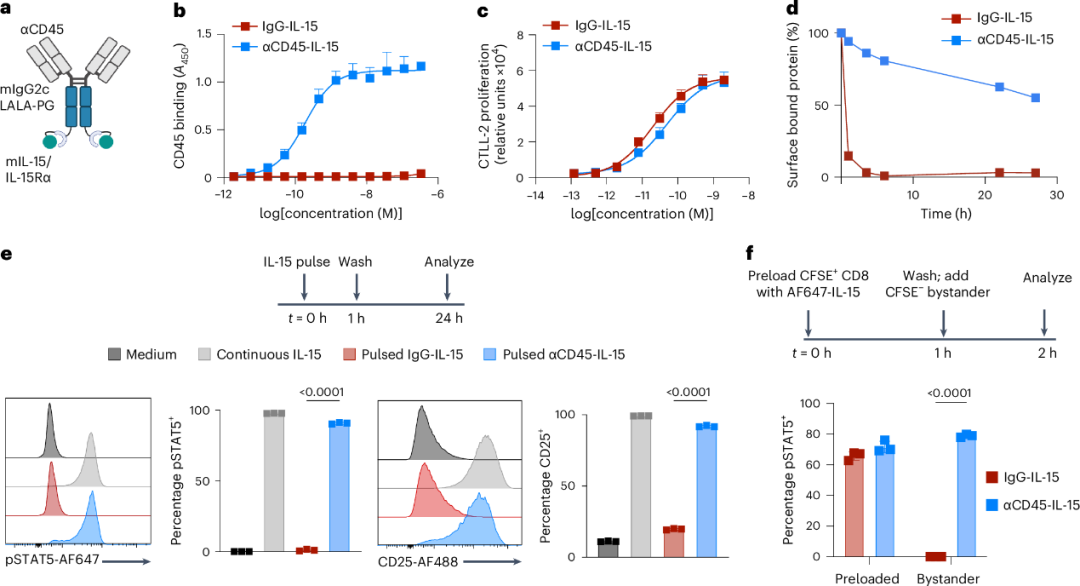
图1 CD45免疫细胞因子保留在细胞表面并显示扩展的信号传导
作者通过优化剂量水平、组织定位和时间可以产生一种高效无毒的细胞因子疗法,能够根除治疗过的肿瘤,并在多个同基因模型中在远端病变处引起完全反应。集中在肿瘤中的单剂量CD45靶向IL-12,随后在肿瘤和TDLN中积累的单剂量CD445靶向IL-15,改变了TDLN中的T细胞编程,扩增了具有转录特征的肿瘤特异性CD8+T细胞,反映了对急性病毒感染的有效反应。这种强效效应T细胞池的传播导致了全身性抗肿瘤免疫,其特征是在治疗和未治疗的肿瘤中都有完全反应(图2)。
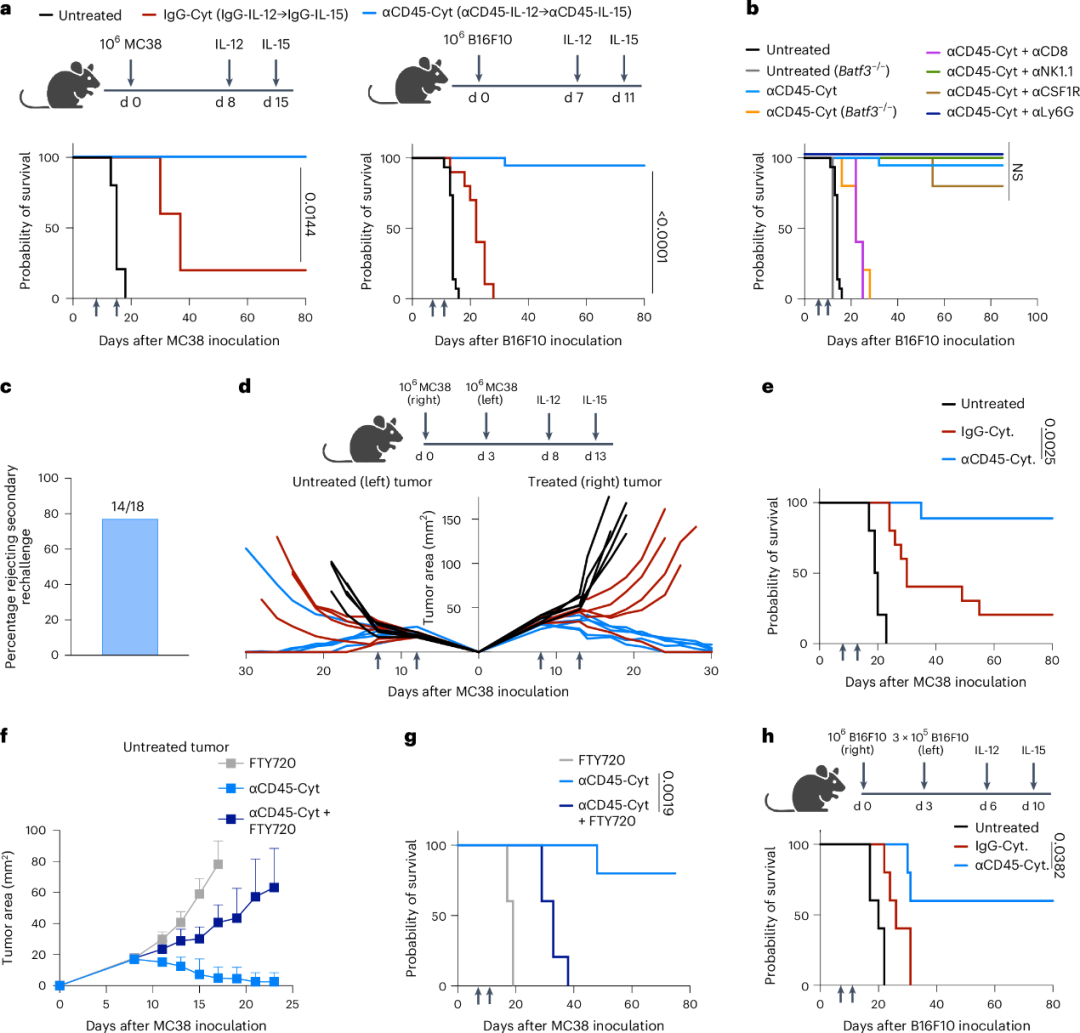
图2 αCD45–细胞因子疗法根除已治疗的肿瘤并引发强大的全身反应
原文链接:
https://www.nature.com/articles/s41590-024-01925-7


