读书报告 | HUDSON研究:基于生物标志物选择的靶向治疗联合度伐利尤单抗治疗晚期NSCLC的饿期伞试验
时间:2024-07-02 10:05:41 热度:37.1℃ 作者:网络
导读
晚期非小细胞肺癌(NSCLC)患者接受的治疗方案主要基于其分子分型。但目前对于没有可靶向的位点突变的NSCLC患者,标准的治疗是抗PD-(L)1的免疫治疗联合或不联合含铂双药治疗。然而,并不是所有患者都获得持久的益处,对免疫治疗产生抵抗是常见的。
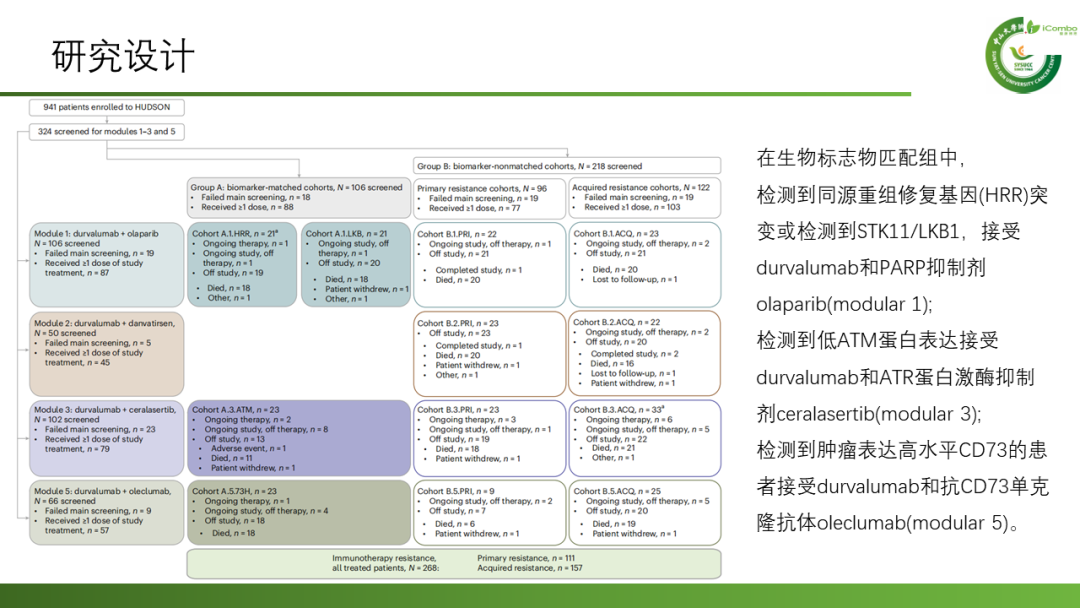
HUDSON研究(NCT03334617)是一项正在进行的、开放标签、多中心、非随机、模块化的2期伞状临床研究,该研究入组268名转移性或局部晚期和复发性NSCLC患者,既往接受抗PD-1/PD-L1治疗联合或未联合含铂双药方案并发生疾病进展。通过一致的基因组检测方法对患者进行肿瘤分子谱筛查,将患者分配至生物标志物匹配组或生物标志物不匹配组。根据肿瘤分子谱筛查结果,生物标志物匹配组患者分别接受:1)durvalumab联合PARP抑制剂olaparib;2)durvalumab联合ATR蛋白激酶抑制剂ceralasertib;3)durvalumab联合抗CD73单克隆抗体oleclumab;4)durvalumab联合STAT3 抑制剂Danvatirsen。
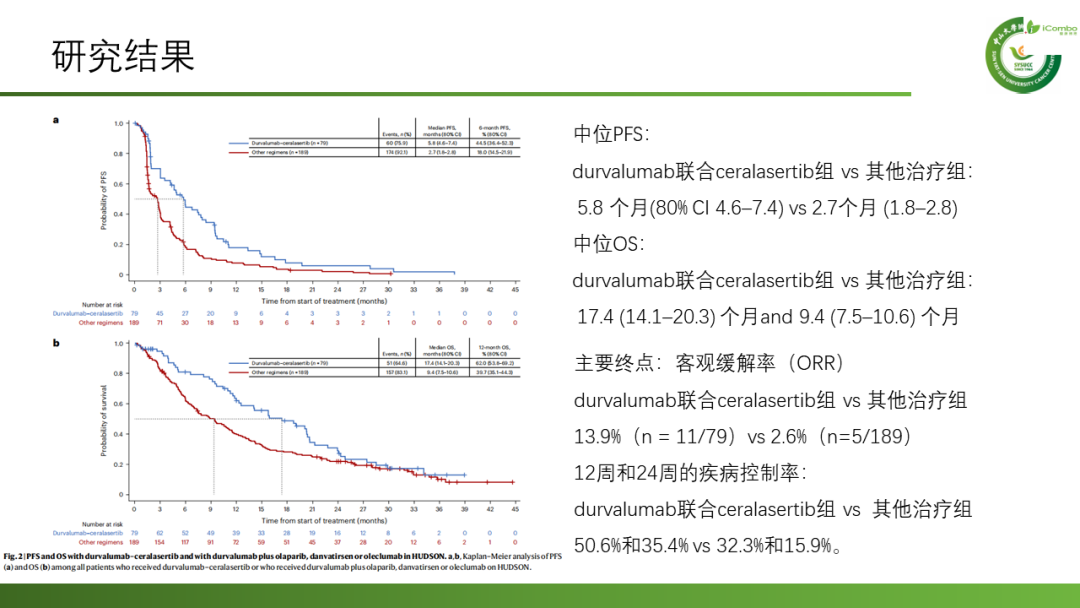
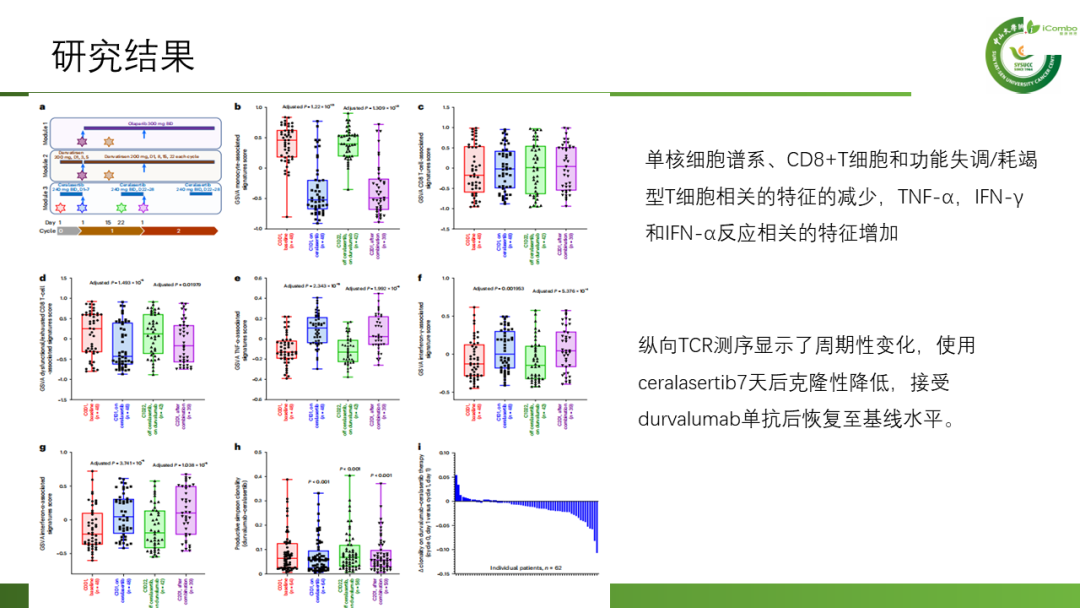
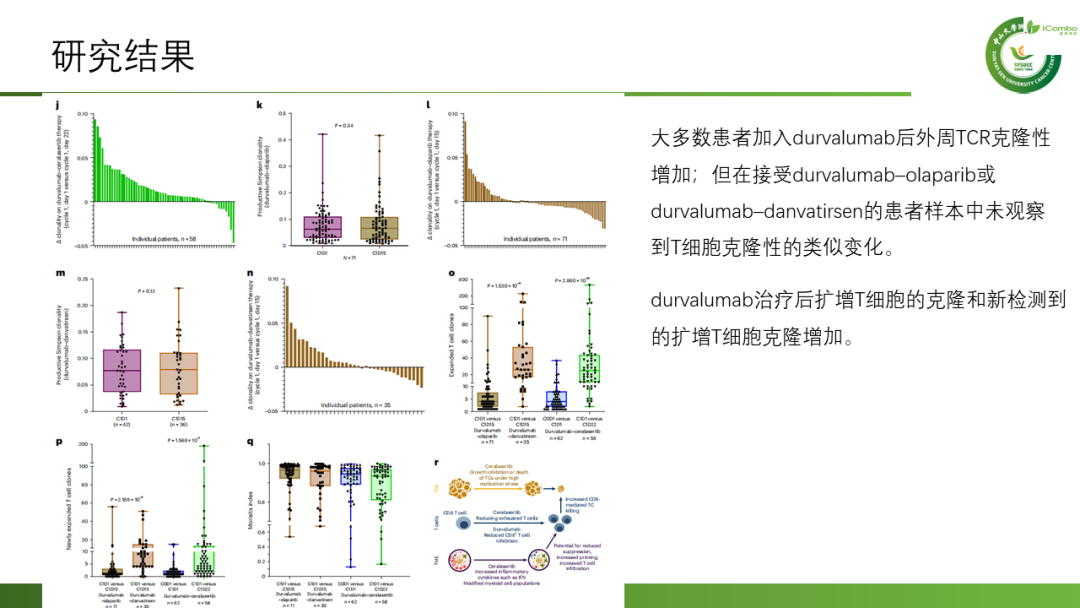
研究结果:在中位PFS方面,durvalumab联合ceralasertib组对比其他治疗组为5.8 个月(80% CI 4.6–7.4)对比2.7个月 (1.8–2.8),中位OS为17.4 (14.1–20.3) 个月对比9.4 (7.5–10.6) 个月。在客观缓解率(ORR)方面,durvalumab联合ceralasertib组对比其他治疗组为13.9%(n = 11/79)对比2.6%(n=5/189)。
HUDSON临床试验显示了durvalumab–ceralasertib组在多线治疗后进展的NSCLC中的显著疗效,与其他方案相比,反应率和疾病控制率明显更高,PFS和OS明显更长,提示在NSCLC免疫治疗进展后中,加入ceralasertib具有潜在的免疫治疗致敏作用(Nat Med. 2024 Mar;30(3):716-729. doi: 10.1038/s41591-024-02808-y)。