首创AKT抑制剂capivasertib治疗三阴性乳腺癌III期临床失败!
时间:2024-06-28 06:00:29 热度:37.1℃ 作者:网络
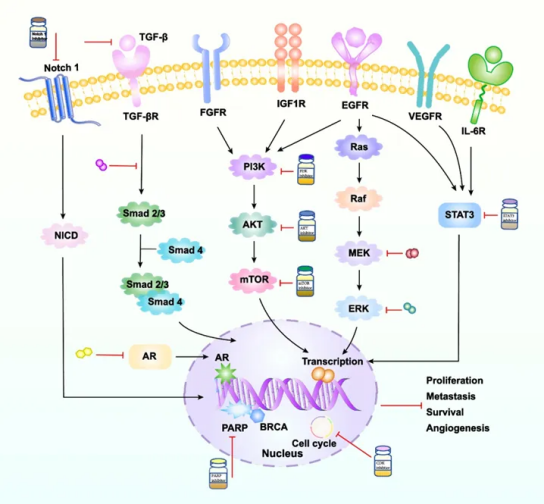
乳腺癌是全球第二大常见癌症,也是导致癌症相关死亡的主要原因之一。其中,三阴性乳腺癌(TNBC)是一种高度侵袭性的乳腺癌亚型,占乳腺癌的 15-20%。由于缺乏雌激素受体(ER)、孕激素受体(PR)和HER2的表达,传统的内分泌治疗和HER2靶向治疗在这类患者中效果有限。目前,化疗仍是TNBC的主要治疗手段,但疗效有限,且副作用较大。晚期或转移性TNBC患者的平均OS为12至18个月,只有约14%的患者在诊断后存活5年。 近日,在乳腺癌治疗领域风头正劲,阿斯利康首创AKT抑制剂Truqap(capivasertib)传来一条令人遗憾的消息:在III期CAPItello-290临床试验中,capivasertib联合紫杉醇一线治疗局部晚期(无法手术)或转移性三阴性乳腺癌(TNBC)患者的III期 CAPItello-290 临床试验未达到总生存期(OS)双重主要终点。可见,最厉害的三阴性乳腺癌治疗有多么困难! 这一结果不仅让研发团队“感到失望”,也再次让人切身感受到三阴性乳腺癌攻坚之难。capivasertib在III期CAPItello-290临床试验中到底发生了什么?三阴性乳腺癌的治疗现状以及靶向治疗的进展如何?我们一起来看! Capivasertib III期 CAPItello-290 惜败三阴性乳腺癌 Capivasertib是同类首创的AKT1/2/3高效选择性抑制剂,在治疗HR+/HER2-乳腺癌中取得突破。此前报道:NMPA受理首个AKT靶点药物Capivasertib!乳腺癌患者治疗迎来新曙光。 2023年11月,它获FDA批准与fulvestrant联合用于治疗此类患者,成为全球首个获批的AKT通路抑制剂。见:NEJM:Capivasertib对HR阳性乳腺癌的治疗效果(CAPItello-291研究)、Lancet Oncol:Capivasertib联合氟维司群可显著延长晚期乳腺癌患者的无进展存活期 III期 CAPItello-290 临床试验旨在评估Capivasertib化疗组合在特定TNBC患者中的潜在一线治疗效果。该研究特别评估了两个主要终点:一是总体试验人群中的OS改善情况,二是携带PIK3CA、AKT1或PTEN生物标志物变异的肿瘤患者亚组的OS改善情况,涉及923名患者。阿斯利康在其公告中并未提供具体数据,只透露Capivasertib组合在总研究人群或携带PIK3CA、AKT1或PTEN基因特定突变的患者亚组中,均未能显著提高总生存期。 TNBC 的传统治疗方法,包括化疗、放疗和手术 因此,寻找更有效的治疗手段迫在眉睫。研究表明,大约35%的TNBC 病例显示PIK3CA、AKT1和PTEN 蛋白发生改变。以Capivasertib攻坚三阴性乳腺癌的III期 CAPItello-290备受关注。 三阴性乳腺癌靶向治疗进展 近些年,根据 TNBC 表达的特定分子和信号通路,出现了多种靶向治疗策略,包括 PI3K/AKT/mTOR 抑制剂、表皮生长因子受体(EGFR)抑制剂、Notch 抑制剂、PARP 抑制剂等。 TNBC 相关信号通路及其抑制剂 1.多聚腺苷二磷酸核糖聚合酶 (PARP) 抑制剂 恶性肿瘤细胞易发生BRCA基因突变,如TNBC患者的BRCA1/2基因。PARP是修复DNA单链损伤的关键酶,PARP抑制剂可导致BRCA1/2缺陷癌症的“合成死亡”。FDA已批准奥拉帕尼和他拉唑帕尼等PARP抑制剂用于BRCA突变的HER2阴性BC患者治疗。 奥拉帕尼:比较奥拉帕尼单药治疗或标准治疗的 HER2 阴性转移性乳腺癌的OlympiAD显示,与标准治疗相比,奥拉帕尼单药治疗延长了 2.8 个月的中位PFS,降低了42%疾病进展或死亡风险,并延长了OS。OlympiA试验则显示,奥拉帕尼在携带BRCA1/2种系突变的早期HER2阴性BC患者辅助治疗中显著改善OS、3 年无侵袭性疾病生存率(iDFS)及无远处疾病生存率(DDFS)。 他拉唑帕尼:EMBRACA试验显示,与化疗相比,他拉唑帕尼组的PFS更长(8.6 个月 vs. 5.6 个月),ORR更高(62.6% vs. 27.2%)。NEOTALA试验显示,他拉唑帕尼单药用于具有BRCA1/2种系突变的HER2阴性BC患者的新辅助治疗中,pCR率显著较高。 2.雄激素受体(AR)抑制剂 约 12% 的 HR 阴性 BC 患者中存在 AR 阳性表达。目前,研究人员已探索出许多用于 TNBC 治疗的 AR 抑制剂。虽然临床试验证明AR抑制剂对TNBC患者的治疗有效,但其确切机制尚不清楚。 比卡鲁胺:治疗TNBC的临床获益率 (CBR) 为 19%,mPFS 为 3 个月,且患者耐受性良好。 恩杂鲁胺:在 AR 阳性 TNBC 患者中 mPFS 和 mOS 分别为 3.3 和 17.6 个月,因此,建议恩杂鲁胺可用于治疗 AR 阳性 TNBC 患者。TBCRC032 试验表明,恩杂鲁胺和 taselisibin 联合治疗 AR 阳性 TNBC 患者 CBR 达 35.7%,mPFS 为 3.4 个月。 阿比特龙:评估阿比特龙联合泼尼松治疗 AR 阳性局晚期 TNBC 的UCBG 12-1 试验表明,接受阿比特龙治疗的患者 mPFS 为 7.5 个月,ORR 为 8.22%,CBR 达 20%。 3.CDK 抑制剂 CDK 是调节细胞周期各阶段过渡的关键酶,持续激活可导致肿瘤细胞增殖。CDK4/6 抑制剂主要抑制 G1-S 期,从而抑制细胞 DNA 复制过程。FDA 已批准 CDK4/6 抑制剂用于治疗 TNBC 患者,其中包括哌柏西利 (Palbociclib) 和瑞波西利 (Ribociclib)。 哌柏西利:既往 PALOMA-2 试验和 PALOMA-3 试验证实,哌柏西利联合内分泌治疗可显著改善了 ER+/HER2− BC 患者的 PFS。 瑞波西利:与哌柏西利类似,瑞波西利联合氟维司群显著改善 ER+/HER2− BC 患者的 OS。 阿贝西利:与哌柏西利相比,阿贝西利联合内分泌治疗可能会延长 ER+/HER2− BC 患者的 iDFS,且具有良好的安全性。此外,阿贝西利联合氟维司群治疗 ER+/HER2− BC 患者可显著改善 PFS 和 ORR。 CDK4/6 抑制剂治疗 TNBC 患者的临床试验仍在进行中。 4.PI3K/AKT/mTOR 信号通路抑制剂 PI3K/AKT/mTOR 信号通路是最普遍的癌症激活通路,它导致肿瘤细胞的增殖和一系列其他恶性生物学行为。据报道,约10%的TNBC存在PI3KCA突变。 LY294002是首个PI3K抑制剂,SF1126为其修饰形式,可抑制肿瘤和血管生成,SF1126与吉非替尼联合可诱导TNBC细胞凋亡。 除 PI3K 抑制剂外,还有 AKT 抑制剂在临床试验中。AZD5363 用于治疗 BC、胃癌和前列腺癌。Ipatasertib 作为 TNBC 的单一疗法。Capivasertib对 AKT1/E17K 突变的肿瘤有抗肿瘤活性。LOTUS 和 PAKT 研究显示,在 mTNBC 紫杉醇治疗中加入 AKT 抑制剂可延长 PFS。FAIRLANE 研究评估了 ipatasertib 联合紫杉醇治疗早期 TNBC 的有效性。 目前,第一代mTOR抑制剂已用于治疗乳腺癌,但针对TNBC的PI3K抑制剂仍在I期临床试验中。 5.表皮生长因子受体 (EGFR) 信号通路抑制剂 EGFR 是 89%TNBC 患者的有效治疗靶点,EGFR 靶向药已被批准用于治疗癌症患者,包括酪氨酸激酶抑制剂(TKI)吉非替尼和单克隆抗体西妥昔单抗等。 吉非替尼抑制 BC 细胞增殖并增加卡铂和多西他赛的细胞毒性。此外,联合使用吉非替尼、卡铂和多西紫杉醇三种抑制剂可能会协同增加 TNBC 细胞的细胞毒性。在转移性 TNBC 患者中,西妥昔单抗联合卡铂或西妥昔单抗联合顺铂可使 pCR 加倍,并延长 PFS 和 OS。 6.成纤维细胞生长因子受体(FGFR) TNBC 中存在 FGFR1 或 FGFR2 的扩增,FGFR1 的激活与 OS 的预后有关。研究表明,FGFR 靶向治疗在乳腺癌治疗中有显著疗效,尤其是当 FGFR 扩增时。 7.血管内皮生长因子受体(VEGFR) 目前,常用的抗 VEGF 药物是贝伐珠单抗。III 期 RIBBON 1 试验表明,贝伐珠单抗与卡培他滨、蒽环类或紫杉类药物联合使用均可改善 mTNBC 患者的 PFS。进一步随访分析显示,与安慰剂组相比,贝伐珠单抗联合组 TNBC 患者的 mPFS 明显延长(6.0 个月 vs 2.7 个月),并且 OS 有改善趋势。 8.Notch 信号通路抑制剂 Notch 信号通路的异常激活与 TNBC 的恶性生物学行为和预后有关。因此,深入探讨 TNBC 在该信号通路中的作用,将进一步加深对 TNBC 发病机制的认识,从而探索新的靶向治疗策略。 9.STAT3信号通路抑制剂 STAT3在TNBC干细胞的进展中起着关键作用。新型 STAT3 抑制剂 WZ-2-033通过阻断 STAT3 的活化,在体内和体外都能显著抑制 TNBC 的增殖和致瘤性。 10.转化生长因子 (TGF)-β 抑制剂 TGF-β 与 TNBC 患者的预后呈负相关。双功能融合蛋白 Bintrafusp alfa 旨在同时抑制肿瘤微环境中的两种免疫抑制途径。研究表明,与单药治疗相比,Bintrafusp alfa 能更有效地阻断 TGF-β,并显示出更强的抗肿瘤反应。抗 TGF-β/PD-L1 双特异性抗体 YM101对 TNBC 表现出更强的抑瘤活性。TGF-β抑制剂可能成为治疗TNBC的有效手段。 结语 目前,三阴性乳腺癌仍是肿瘤治疗领域最具挑战性的方向之一。然而,随着对疾病分子机制的深入了解和新药研发的不断进展,我们有理由相信,未来将有更多的治疗选择。尽管AKT抑制剂在III期临床试验中遭遇了挫折,但这不会阻挡我们攻坚“最凶险”乳腺癌的脚步。让我们一起期待未来,乳腺癌患者将有更多效果更好、毒性更少的靶向治疗选择。 参考文献: [1] AstraZeneca’s Truqap Flops in Phase III Triple-Negative Breast Cancer Trial.By Tristan Manalac.Published: Jun 18, 2024. [2] [2]AstraZeneca's Truqap misses the mark in late-stage triple-negative breast cancer trial.By Fraiser Kansteiner.Jun 18, 2024 9:09am. [3] Zhu, S., Wu, Y., Song, B. et al. Recent advances in targeted strategies for triple-negative breast cancer. J Hematol Oncol 16, 100 (2023). https://doi.org/10.1186/s13045-023-01497-3