结肠癌转移能活多久?一例 69 岁女性肝转移性结肠癌病例分享
时间:2024-06-16 06:04:39 热度:37.1℃ 作者:网络
01病例介绍
患者:女性,69 岁
就诊时间:2016 年 12 月
既往史:有高血压病史 20 余年,规律口服硝苯地平缓释片,血压控制可。
个人史/婚育史/家族史/过敏史:无特殊。
现病史:患者 2015-12-15 因“反复腹痛 1 月余”就诊当地医院,查 CEA 25.2ng/ml,
CT 检查示降结肠肿物,考虑结肠癌。
2015-12-15 当地医院开腹行降结肠切除术,术后病理示降结肠腺癌,肠周淋巴结(0/12)
未见癌转移,免疫组化不详。术后行 6 次辅助化疗(具体方案不详)。
2016 年 12 月初当地医院复查,上腹部增强 CT 提示肝右叶下段占位(47╳45╳55mm)。
病理会诊: (降结肠)中分化腺癌,伴坏死。癌组织侵犯肠壁全层。
免疫组化:CK20(+),CDX-2(+),Villin(+),ki-67(+,80%),P53(错意义突变型);
错配修复蛋白 MSH2(+),MSH6(+),MLH1(+),PMS2(+)。
肿瘤标志物:
CEA:17.5ng/ml;CA19-9:118.08U/ml。
影像学检查
头、胸及盆腔 CT 和骨ECT:无特殊。
(普美显)肝脏 MR:
肝右叶转移瘤,大小约 64 ╳ 54mm.
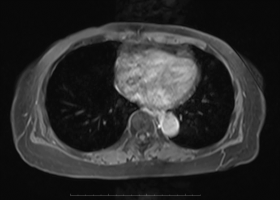
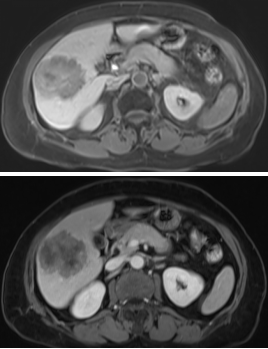
CRS 2 分,
手术治疗:2016-12-27 全麻下行肝右叶转移瘤切除术。
术后病理:(肝肿物)中分化腺癌,伴显著坏死,侵犯突破肝被膜,累及肝切缘。
免疫组化:CK7(-),CK20(+),CDX-2(+),CK19(+), Glypican-3(-),Ki67(+,80%)。支持肠道来源。
基因检测:KRAS、NRAS、BRAF V600E 基因检测均为野生型。
术后诊断:降结肠癌术后化疗后肝转移, rT3N0M1a,IVa 期,pMMR,KRAS/NRAS/BRAF
术后全身治疗
2017-2~2017-6行CapeOX方案治疗6程,耐受性差,出现Ⅱ~Ⅲ°骨髓抑制及Ⅱ°恶心、呕吐。
2017-7~2017-8 行卡培他滨单药治疗 2 程。
疗效评价-NED
2017-8 复查 肿瘤标志物:CEA:1.5ng/ml;CA19-9:11.9U/ml。
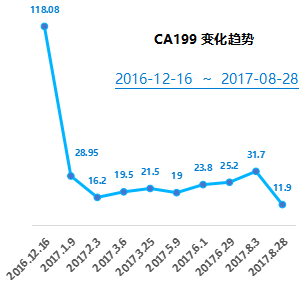
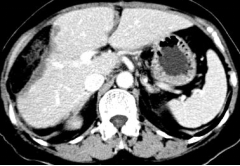
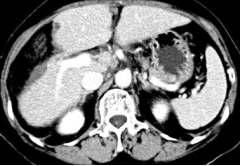
术后2017-2-5
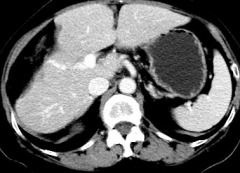
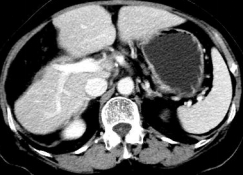
8程术后化疗后2017-8-4
胸腹盆腔CT:肝呈术后改变,未见肿瘤复发转移。
随访:
术后肿瘤标志物正常,CT、MR未见明显肿瘤残留征象,达到NED。
术后化疗结束后2017-8~2018-3定期返院随访。
2018-3复查:肿瘤标志物:CEA:2.3ng/ml;CA19-9:8.6U/ml。
2018-3-25(普美显)肝脏MR:肝右前叶下段近术缘后方新发转移瘤,大小约0.4╳0.5cm。
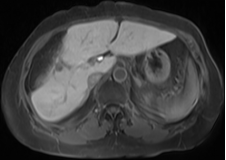
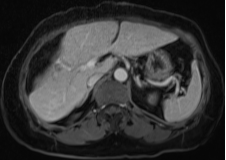
2018-3-25(普美显)肝脏MR:肝右前叶下段近术缘后方新发转移瘤,大小约0.4╳0.5cm。
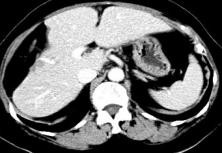
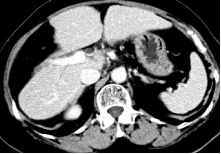
2018-3-21全身CT:肝右叶新发转移瘤,余颅脑、胸部、盆腔未见明确异常。
疗效评价-PD
第一次院内MDT
患者评估:降结肠癌术后化疗后肝转移,
rT3N0M1a,IVa期,pMMR,KRAS、NRAS、BRAFV600E野生型
肝内新发转移灶1枚(大小约0.4╳0.5cm)
患者68岁,ECOGPS:1分,多年高血压病史,
既往服用卡培他滨期间出现II度恶心、呕吐不适
治疗建议:
局部治疗:行手术治疗或射频消融
二线治疗:可考虑联合西妥昔单抗+伊立替康+雷替曲塞方案治疗
治疗目标:NED
局部治疗2018-3-28行肝转移瘤射频消融术。
术后因个人原因未能按时返院进一步评估及治疗。
2018-5复查:肿瘤标志物:CEA:5.2ng/ml;CA19-9:14.1U/ml。
2018-5-23全身CT:肝右前叶转移瘤较前增大,余颅脑、胸部、盆腔未见明确异常。
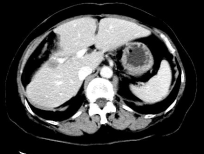
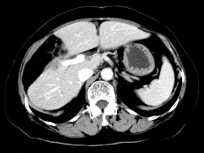
2018-5-23全身CT:肝右前叶转移瘤较前增大,余颅脑、胸部、盆腔未见明确异常
局部治疗2018-5-29再次行肝转移瘤射频消融术。
全身治疗2018-7~2018-12行西妥昔单抗+伊立替康+雷替曲塞方案治疗8程。耐受性差,出现III°骨髓抑制及III°腹泻。
2018-11复查:肿瘤标志物:CEA:4.2ng/ml;CA19-9:16U/ml。
胸腹盆CT:肝右前叶转移瘤较前缩小,余未见肿瘤复发。
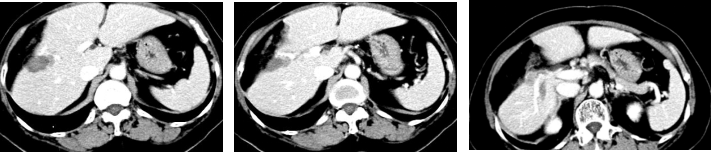
2018-07-06化疗前
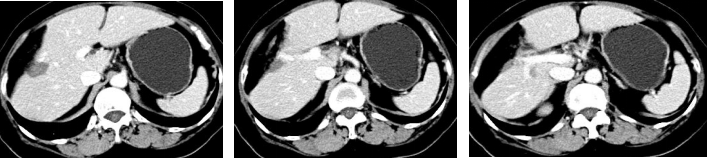
2018-09-03 3周期化疗后
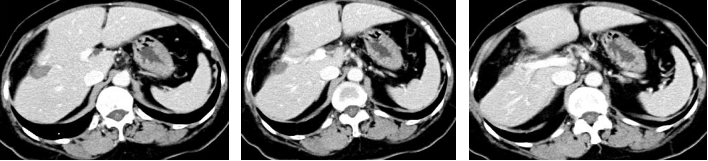
2018-12-27 8周期化疗后
疗效评价-PR
维持治疗
考虑肝脏复发风险高,2019-01~2019.11行西妥昔单抗+雷替曲塞方案治疗12程。耐受性可,无明显不适反应。
2019-11 复查:肿瘤标志物:CEA:3.2ng/ml;CA19-9:16.7U/ml。
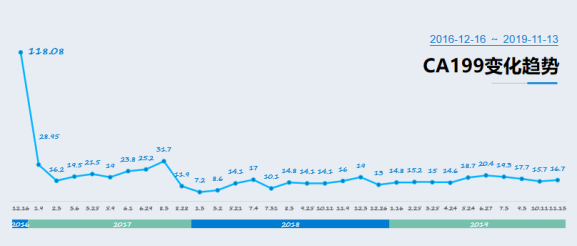
全身CT:肝内新发一转移瘤,大小约21 ╳ 19mm ,余未见明确异常。
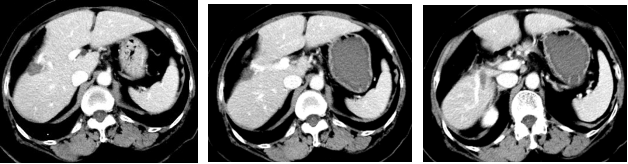
维持治疗6程后2019-5
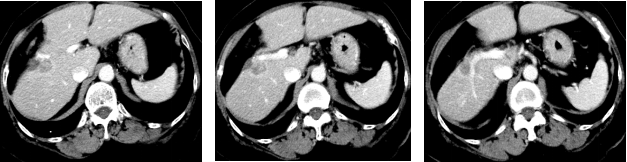
维持治疗12程后2019-11
疗效评价-PD
第二次院内MDT
患者评估:
降结肠癌术后化疗后肝转移,
rT3N0M1a,IVa期,pMMR,KRAS、NRAS、BRAFV600E野生型
肝内经射频消融转移灶旁出现新发病灶(大小约2.1╳1.9cm,邻近血管)
患者69岁,ECOG PS:1分,多年高血压病史,不愿意接受强烈治疗
治疗建议:
行局部治疗:手术或射频消融+放疗
可考虑予贝伐珠单抗联合氟尿嘧啶类药物维持治疗
治疗目标:NED
局部治疗2019-11-20行肝转移瘤射频消融术。
2019-12~2020-01行肝转移瘤立体定位放疗
2020-3复查:
胸腹盆CT:肝右叶病灶治疗后改变,增强扫描未见强化。
PET-CT:肝脏呈治疗后改变,肝右叶混杂低密度灶,未见代谢。
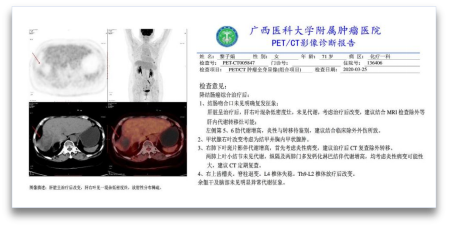
疗效评价-NED
维持治疗
2020-2~2021-11 行雷替曲塞单药治疗。
耐受性可,无明显不适反应。
2021-11 复查:
肿瘤标志物:CEA:5.68ng/ml;CA19-9:52.8U/ml。
胸腹盆CT:肝右叶病灶上缘新发转移灶,双肺新发小结节。
患者不考虑进一步治疗,2021-11~2022-8观察。
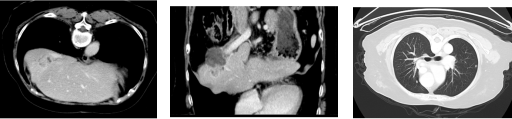
2021-11-16CT
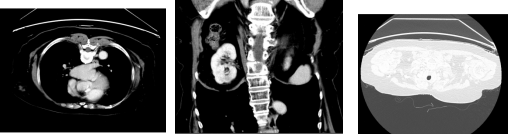
2022-8-29CT
疗效评价-PD
第三次院内MDT
患者评估:
降结肠癌术后化疗后肝转移综合治疗后肝、双肺多发转移,
rT3N0M1b,IVB期,pMMR,KRAS、NRAS、BRAFV600E野生型
肝内再次出现新发病灶,双肺多发转移结节
患者72岁,ECOGPS:2分,既往已行多线治疗,不适合强烈治疗
治疗建议:TAS-102+贝伐珠单抗全身系统治疗
全身治疗2022-9~2023-04行TAS-102+贝伐珠单抗方案治疗6周期。耐受性可,无明显不适反应。
2023-03复查肿瘤标志物:CEA:2.18ng/ml;CA19-9:15.7U/ml。
全身CT:双肺转移瘤部分同前、部分缩小,肝内转移瘤较前缩小。
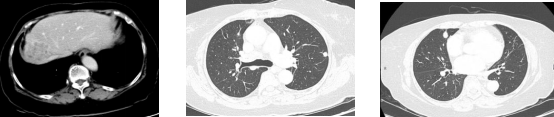
2022-8-29
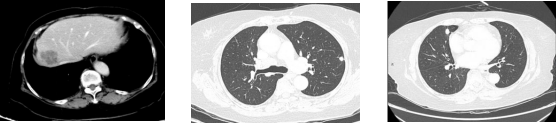
2022-11-03
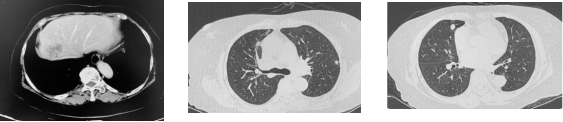
2023-03-09
疗效评价-SD
复查评估2023-05、2023-07、2023-09、2023-11、2024-01
复查全身CT:疗效评估SD。
全身治疗2023-05~2024-01行TAS-102+贝伐珠单抗方案继续治疗10周期。
耐受性可,无明显不适反应。
整体治疗历史回顾
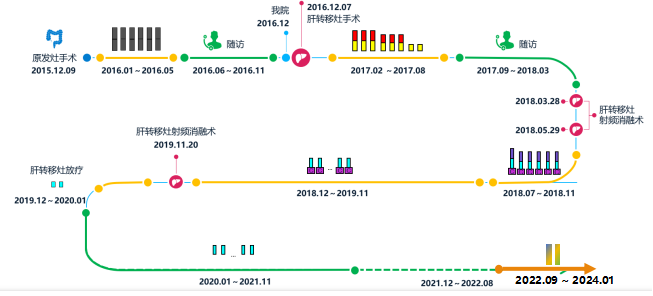
02 病例讨论
问题1:根据该结肠癌肝转移患者2016年12月检查结果,是否建议直接手术治疗?
中山大学附属肿瘤医院MDT团队-影像科-蔡培强:第一次转移病灶挺大,边缘有点凸起,不光滑,临近没有很大的血管。
中山大学附属肿瘤医院MDT团队-肝胆外科-郑云:对结直肠癌肝转移,首先要看肝转移病灶的定位定性和可切除程度,或者说可NED的程度,这个病例是非常成功的,后面手术的选择也是对的。第一次6公分多的转移,CRS 2分,从治疗技术上看,手术是首选的。
中山大学附属肿瘤医院MDT团队-内科-任超:可以切除,建议先行新辅助治疗。在内科的角度来看,因为这次转移距离上次手术时间刚好大概一年,虽然CRS 2分,算低危组,但鉴于转移灶的位置和单个直径超过5厘米的大小,会考虑先做两到三个疗程的一个新辅助治疗,即不加靶向的单纯化疗。
中山大学附属肿瘤医院MDT团队-结直肠科-彭健宏:根据ESMO指南可以直接手术,但考虑到肿瘤大,位置上也占据了肝脏的一大部分,直接切除损失的肝脏可能是有点大的,可以用新辅助治疗结节,也降低手术难度。
中山大学附属肿瘤医院MDT团队-病理科-奚少彦:P53为错意义突变型,只是一个参考,不一定准确,整个病例的生物学行为差,所以虽然基因检测是野生型,我们会建议做一个二代测序来看看整个P53的状态和其他的一些基因,可能在治疗策略和肿瘤的预后上提供一些参考。
问题2:该患者行肝右叶转移瘤切除术后经8程化疗达到NED,于2018年3月复查再次发现肝右叶新发转移瘤,下一步治疗方案推荐什么?
中山大学附属肿瘤医院 MDT 团队-影像科-蔡培强:可以看到右肝门脉右前支旁边 出现了一个结节,感觉在切缘旁边。
中山大学附属肿瘤医院 MDT 团队-介入科-张天奇:病人术后一年多出现边缘新发 病灶,首先普美显的应用非常及时,可以帮助我们发现 4-5mm 的小病灶,准确地去定性 定位,对于术后检测新发病灶以及疾病的治疗是非常有价值的。对于这个边缘的局部病灶, 这个地方做消融是有些风险的,因为周围的结构非常复杂,有门脉的右支和右前支的主干。另外在一个层面是有看到胆道扩张,该病例可能是基于此选择了射频消融。这边可能不会 建议做消融,会请外部专家看看能否做一个小的腔镜下手术,或者考虑放疗。纵观病人后 来的一系列治疗,病灶总是出现在这个部位,其实总在这一个区域局限的话,相当于这个 生物学行为还是给了我们很多治疗机会的。
中山大学附属肿瘤医院 MDT 团队-放射治疗科-王俏镟:病灶较小,一公分左右, 这种位置贴边,近大血管,放疗是比较安全有优势的。而且患者后续这个位置又出现进展, 反过来也印证了这次消融可能不是特别彻底。
中山大学附属肿瘤医院 MDT 团队-肝胆外科-郑云:肝右前叶基本切完了,不像术 后复发,像新发转移。不会考虑二次手术,因为该病人做过一次手术,粘连很厉害,二次 手术的创伤很大,可能开到病灶的时候出不少血。如果做消融,前面大网膜覆盖,超声可 能看不到,只能行 CT 引导下消融。射频消融关注胆道风险,不是说靠近血管就不能做, 最重要的是保证右前叶右后叶的交会分布和后叶胆道的完整。临床上肠癌肝癌我会更提倡 微波消融。当然 SBRT 范围可能更大一点,保护胆道更好,确实是个很好的选择。
中山大学附属肿瘤医院 MDT 团队-内科-任超:病灶很小,不到 1cm,距离上次治 疗 7、8 个月左右,没有必要行新辅助治疗。术后也没必要用很强的特殊辅助治疗,可能 会选择单药的卡培他滨或者定期观察。
问题3 :患者经三线治疗后于2021年11月复查再次发现肝右叶病灶上缘新发转移灶,此时的治疗目标和策略是什么?
中山大学附属肿瘤医院 MDT 团队-影像科-蔡培强:前后一年肝内病灶发展比较稳定。
中山大学附属肿瘤医院 MDT 团队-内科-任超:虽然治疗多次复发,但其实总体肿瘤负荷 并不大,并且现在很难说追求 NED 了,那这时候我们也会用一个相对弱一点的方案,就 有点像维持治疗这种模式。考虑到在第二轮用药时候的耐受性差,估计治疗过程中换药比 较辛苦,那对于这个患者肿瘤负荷不大,没必要变得这么快又去遭受一轮痛苦,先用弱的 方案能维持住的话,患者会有一个更好的一个生活质量,甚至更方便一点,毕竟贝伐珠单 抗要跑来医院打针,患者可以在家服药,定期做 CT 检查。不过在当时这个年代选择 TAS-102+贝伐珠单抗,当肿瘤又开始迅速增长的时候,再把其他化疗药物引入,从抗肿瘤 治疗角度这样有可能疗效会更好。
问题4:病人的病情还会继续进展,对于下一步进展的治疗建议
中山大学附属肿瘤医院 MDT 团队-内科-任超:可以选择把之前有效的西妥昔单抗再 引入,再加上伊利替康,但患者 PS2 分,有可能治疗强度太高。还可以选择去化疗化的 使用贝伐珠单抗+ PD-1+西达本胺,即靶向免疫药加表观遗传抑制剂,这样对病人身体状 况要求比化疗要低很多。但这里面有两个自费药,要看病人的经济情况能否接受,可以接 受的话在肝转移不是非常严重的情况下可以按照这个方式去进行尝试。但如果发生弥漫广 泛性肝转移就不能随意按照这种模式了。
03 MDT小结
患者是一位 69 岁女性,于 2015 年底首次确诊降结肠腺癌后,16 年底发生肝转移,之 后经历多次复发肝转移、外科放疗等局部治疗和多线药物治疗,至今生存期已达八年余。期 间每次复查发现疾病进展后,院方都召集进行 MDT,全面评估患者状况,根据患者对药物 的耐受性和不良反应,参照治疗方案的更新完善,明晰患者下一步治疗方向,病人多次获得 NED 机会,总体上治疗是非常成功的,获得了较长的生存期,目前患者 TAS-102+贝伐珠单抗 治疗方案的无进展生存期(PFS)已超过 12 个月。
40983 研究也显示,结直肠癌肝转移经过围手术充分治疗达到 NED 以后,两年内复发的 仍然过半,因此对于这类病人应该严密追踪,尽早发现肝内的新发病灶。
莫显伟 述评——广西医科大学附属肿瘤医院
MDT可以规范结直肠癌的治疗,借助多学科团队的通力协作,避免个人倾向性。哪怕从治疗效果很好的病例去复盘也能碰撞出不小的火花,给下一次遇到这种病例的时候提供更多的选择。目前MDT推广是没有问题的,基层医院的MDT从前几年的缺失到现在已经成为了一种风向。而如何提升MDT的质量是关键,MDT应该使更多的病人真正从中获益,而不是变成一种必须执行的流程。因此要通过数据溯源,做好从病例讨论、方案实施到随访的MDT全过程质控,促进龙头单位到基层单位的整个MDT实施规范化,建设更完整的团队并执行。


