Ann. Oncol | SERENA-1试验:评估口服SERD药物卡米司群在ER阳性HER2阴性晚期乳腺癌患者中的安全性和有效性
时间:2024-05-26 13:00:17 热度:37.1℃ 作者:网络
大约80%的绝经后乳腺癌患者为ER阳性,这意味着它们对激素治疗具有响应性,内分泌治疗可以阻断ER驱动的信号,从而抑制肿瘤的生长,目前主要有四种类型的内分泌治疗药物,尽管内分泌治疗在初期疗效显著,但患者往往会出现获得性耐药,特别是通过ESR1突变实现的耐药,氟维司群是第一个批准的SERD药物,但由于其口服生物利用度低,需要肌肉注射,限制了剂量的递送,基于上述限制,有必要开发更有效的口服SERD药物,以实现更高的ER降解活性,并提高治疗效果,卡米司群是正在开发的新一代口服SERD药物,具有潜在的疗效优势,是当前研究的主要焦点。

方法
SERENA-1是一项多中心的Ⅰ期临床试验,分为剂量递增和扩展两个阶段,递增阶段评估了25-450mg卡米司群的剂量安全性,扩展阶段则随机分配患者接受75mg、150mg和300mg 卡米司群治疗,入组的患者为18岁或以上的绝经前或绝经后女性,患有ER阳性、HER2阴性的晚期乳腺癌,且对现有标准治疗耐药或无法耐受,绝经前女性必须在入组前至少4周接受促性腺激素释放激素激动剂治疗,并在试验期间继续使用,所有患者必须已接受过至少1种内分泌治疗但不超过2种化疗,递增阶段按25mg、75mg、150mg、300mg、450mg顺序进行,每个剂量水平评估3-6例患者,扩展阶段绝经后患者按1:1:1随机分配,绝经前患者全部接受300mg治疗。主要终点为安全性、耐受性和药代动力学,次要终点包括抗肿瘤活性和疗效、药代动力学特征、对ESR1突变的影响等。
研究结果
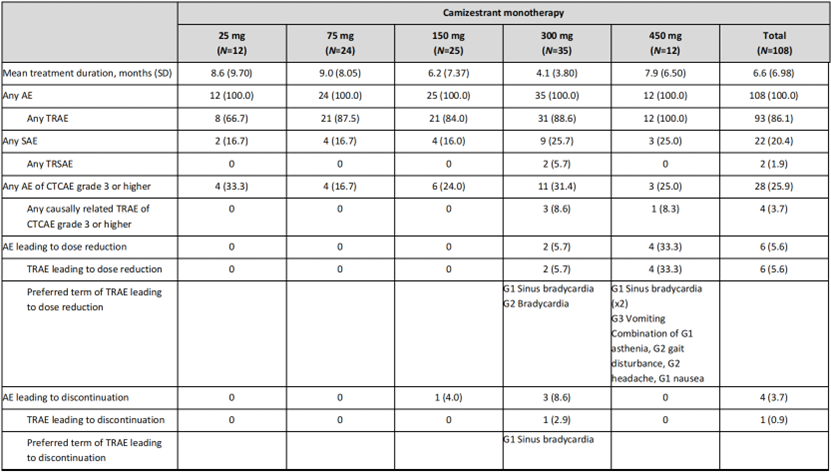
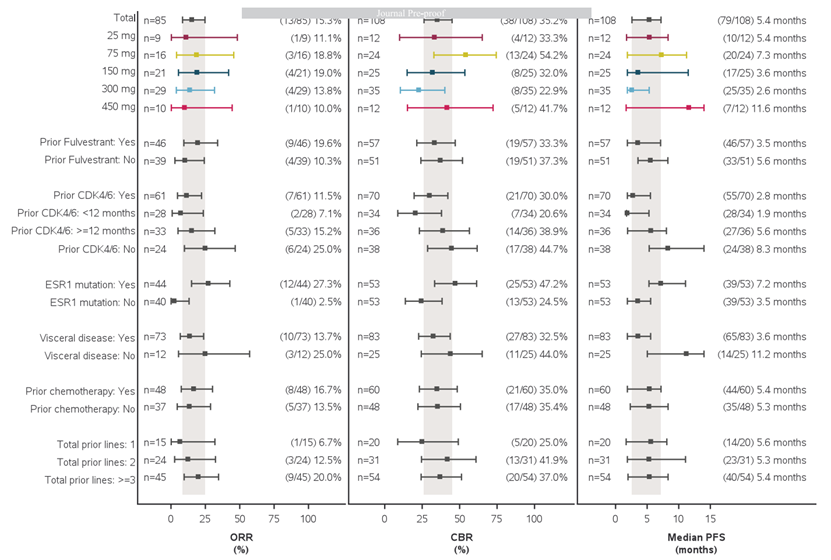
在108名患者中,93名(86%)经历了治疗相关的不良事件,其中82.4%为1-2级,最常见的不良事件是视觉效应(56%)、窦性心动过缓(44%)、疲劳(26%)和恶心(15%),在150mg或更低剂量下,未观察到3级或以上的不良事件,卡米司群的tmax约为2-4小时,半衰期约为20-23小时,25-450mg的剂量范围内,Cmax和AUC0-24随剂量增加呈比例增加,在所有测试剂量下,均观察到了卡米司群的疗效,整体响应率为15.3%,临床受益率为35.2%,中位无进展生存期为5.4个月,在75mg剂量下,响应率为18.8%,临床受益率为54.2%,中位无进展生存期为7.3个月,卡米司群可显著降低肿瘤中ERα、PgR和Ki67的表达,在存在ESR1突变的患者中,疗效更显著,卡米司群可显著降低患者循环肿瘤DNA中的ESR1突变丰度,使其中的大多数变异达到不可检测水平。
结论
卡米司群是一个具有良好安全性和耐受性的下一代口服SERD药物,其药代动力学特征支持每日一次给药,在经过大量预治疗的晚期乳腺癌患者中显示出明显的药效动力学和临床疗效,无论患者是否存在ESR1突变。卡米司群的75mg、150mg和300mg剂量已确定用于进行后续的Ⅱ期临床试验,其疗效与EMERALD试验中口服SERD药物艾拉司群的结果一致,即在ESR1突变阳性患者中观察到更显著的疗效,卡米司群的开发为ER阳性、HER2阴性晚期乳腺癌患者提供了一个新的治疗选择,SERENA-1试验为卡米司群的进一步开发提供了重要的临床数据支持。
原始出处
Hamilton E, et al. 2024. A Phase 1 dose escalation and expansion trial of the next-generation oral SERD camizestrant in women with ER-positive, HER2-negative advanced breast cancer: SERENA-1 monotherapy results. Annals of Oncology.


