The innovation:IBI310(抗CTLA-4抗体)单药或联合信迪利单抗治疗晚期黑色素瘤或尿路上皮癌的I期研究
时间:2024-05-24 10:00:27 热度:37.1℃ 作者:网络
CTLA-4是激活的CD4+和CD8+ T细胞表面表达的分子,其靶向可以诱导抑制性信号,目前唯一获准用于治疗多种人类恶性肿瘤的抗CTLA-4单克隆抗体是伊匹木单抗,黑色素瘤长期以来被认为是免疫原性肿瘤,其死亡率高,中国晚期患者的5年生存率低于5%,伊匹木单抗与纳武利尤单抗联合治疗在西方国家改变了晚期黑色素瘤的临床管理,5年生存率超过50%,亚洲国家中,黏膜和肢端黑色素瘤更为常见,需要获得亚洲患者的临床证据,以了解不同黑色素瘤亚型的遗传背景和疗效差异,IBI310是一种重组全人IgG1抗CTLA-4抗体,与伊匹木单抗氨基酸序列相同,信迪利单抗是一种抗PD-1抗体,在中国已获准用于治疗多种人类恶性肿瘤,该研究报道了IBI310单药或与信迪利单抗联合治疗晚期黑色素瘤或尿路上皮癌的I期剂量递增和扩展研究,评估了IBI310的安全性、耐受性、药代动力学和抗肿瘤活性。

方法
该研究招募了53名18-70岁的晚期、复发性或转移性黑色素瘤或尿路上皮癌患者,ECOG体能状态为0或1,且至少有一个可测量疾病,研究共分为两阶段:单药治疗阶段(Ia)和联合治疗阶段(Ib),Ia阶段使用0.3mg/kg的IBI310,然后采用3+3剂量递增设计,评估1mg/kg、2mg/kg和3mg/kg的IBI310,Ib阶段给予1mg/kg、2mg/kg和3mg/kg的IBI310联合200mg的信迪利单抗治疗4个周期,然后维持信迪利单抗治疗,主要终点是评估IBI310单药或联合信迪利单抗的安全性,次要终点是评估药代动力学特征和抗肿瘤活性,包括响应率、疾病控制率、反应时间、反应持续时间、无进展生存期和总生存期。
研究结果
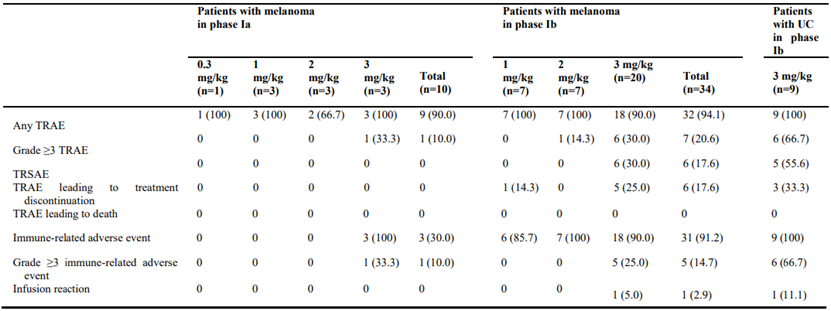
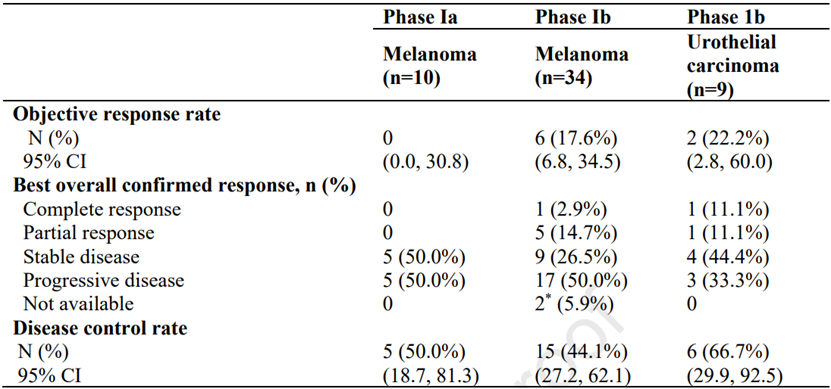
总体来说,94.3%的患者出现至少1种治疗相关不良事件,大多数为1-2级,26.4%的患者出现≥3级TRAE,IBI310单药或联合信迪利单抗治疗具有良好的耐受性。Ia阶段:10名黑色素瘤患者,无CR或PR,SD为50%,DCR为50%。Ib阶段:34名黑色素瘤患者,ORR为17.6%,DCR为44.1%;9名尿路上皮癌患者,ORR为22.2%,DCR为66.7%。IBI310在0.3-3 mg/kg剂量范围内呈线性药代动力学特征,总体来说,IBI310单药或联合信迪利单抗在晚期黑色素瘤和尿路上皮癌患者中显示出良好的安全性、耐受性和抗肿瘤活性。
结论
IBI310单药或联合信迪利单抗治疗在晚期黑色素瘤和尿路上皮癌患者中表现出良好的安全性和耐受性,未发现新的安全信号,值得进一步临床研究。
原始出处
Cui C, et al. 2024. IBI310 (anti-CTLA-4 antibody) monotherapy or in combination with sintilimab in advanced melanoma or urothelial carcinoma. The Innovation.


