脊肌萎缩症:诺西那生治疗的安全性和有效性
时间:2023-11-23 14:25:43 热度:37.1℃ 作者:网络
论坛导读:脊髓性肌萎缩症(Spinal muscular atrophy,SMA)是一种常染色体隐性神经肌肉疾病,其特征是骨骼肌进行性衰弱和萎缩。它是由存活运动神经元(SMN)基因的双等位基因突变(最常见的是缺失)引起的,结果导致SMN蛋白丢失。人类的旁系同源SMN2基因提供了部分拯救;除了5%到10%的成熟SMN2转录物外,外显子7被排除在外,因此只表达有限量的功能性全长蛋白。
由此产生的SMN蛋白不足是SMA表型的原因。SMN2基因拷贝数因个体而异,是疾病严重程度的重要决定因素。
诺西那生钠注射液(Nusinersen)是一种合成的反义寡核苷酸,在欧洲、美国和其他地方被批准用于治疗SMA。Nusinersen通过与内含子内的抑制性剪接位点结合,改变SMN2前信使RNA的剪接,导致外显子7包含在前信使RNA转录物中,从而增加功能性全长SMN蛋白的产量。是全球首款脊髓性肌肉萎缩症(SMA)治疗药物,于2016年获得美国FDA批准上市,用于成人和儿童的脊髓性肌萎缩症的治疗。该药物通过鞘内注射给药,可以直接将药物输送到脊髓周围的脑脊液中,从而改善运动功能、提高生存率,改变SMA的疾病进程。
目前在有症状的个体中使用鞘内nusinersen进行的两项关键的3期试验证明了运动功能的显著和有临床意义的改善以及有利的获益-风险特征。根据症状发作的年龄和两个SMN2基因拷贝,ENDEAR登记的婴儿预测有SMA型。根据症状发作时的年龄,珍惜预测患有II型或III型SMA的入选儿童。培育是一项额外的、持续的、开放性研究;中期数据显示,在症状出现前开始使用nusinersen具有显著的临床益处。
2021年EMBRACE研究结果支持在患有SMA的婴儿和儿童的广泛人群中使用nusinersen作为每4个月一次的维持剂量。在完成EMBRACE的20名参与者中,所有人都参加了综合SHINE方案(NCT02594124),该方案结合了来自早期nusinersen临床试验的参与者进行长期随访。最常见的AE包括发热、咳嗽、肺炎和上呼吸道感染。在最近一次评估中,接受nusinersen治疗的患者的运动里程碑反应率(93%)高于接受第1部分假手术的患者(29%)或从假手术过渡到第2部分nusinersen治疗的患者(83%)。
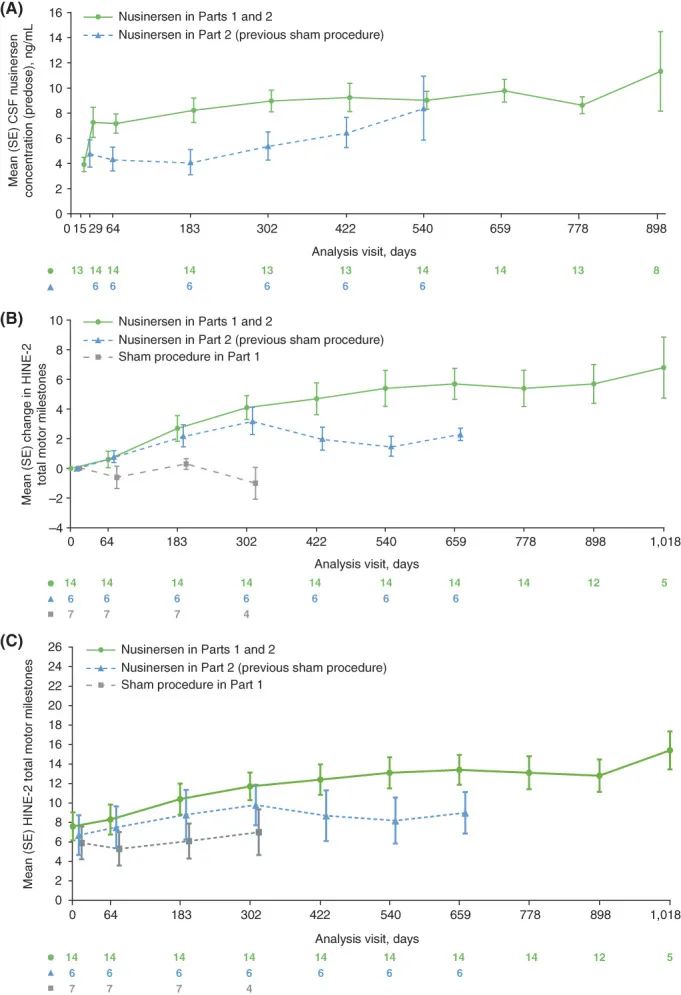
2023年一项研究报告了nusinersen治疗的广泛早发性脊肌萎缩症患者的真实世界证据,重点是在治疗的第一年中对运动里程碑、呼吸和延髓功能不全的影响。在SMArtCARE注册表中,所有接受nusinersen治疗且在治疗开始前从未有独立坐位能力的患者都被确定用于数据分析。这项分析的主要结果是运动功能的变化,用费城儿童医院的神经肌肉疾病和运动里程碑婴儿测试评估,考虑世界卫生组织的标准。此外,我们评估了对呼吸机支持和管饲的需求以及死亡率的数据。总共有143名早发性脊肌萎缩症患者纳入数据分析,随访期长达38个月。我们观察到费城儿童医院神经肌肉障碍婴儿测试评估的运动功能有显著改善。开始治疗时,2岁以上的儿童比年龄较大的儿童改善更大。24.5%的儿童获得了独立坐的能力。在治疗的前14个月中观察到了显著的改善。尽管使用nusinersen治疗,对间歇呼吸机支持和管饲的需求增加。我们的发现证实了越来越多的现实证据,即nusinersen治疗对早发性脊髓性肌萎缩症患者的疾病进展和生存率有显著影响。开始治疗时,小于2岁的儿童运动功能有显著改善。需要密切监测延髓和呼吸功能,因为这些功能的改善不等同于运动功能。
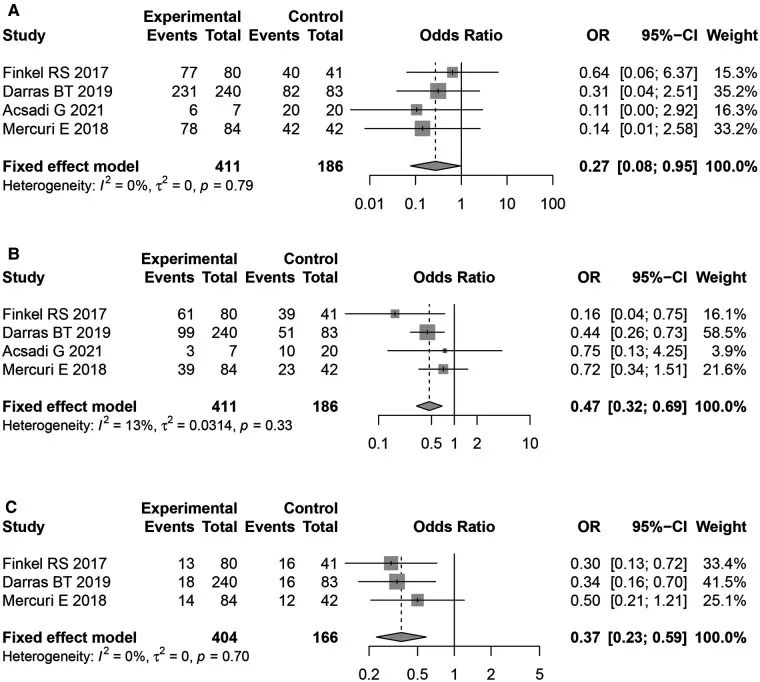
最近一项荟萃分析系统分析了诺西那生钠注射液(Nusinersen)在儿童及青少年的SMA治疗中的不良反应。研究显示诺西那生治疗儿童脊髓性肌萎缩症有运动里程碑改变61.38%(95%Cl:37.60%-82.58%),在治疗过程中发生的不良事件绝大部分为脊髓性肌萎缩症原发病以及相关并发疾病,而明确是诺西那生导致药物不良事件发生率为0.57%,可能是诺西那生导致药物相关性不良事件发生率为7.76%。总体不良事件(大部分为SMA疾病本身)发生率88.67%(95%Cl:72.53%-98.19%),严重不良事件发生率33.04%。在具体不良事件中,发热40.07%、上呼吸道感染39.94%、肺炎26.62%、疼痛22.75%、呼吸衰竭18.77%、,呼吸窘迫17.83%、吸入性肺炎17.83%、呕吐21.4%、便秘19.59%、腹泻28.11%、咳嗽31.81%、胃食管反流10.08%、肺不张16.2%、吞咽困难8.98%、鼻咽炎21.19%、皮疹7.16%、中耳炎12.56%、血小板减少1.81%、腰穿后遗症14.16%。诺西那生纳组和安慰剂对照组中,总体不良事件发生率较安慰组低,有统计学差异(OR=0.27),严重不良事件发生率亦较安慰组低,有统计学差异 (OR=0.47);致命不良事件发生率亦有统计学差异(OR=0.37)。
参考文献
Acsadi G, et al. Safety and efficacy of nusinersen in spinal muscular atrophy: The EMBRACE study. Muscle Nerve. 2021 May;63(5):668-677.
Zhong ZJ, et al. Adverse events in the treatment of spinal muscular atrophy in children and adolescents with nusinersen: A systematic review and meta-analysis. Front Pediatr. 2023 Apr 25;11:1152318.
Pechmann A,et al. Effect of nusinersen on motor, respiratory and bulbar function in early-onset spinal muscular atrophy. Brain. 2023 Feb 13;146(2):668-677.

